Apparato respiratorio UFFICIALE - filippolotti.it ANNO/Apparato respiratorio_UFFICIALE.pdf · •...
Transcript of Apparato respiratorio UFFICIALE - filippolotti.it ANNO/Apparato respiratorio_UFFICIALE.pdf · •...
2
VALUTAZIONE DEL PAZIENTE Avviene mediante:
1. anamnesi 2. esame obiettivo 3. valutazione strumentale
Anamnesi
L’anamnesi è la storia clinica e familiare di un paziente al fine dell’inquadramento diagnostico, si divide in familiare, fisiologica, patologica remota e patologica prossima. Anamnesi familiare → Storia clinica dei parenti di un paziente, esaminata allo scopo di evidenziare eventuali patologie congenite o predisposizioni a malattie ereditarie. Anamnesi fisiologica → Si riferisce all’anamnesi del normale funzionamento dell’organismo. Anamnesi patologica remota → In questo tipo di anamnesi viene domandato al paziente se ha avuto degli interventi precedenti. Inoltre ci interessa sapere in particolare modo se il paziente ha avuto un’epatite, oppure la TBC. Per la TBC chiedere al pz se ha avuto una pleurite; 9 volte su 10 è tubercolosi. Se il paziente ha una malattia infettiva bisogna mettere in atto una serie di procedure. Anamnesi patologica prossima → Bisogna descrivere quello che racconta il paziente con un linguaggio scientifico per descrivere il quadro patologico.
Esame obiettivo
Ricerca dei segni clinici(dati oggettivi apprezzabili con gli strumenti quali fonendoscopio,sfigmomanometro,ecc). Si divide in Generale (aspetto del paziente, della cute,delle mucose,lo stato di idratazione,aspetto del volto) e Distrettuale (Dell’apparato cardiovascolare quindi mediato da strumenti come fonendoscopio,mani;) L’esame obbiettivo va fatto quello di Base e nell’evoluzione infatti non è solo importante come ci si presenta i soggetto al primo esame ma anche i cambiamenti che abbiamo nel corso del tempo. Nell’esame obbiettivo dell’apparato respiratorio è molto importante la Semeiotica fisica:
• Ispezione: si guarda la forma del torace, il tipo di respiro, espansione della gabbia toracica, l’utilizzo dei muscoli accessori come gli scaleni e lo sternocleidomastoideo. Quando questi muscoli prendono parte al processo della respirazione siamo già in presenza di dispnea perché è il tentativo del soggetto di utilizzare altri muscoli per la respirazione perché quelli fisiologici non sono sufficienti.
3
• Palpazione: si valuta il fremito – vocale –tattile. Quando un soggetto parla le onde sonore si espandono sulla superficie del torace e vengono percepite dalla mano messa a piatto sul torace. La modalità di trasmissione delle onde cambia in caso di patologie e quindi ci da informazioni su possibili patologie della gabbia toracica. E’ il classico Dica 33. Se ad esempio un soggetto ha un versamento pleurico le onde si trasmettono in malo modo alla gabbia toracica e quindi vengono percepite meno o per niente dalla mano del medico.
• Percussione: serve per mettere in risonanza le strutture al di sotto delle dita, dal
rumore che si percepisce in risposta alla percussione si stabilisce il contenuto di aria a livello del polmone e la presenza o meno di altre condizioni che riducono la quantità di aria. Il suono in presenza di un versamento pleurico sarà diverso rispetto ad un enfisema dove la quantità di aria è aumentata.
• Auscultazione: si percepisce il suono fisiologico che si chiama murmure vescicolare, è
il rumore che fa l’aria fisiologicamente entrando negli alveoli. Il rumore può essere alterato e pio ci possono essere dei rumori aggiunti che possono essere secchi o umidi. Secchi sono di derivazione pleurica o bronchiale e sono di vario tipo: fischi, sibili, ronchi, si percepiscono soprattutto in caso di asma. Umidi: sono rantoli e crepitii e si verificano quando siamo in presenza di liquido infiammatorio o non, classica è la presenza nella broncopolmonite.
4
INDAGINI DIAGNOSTICHE
Diagnostica per immagini
• Radiografia La tecnica si basa sulla formazione di un’immagine per annerimento di una pellicola fotografica, abitualmente ortocromatica, cioè impressionabile solo da alcune lunghezze d’onda, da parte di un fascio di radiazioni variamento assorbite al passaggio attraverso al corpo umano. I raggi X traenti origine si propagano in linea retta, incontrando un ostacolo, il fascio viene assorbito in misura più o meno elevata in rapporto alla quantità e alla qualità del materiale attraversato. Attraversando un solido non omogeneo, quale il corpo umano, il fascio che emerge si presenta in alcune zone attenuato, in altre poco modificato, in relazione appunto alla quantità e alle caratteristiche dei diversi elementi presenti nella regione attraversata. Il calcio, elemento presente in notevole quantità nel tessuto osseo, assorbe in modo considerevole il fascio: quindi la porzione di pellicola sottostante un segmento osseo sarà poco annerita, in quanto colpita da una quantità modesta di radiazioni. I tessuti molli, costituiti in prevalenza da idrogeno, ossigeno, e carbonio assorbono in modo assai più modesto il fascio; la pellicola sottostante si annerirà in misura maggiore. Queste caratteristiche suggeriscono le indicazioni attuali all’impiego della radiologia tradizionale, che è da utilizzarsi ove esistono forti contrasti naturali, (torace e apparato scheletrico soprattutto). Invece la radiografia è inadatta allo studio degli organi parenchimatosi (fegato, pancreas, cervello…) così come i muscoli. La radiografia del torace è l’esame diagnostico più comunemente utilizzato per l’indagine delle malattie respiratorie. Fornisce informazioni sul parenchima polmonare, la pleura, le vie aeree e il mediastino, ma può anche evidenziare alterazioni delle strutture ossee. Molte strutture dotate di basso contrasto naturale possono essere studiate con un artificio, creando cioè un contrasto artificiale. Questo si realizza con l’impiego di cosiddetti mezzi di contrasto che sono sostanze le quali, introdotte in cavità naturali o in sistemi di conduzione (vasi, tubo digerente …) creano artificiosamente un livello di contrasto tale da poter essere rilevato dalla radiografia. Il mezzo di contrasto intravasale rende opaco il territorio vasale in cui è stato introdotto; si realizza così le arteriografie (studio delle arterie), la sostanza introdotta in un vaso viene poi eliminata dai reni. Il mezzo di contrasto è introdotto in una vena: nei reni viene eliminato per filtraggio e avviato lungo i calici, la pelvi e l’uretere sino alla vescica. Questa progressione rende tali strutture anatomiche visibili e quindi clinicamente studiabili. Oltre mezzi di contrasto opachi, come quelli impiegati in tutte le indagini suddette, possono essere usati mezzi trasparenti, per lo più gas, realizzando indagini contrastografiche denominate variamente: pneumoperitoneo, pneumomediastino. Queste ultime contrastografie sono oggi meno praticate che in passato, in quanto sostituite con esami meno invasivi. I limiti della radiologia convenzionale sono soprattutto connessi alla sua limitata risoluzione di contrasto, che ostacola particolarmente lo studio dei parenchimi. Le controindicazioni sono legate ai danni biologici che le radiazioni ionizzanti possono indurre, sia a dosi elevate sia a dosi moderate. A causa degli effetti biologici dannosi sono controindicati gli esami inutili.
5
• (TAC) Tomografia assiale computerizzata La metodica utilizza un fascio di fotoni X prodotti da un tubo, che attraversa una sezione corporea seguendo traiettorie diverse. Tramite una complessa analisi dei dati, l’elaboratore è in grado do fornire sezioni trasversali che, in sequenza, forniscono una rappresentazione fedele del corpo umano, ciascuna sezione prende il nome di scansione assiale. La tac viene impiegata nello studio di tutte le regioni del corpo umano e presenta alcuni limiti per quanto riguarda lo studio dell’apparato cardiovascolare e del midollo.Di notevole importanza è l’impiego della tac in campo oncologico. La metodica viene utilizzata per la diagnosi e per la stadiazione dei tumori di tutti i distretti del corpo. L’estrema utilità dell’indagine è dovuta alla sua capacità di distinguere il tessuto neoplastico anche quando questo presenta caratteristiche simili alle strutture limitrofe. La risoluzione della metodica viene ulteriormente amplificata dall’impiego di mezzi di contrasto iniettato per via endovenosa durante l’esame, quando la sostanza è presente in concentrazione elevata nel compartimento vascolare, accentua ulteriormente le differenze di densità tra i diversi tessuti.
• Scintigrafia
La scintigrafia polmonare permette l’acquisizione di immagini del polmone dopo la somministrazione di isotopi radioattivi per via inalatoria o endovenosa. Il suo impiego più importante è nello studio della malattia embolia polmonare per mezzo della combinazione di due distinte metodiche: la scintigrafia endovenosa di microaggregati di albumina marcata, di individuare le aree polmonari non per fuse. La scintigrafia polmonare ventilatoria, invece, permette di studiare la ventilazione delle diverse regioni polmonari con la somministrazione per via inalatoria di xenon radioattivo. Dal confronto delle immagini ottenute con le due metodiche si può distinguere un’embolia polmonare.
• Risonanza magnetica La risonanza magnetica sfrutta la perturbazione indotta da onde elettromagnetiche su di un sistema. Una caratteristica della risonanza magnetica è quella della multiplanarietà, cioè la possibilità di eseguire scansioni su tutti i piani dello spazio. Indicazioni all’esecuzione della risonanza magnetica sono essenzialmente lo studio dell’encefalo, dell’apparato ateo-articolare e del midollo. Sono controindicazioni assolute all’esecuzione di una risonanza magnetica la presenza di pace-maker, di corpi estranei ferromagnetici o clips metalliche vascolari. Sono controindicazioni relative la gravidanza.
• Angiografia L’angiografia è una indagine radiologica che consente lo studio dei diversi distretti vascolari mediante l’opacizzazione dei vasi, utilizzando mezzo di contrasto iniettato selettivamente nel lume del arterioso o venoso attraverso un catetere. Già l’anno successivo alla scoperta dei raggi X veniva dimostrata la possibilità di visualizzare radiograficamente vasi arteriosi o venosi, iniettati con sostanze radiopache. Nacque così l’angiografia che consentì i primi studi delle arterie (arteriografia) e delle vene (venografia). Tale procedura consiste, previa anestesia locale, nella puntura del vaso, in
6
genere viene utilizzato l’arteria femorale, mediante un ago costituito da una cannula metallica con all’interno un mandrino appuntito. La puntura è effettuata fino a trapassare la parete del vaso; in seguito, rimosso il mandrino, l’ago viene lentamente sfilato. A questo punto all’interno dell’ago viene fatta scorrere una guida metallica fino in aorta addominale, sulla guida dopo aver sfilato l’ago, si introduce il catetere agiografico. L’angiografia è applicabile a quasi tutti i distretti del corpo: cuore, arterie coronarie, polmoni, encefalo, vari organi dell’addome. Le indicazioni principali dell’angiografia riguardano le malattie intrinseche delle arterie e delle vene. I vasi possono andare in contro a delle malattie che modificano il loro calibro. La stenosi del loro calibro sono dovuti a processi degenerativi di invecchiamento. In alcuni pazienti e possibile affiancare alla fase diagnostica la fase terapeutica, intervenendo mediante l’iniezione con il catetere posto nella sede del sanguinamento di materiale particolari che occludono il punto dal quale si ha l’emorragia. Le stenosi arteriose possono essere dilatate con l’impiego di cateteri a palloncino i quali vengono distesi all’interno del tratto stenotico, permettendo di ripristinare il calibro originario del vaso. Tale metodica è denominata angioplastica.
• Ecografia L’ecografia non utilizza radiazioni ionizzanti, ma onde elastiche, gli ultrasuoni, identiche alle onde sonore. Il fascio ultasuonico nell’attraversare la materia viene infatti riflesso ogni qualvolta incontra una superficie di separazione tra parti non omogenee. Nei liquidi omogenei, dunque, il fascio si propagherà senza alcuna sensibile attenuazione e riflessione, mentre nello studio dei vari parenchimi i fenomeni di riflessione e di attenuazione saranno tanto maggiori quanto più sensibile sarà la discontinuità dei tessuti attraversati e quanto più numerose saranno le superfici di separazione tra mezzi a differenza impedenza acustica. Questa è la ragione per cui le raccolte liquide e le cisti risultano ben distinguibili dalle formazioni solide. Nello studio degli organi superficiali non è richiesta alcuna preparazione specifica per il paziente. Per quanto riguarda l’esame degli organi addominali, il meteorismo intestinale costituisce un ostacolo all’esame ecografico, in quanto il fascio ultrasonoro viene totalmente riflesso dal gas intestinale. L’ecografia della regione pelvica richiede una completa distensione della vescica, che viene utilizzata come finestra acustica, per la visualizzazione degli organi pelvici.
• PET
Sigla di Positron Emission Tomography, tomografia a emissione di positroni, metodo radiologico che mira all’ottenimento di immagini nitide con l’utilizzo di radioisotopi emettitori di positroni. Può essere utilizzata per lo studio del metabolismo delle cellule cerebrali, oltre che in campo cardiologico e oncologico (per esempio per la diagnosi differenziale tra benignità e malignità nel caso di un nodulo solitario polmonare). Si utilizzano in genere molecole di glucosio marcato, che si concentrano nelle zone di tessuto ad alto metabolismo, come le cellule tumorali. Oltre all'impiego diagnostico, la PET ha in sè un potenziale terapeutico, in quanto riesce a irradiare la zona dove si concentra.
7
Mezzo di contrasto(MdC): Sostanza inserita nell’organismo per varie vie essenzialmente orale o per via endovenosa, e che serve a dare un maggiore contrasto alle varie strutture. Se si inietta per via EV avrò che questo arriverà prima nelle strutture più vascolarizzate. Es in una Tac con MdC viene evidenziata attraverso la zona più opacizzata(la zona bianca)che assorbe più raggi X. Evidence Base Medicine: La medicina basata sull’evidenza ovvero curare il paziente in base alle informazioni che si rilevano in base alla ricerca Medico scientifica (in base quindi agli studi clinici). Questo perché spesso la medicina è basata su consuetudini che non sempre sono sostenute dalle evidenze scientifiche , ma che vengono tramandate. Linee guida: sono consigli elaborati da esperti che danno dei suggerimenti su come si deve procedere in certe situazioni. La linea guida si applica in generale ma comunque deve essere considerata anche la complessità del paziente.
8
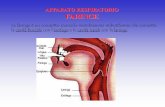
APPARATO RESPIRATORIO La funzione principale dell’apparato respiratorio consiste nel rifornire l’organismo di ossigeno, necessario per la produzione di energia, e nell’eliminazione dell’anidride carbonica, prodotto di scarto del metabolismo cellulare. Oltre allo scambio dei gas, l’apparato respiratorio svolge anche altre importanti funzioni, quali il mantenimento, insieme al rene, dell’equilibrio acido-base e la difesa contro le particelle e i microrganismi inalati. Anatomia delle vie respiratorie L’aria entra attraverso il naso o la bocca, quindi attraversa la faringe, supera la glottide e poi, tramite la laringe, raggiunge l’albero tracheo-bronchiale. La trachea è un condotto fibromuscolare formato da anelli cartilaginei che si divide a formare il bronco destro e il bronco sinistro. Successivamente i bronchi si dividono in bronchioli, nei quali cominciano ad essere presenti alcuni alveoli. Le vie aeree, a eccezione della faringe, della regione anteriore delle fosse nasali e dei bronchioli respiratori, sono rivestite da un epitelio cigliato ricoperto da muco. Il movimento delle ciglia provoca la progressione del muco e delle particelle inalate ristagnanti nelle vie aeree verso la faringe. Questo meccanismo di rimozione è coadiuvato dalla tosse. Nell’alveolo avvengono gli scambi gassosi tra l’aria inspirata e il sangue capillare. La superficie alveolare è costituita da un sottile strato di cellule epiteliali squamose intervallate da cellule cuboidali, che producono il surfactante. Esiste anche un terzo tipo di cellule, i macrofagi alveolari, che svolgono un’azione di difesa. Il surfactante è fondamentale per la normale funzionalità alveolare; abbassando la tensione superficiale degli alveoli, ne stabilizza la struttura, impedendo così il loro collasso. La mancanza del surfactante alveolare nei polmoni dei bambini nati prematuramente è la cusa della sindrome da di stress respiratorio del neonato, così come il danno infiammatorio e ipossico delle cellule alveolari, e il conseguente deficit alveolare di surfactante, sono importanti fattori nella genesi della sindrome da di stress respiratorio acuto. Il polmone ha una doppia vascolarizzazione. Il flusso ematico polmonare che giunge al polmone tramite l’arteria polmonare è costituito dall’intera portata del ventricolo destro e consiste nel sangue venoso refluo dai tessuti dell’organismo; è il sangue che giunge agli alveoli e partecipa agli scambi gassosi. La circolazione bronchiale irrora parte dell’albero tracheo-bronchiale, fino ai bronchioli terminali, con sangue arterioso proveniente dall’aorta. I bronchioli respiratori, i dotti alveolari e gli alveoli vengono ossigenati dall’aria alveolare e nutriti dal sangue venoso misto della circolazione polmonare. Fisiologia della respirazione Lo scambio gassoso tra gli alveoli e i capillari avviene per diffusione attraverso la barriera alveolo-capillare in modo passivo, secondo i gradienti di concentrazione dei gas stessi. L’ossigeno diffonde Dall’aria inspirata (dove ha una pressione, PO2, di circa 150 mmHg ), al sangue venoso capillare (PO2 circa 40 mmHg). L’anidride carbonica diffonde dal sangue capillare (dove ha una pressione, PCO2, di circa 45 mmHg) all’aria inspirata (PCO2 0 mmHg). La ventilazione alveolare porta ossigeno nel polmone e rimuove l’anidride carbonica, mentre il sangue capillare polmonare scarica anidride carbonica negli alveoli e assume ossigeno;
9
l’efficienza di questi scambi dipende da valori ottimali della ventilazione alveolare e della per fusione dei capillari polmonari. I polmoni sono costituiti da materiale fibroelastico e si trovano all’interno della gabbia toracica, separati da essa per mezzo di due foglietti sierosi, uno dei quali riveste la superficie esterna polmonare, (pleura viscerale), mentre l’altro ricopre la superficie interna della parete toracica (pleura parietale). I foglietti racchiudono uno spazio virtuale (spazio pleurico).
MANIFESTAZIONI CLINICHE DELLE MALATTIE RESPIRATORIE Tosse: Espirazione “esplosiva” che rappresenta un meccanismo di protezione per liberare le vie aeree di secrezioni o materiale estraneo, la tosse è un violento atto espiratorio a glottide chiusa. La brusca contrazione dei muscoli espiratori e della parete addominale provoca un improvviso aumento della pressione intratracheale, con successiva apertura della glottide e violenta fuoriuscita dell’aria dai polmoni. Può essere volontaria o riflessa Stimoli alla tosse
1. Agenti irritanti che raggiungono le vie aeree per inalazione (fumo, poveri, vapori) o per aspirazione (secrezioni delle vie aeree superiori, corpi estranei, contenuto gastrico).
2. Infiammazione (bronchiti) 3. Stenosi o costrizione (asma) 4. Compressione delle vie aeree (linfonodi, aneurismi) 5. Infiltrazione (neoplasie) 6. Edema
La tosse può essere secca e non accompagnata da emissioni di secrezioni. La tosse umida (anche detta rosse grassa) è caratterizzata dalla presenza di secrezioni nell’albero bronchiale e i colpi di tosse sono in genere seguiti dalla loro eliminazione. Espettorato L’espettorato è costituito da materiale proveniente dall’albero bronchiale, generalmente emesso con i colpi di tosse. A seconda della sua natura se ne distinguono diversi tipi:
1. Espettorato mucoso, di colore bianco, vischioso, costituito quasi esclusivamente da muco.
2. Espettorato muco-purulento, di aspetto più torbido, e di colore che può variare dal giallognolo al verdastro per la presenza di leucociti frammisti a muco; si ritrova nella gran parte delle affezioni respiratorie.
3. Espettorato sieroso, schiumoso, spesso per la presenza di sangue; si riscontra nell’edema polmonare.
10
Emottisi: L’emottisi è l’emissione, genere in seguito a colpi di tosse, di sangue puro o frammisto a muco proveniente dalle vie respiratorie. Il sangue è generalmente rosso chiaro perché arterializzato, cioè ricco di ossigeno, e spesso schiumoso poiché si mescola con l’aria dei polmoni. Si riscontra nei tumori polmonari, nella tubercolosi polmonare, nell’infarto polmonare, ma anche nelle polmoniti. E’ importante distinguere l’emottisi dall’ematemesi: nell’ematemesi il sangue, proveniente dalle prime vie digestive , viene emesso con il vomito, è scuro, non schiumoso e spesso presenta dei coaguli, inoltre se il sangue viene dallo stomaco avrà un Ph acido. Diagnosi Differenziale: da sangue proveniente dal nasofaringe o dallo stomaco (pH) Cause di emottisi
• Tracheobronchiali - Neoplasie - Bronchiti - Traumi - Corpi estranei
• Parenchima polmonare - Polmonite (es. da germi comuni per distinguerli dal Myco-batterio della tubercolosi) - TBC - Vasculiti (infiammazioni della componente vascolare del polmone)
• Vascolari - Embolia polmonare
- Aumento della pressione polmonare (es. stenosi mitralica (valvulopatia tra l’atrio e il ventricolo sx) provoca un aumento della pressione a livello dell’atrio sx che si ripercuote sulle vene polmonari e sui capillari polmonari e darà un ipertensione polmonare. Quindi ci saranno degli shunt (comunicazioni) attraverso i vasi bronchiali e non solo, che diventeranno più ingranditi ma possono rompersi e quindi dare emottisi)
Dispnea: Una anormale e sgradevole consapevolezza della respirazione (perché comunque tutti hanno la percezione di una respirazione cosiddetta normale)La dispnea è diversa dalla Polipnea cioè l’aumento degli atti respiratori che compare per es. dopo una corsa.
• D. da sforzo - Rapporto con l’entità dello sforzo(quella che compare durante lo sforzo ma che comunque non è proporzionata allo stesso)
• D. a riposo (solitamente aggravamento della condizione da dispnea da sforzo) • D. improvvisa • D. notturna (es. può comparire nell’asma quando questa compare di notte o
nell’insufficienza cardiaca con un quadro chiamato Dispnea Parossistica Notturna (comparsa improvvisa di notte))
11
• Ortopnea (dispnea che costringe il soggetto a mettersi in posizione seduta o eretta. Compare solitamente nell’insufficienza cardiaca quando la persona è in posizione ortopnoica. Da ciò deriva il cosiddetto Decubito Ortopnoico(es. paziente con insufficienza cardiaca che deve stare con la testa sollevata rispetto al tronco per evitare la Dispnea) che farte dell’esame obbiettivo generale )
Cause
• Ostruzione delle vie aeree • Malattie parenchimali diffuse • Malattie della cavità pleurica • Malattie vascolari del polmone • Alterazioni della parete toracica o dei muscoli respiratori • Malattie cardiache
Meccanismi Asma → aumentato senso dello sforzo → irritazione delle vie aeree Bronchite cronica → Sforzo → Ipossia → Ipercapnia → Compressione dinamica delle vie aeree Embolia polmonare → stimolazione di recettori di pressione
12
INDAGINI DIAGNOSTICHE NELLE MALATTIE RESPIRATORIE
Test di funzionalità respiratoria
• Spirometria: Serve per vedere i volumi (quantità)e i flussi (velocità con la quale un liquido oppure l’aria si muove in un certo spazio che si può misurare in litri/sec)respiratori. Definizione dei volumi polmonari:statici, che sono illustrati nella figura 14.6. Durante la respirazione tranquilla si ha ad ogni atto respiratorio la costante immissione ed emissione di una certa quantità di aria, che viene definita volume corrente (VC) ed è pari a circa 500-700 ml nel normale. Un’inspirazione profonda consente di incrementare al massimo il volume polmonare, fino al raggiungimento della capacità polmonare totale (CPT), che è intorno ai 6 l nell’adulto. D’altra parte, prolungando quanto più è possibile la espirazione, si espelle una certa quantità di aria (riserva espiratoria), ma non tutta quella presente nei polmoni. Quest’ultima è detta volume residuo (VR) ed è pari a circa 1200 ml, mentre il volume di aria contenuto nei polmoni al termine di una espirazione tranquilla è definito capacità funzionale residua (CFR). La capacità vitale (CV) corrisponde al massimo di aria ventilabile, ed è ottenuto sottraendo il volume residuo alla capacità polmonare totale (CV = CPT – VR = 5000 ml circa).
Nel grafico sottostante abbiamo in ascissa il tempo e in ordinata i Volumi. La variazione dei volumi rapprsentati nel tempo rappresentano i flussi ovvero la maniera con la quale il volume si modifica nel tempo.
13
RV: volume residuo (1200ml). FRC:capacità funzionale residua VC: capacità vitale TLC: capacità polmonare totale VT: Volume corrente
La spirometria serve quindi sia per evidenziare questi volumi ma anche per misurare come questi si modificano soprattutto durante una espirazione forzata (per evidenziare se c’è un ostacolo all’efflusso cioè alla espirazione di aria dai polmoni). Inoltre la spirometria è importante perché ci consente di dividere le malattie respiratorie in 2 grandi categorie:
• Ostruttive :cioè caratterizzate da un ostacolo all’efflusso di aria.(es. Asma – dove i bronchi sono costretti; Bronchiolite ,ecc)
• Restrittive che si dividono a loro volta in parenchimali ed extraparenchimali. Nelle malattie restrittive il parenchima(la parte funzionale del polmone) polmonare è ridotto Le patologie restrittive parenchimali sono per es. pneumectomia totale cioè asportazione di un polmone; La fibrosi polmonare dove il parenchima è sostituito da tessuto cicatriziale ; Sarcoidosi patologia infiammatoria cronica del polmone dove questo si ritrova ad essere infiltrato da granulomi infiammatori che provocano riduzione dello spazio per lo scambio respiratorio. Nelle patologie restrittive extra parenchimali: la patologia non dipende dal polmone es. trauma toracico con rottura di coste che recidono i vasi intercostali e si accumula sangue nella cavità toracica .Questo sangue tenderà a comprimere i polmoni e collassarli (Emotorace )che non potrà più ventilare o ventilare solo in parte. Un altro es. può essere lo schiacciamento;soggetti con malattie neurovegetative (come la poliomielite- in cui c’è bisogno del polmone d’acciaio) che coinvolgono i muscoli che partecipano alla respirazione (diaframma, intercostali,ecc);
Nel grafico successivo abbiamo sempre i volumi in ordinata e i tempi in ascissa. All’apice delle curve siamo nella situazione in cui il soggetto ha fatto un inspirazione massimale. A questo punto viene invitato ad espirare più rapidamente possibile. Misurando il volume che viene espirato nel primo secondo (VEMS (corrisponde nel disegno alla FEV) e significa volume espiratorio massimo al primo secondo) abbiamo una misura dell’eventuale presenza di una ostruzione all’efflusso di aria. Nella situazione B abbiamo una patologia ostruttiva. Quindi si parte da un volume più alto (perché l’aria viene inspirata correttamente ma non inspirata completamente ) e al primo secondo la quantità di aria espirata(VEMS) è minore rispetto alla normalità. Quindi il polmone tenderà in questa forma ad essere iperinsuflato.
14
Nella situazione C abbiamo una patologia restrittiva. Abbiamo sempre una riduzione della VEMS ma associata ad una riduzione di tutti i volumi. Quindi si parte da un volume più basso rispetto alla normalità e la quantità aria espirata al primo secondo (VEMS)è minore. Nella situazione A abbiamo la respirazione normale.
• Emogasanalisi sistemica:
L’emogasanalisi arteriosa è di fondamentale importanza nella valutazione dell’efficienza degli scambi gassosi. Il prelievo può essere effettuato dall’arteria radiale, brachiale o femorale. Permette la misurazione del pH, della PO2, della PCO2 e dei bicarbonati.
Diagnostica per immagini
• Radiografia • Tomografia computerizzata: (+ HRCT) può essere fatta ad alta risoluzione per vedere
le malattie del parenchima polmonare • Scintigrafia: si usa soprattutto la scintigrafia di perfusione (ovvero per evidenziare
in che modo i polmoni sono per fusi dalle arterie polmonari. Questa è molto importante nella diagnostica dell’embolia polmonare)
• Angiografia: (o Angiopneumografia): si vanno a visualizzare i vasi polmonari soprattutto le arterie polmonari ma in questo caso non si introduce un catetere arterioso, ma venoso attraverso la vena femorale, si risale vena cava, poi si arriva al ventricolo dx, e infine nel tronco dell’arteria polmonare dove viene iniettato il MdC per evidenziare se ci sono dei trombi o emboli,ecc. Inoltre oltre ad essere una tecnica diagnostica è anche terapeutica quando per es. viene utilizzata per dilatare restringimenti di vasi (Angioplastica)
• Ecografia: si usa poco ma può servire per le malattie della pleura es. versamenti pleurici in cui il liquido separa il foglietto parietale da quello viscerale.
• L’endoscopia: può essere sia diagnostica(prelievo materiale biologico) che terapeutica(asportazione di corpo estraneo attraverso delle piccole pinze che vengono
15
fatte passare attraverso un condotto centrale dell’endoscopio oppure ancora somministrazione farmaci, ancora biopsia bronchiale,rimozione stenosi bronchiale,rimozione polipi,ecc). L’introduzione dello broncoscopio si ha (strumento flessibile in fibra ottica alla cui estremità presenta una telecamera) attraverso il naso – trachea – bronchi che va ad evidenziare l’aspetto macroscopico e le alterazioni (sanguinamenti, coaguli, neoformazioni, secrezioni purulente, corpo estraneo) . Durante l’introduzione dall’endoscopio viene spruzzato un anestetico locale che consente al soggetto di tollerare la presenza dell’endoscopio.
Raccolta di materiale biologico
• Analisi dell’espettorato: l’escreato viene raccolto con facilità in caso di tosse produttiva, ma, in alcuni casi per la presenza si scarse secrezioni bronchiali o di tosse poco efficace dovuta alle scadute condizioni del paziente, è necessario stimolare la produzione delle secrezioni con la somministrazione di aerosol si soluzione salina. Le secrezioni bronchiali emesse con la tosse, però, vengono facilmente contaminate da materiale proveniente, dal cavo orale e dalle alte vie respiratorie, e ciò ne rende poco significativo lo studio. Può essere di aiuto l’esame delle cellule presenti nell’escreato: un elevato numero di macrofagi alveolari e leucociti polimorfinucleati indica che il campione proviene dalle basse vie aeree, mentre l’abbondante presenza di cellule squamose epiteliali è indice di significativa contaminazione con le secrezioni delle alte vie aeree.
• Toracentesi: la toracentesi, cioè il prelievo del liquido pleurico mediante puntura della parete toracica, può essere effettuata a scopo diagnostico o a scopo terapeutico (toracentesi evacuativa), al fine di alleviare la dispnea alla presenza di un versamento pleurico.
• Biopsia percutanea: può essere utilizzata quando la toracentesi non permette una diagnosi, in caso si sospetti una tubercolosi o una neoplasia.
• Broncoscopia: la broncoscopia permette, oltre a una visualizzazione diretta dei bronchi, il prelievo di materiale direttamente dall’albero tracheobronchiale e l’esecuzione di biopsie delle vie aeree, del parenchima polmonare e delle strutture mediastiniche. I campioni possono essere prelevati mediante lavaggio (istillazione e riaspirazione di soluzione salina). La broncoscopia può avere, inoltre, finalità terapeutiche, come per esempio la rimozione di corpi estranei, l’interruzione di un sanguinamento mediante catetere gonfiabile o il posizionamento di stent endobronchiali.
• Toracoscopia (VATS): La toracoscopia cioè l’esame della cavità pleurica dopo induzione di pneumotorace, permette di prelevare campioni bioptici. Recentemente il toroscopio è stato utilizzato anche nella chirurgia toracica video-assisstita (VATS).
16
• Mediastinoscopia: Viene utilizzata per il prelievo di campioni bioptici da masse e linfonodi mediastinici.
17
CATEGORIE DIAGNOSTICHE DELLE MALATTIE RESPIRATORIE Ostruttive: Le malattie polmonari caratterizzate da un’ostruzione delle vie aeree, con una conseguente riduzione dei flussi espiratori e, spesso, con un aumento della capacità funzionale residua e del volume residuo, cioè della quantità di gas che rimane intrappolata negli alveoli alla fine dell’espirazione. Le principali malattie responsabili di ostruzioni delle vie aeree sono l’asma, B.P.C.O e bronchiolite.
• Asma • Broncopneumopatia cronica ostruttiva • Bronchiolite
Restrittive parenchimali
• Fibrosi polmonare • Sarcoidosi • Pneumoconiosi • Interstiziopatie
Restrittive extraparenchimali
• Neuromuscolari • Di parete
Restrittive vuol dire che la quantità di parenchima è minore sia che è ridotta la mole di parenchima sia perché sono meno quelle strutture che consentono una regolare espansività del polmone.
18
DISTURBI DEGLI SCAMBI GASSOSI E INSUFFICIENZA RESPIRATORIA
Requisiti per un corretto scambio gassoso:
• Ventilazione: Il processo della ventilazione è quello per cui si ha un’espansione della gabbia toracica dovuta all’azione dei muscoli intercostali e del diaframma e dei muscoli accessori (come gli scaleni, e lo sterno cleido mastoideo) che consente introdurre negli alveoli aria ricca di ossigeno tramite l’inspirazione e di eliminare aria ricca di anidride carbonica durante l’espirazione. Vi è un’alterazione della ventilazione quando vi è un’alterazione neuro-muscolare che impedisce il corretto funzionamento del mantice polmonare.
• Per fusione: gli alveoli sono circondati dai capillari polmonari nei quali circola il sangue
venoso che proviene dalle arterie polmonari. Questo sangue che proviene dal circolo sistemico arriva alle cavità destre del cuore e viene immesso nel circolo polmonare attraverso l’arteria polmonare che poi si dirama, fino ad arrivare attorno agli alveoli dove chiaramente se il sangue non arriva in maniera congrua non avremo un adeguato scambio gassoso.
• Diffusione: Processo per cui il sangue povero di ossigeno (emoglobina a bassa
saturazione di ossigeno) si arricchisce di ossigeno mentre cede anidride carbonica a livello alveolare.
• Rapporto ventilazione/per fusione: infatti gruppi di alveoli possono avere una discrepanza tra ventilazione e perfusione. Esempio:l’emoglobina a livello della giunzione alveolo capillare deve rilasciare CO2 e legare Ossigeno. E’ evidente che c’è bisogno sia dell’ossigeno,sia dell’emoglobina per avere un corretto scambio e basta che non si realizzi una delle due condizioni perché ci sia un alterazione del rapporto ventilazione / perfusione. Es. In una situazione di embolia polmonare nella quale un coagulo o materiale insolubile blocca il flusso arterioso del polmone ,non arriverà il sangue in alcune zone per via dell’ostruzione anche se posso avere comunque un adeguata ventilazione. Questo è un classico esempio di alterazione del rapporto ventilazione /per fusione nel senso che ci saranno alveoli ben ventilati, ma poco per fusi. Altro esempio: bronco polmonite dove avremo che il sangue fluisce a livello dei capillari ma l’aria non arriva perché gli alveoli sono occupati da materiale infiammatorio liquido. Altro esempio: è l’edema polmonare, dove gli alveoli in tal caso sono ben per fusi ma poco ventilati
19
Valutazione degli scambi gassosi a) Emogasanalisi sistemica arteriosa: Si punge con una siringa eparinata l’arteria radiale a livello del polso e si preleva sangue arterioso che sarà analizzato con una speciale macchina detta EMOGAS ANALIZZATORE che ci informa sullo stato dei gas sanguigni. Si fa a livello del polso perché anche se ci sono altri vasi come l’arteria brachiale non si usa perché essendoci intorno il plesso brachiale può risultare doloroso. Quando non si punge la radiale si punge la femorale, arteria molto grossa ma che presenta 2 problematiche: 1) Se il paziente ha una posizione ortopnoica per edema polmonare metterlo disteso per pungere la femorale può essere problematico 2) A livello della radiale c’è un piano osseo sottostante che permette di metterci una garza e di incerottare per evitare l’ematoma (vista la pressione alta dell’arteria di 100 mmHg non ci si può lasciare un cerotto come in una vena)mentre a livello della femorale non essendoci piani ossei il paziente se non è in grado di premere c’è bisogno che l’operatore lo faccia per lui. L’emogasanalisi arteriosa sistemica ci da informazioni riguardo:
• Gas (che ci consentono di valutare l’equilibrio respriratorio) • PH (acidità del sangue).abbiamo quindi informazioni sull’equilibrio acido-base molto
relazionato a quello respiratorio. • OSSIGENAZIONE DEL SANGUE(PaO2) misurato con la pressione parziale di
ossigeno (PaO2 misurata in mm di mercurio). Questa pressione varia con l’età ed è in genere attorno ai 90 mmHg. N.b.Esiste una formula che ci consente di calcolare il valore della PaO2 e consiste nel sottrarre 1/3 dell’età da 103. esempio: in un soggetto con 30 anni 1/3 di 30 è 10 sottrarrò 10 da 103 (103-10= 93) e quindi 93 è la pressione parziale d’ossigeno ideale nel soggetto.
• PRESSIONE PARZIALE DI CO2(PaCO2) si misura anch’essa in mmHg ed è in genere attorno ai 34-38 senza superare 40;
• SATURAZIONE IN OSSIGENO DELL’EMOGLOBINA (VAL.NORMALI: 90-99%)si misura in %, e rappresenta la percentuale dell’emoglobina satura(occupata) di ossigeno . Comunque è proporzionale alla PaO2
• CONCENTRAZIONE ARTERIOSA DEI BICARBONATI HCO3-. In base a tali parametri si valuta se c’è insufficienza respiratoria, se c’è acidosi e se l’acidosi è respiratoria o metabolica ( causata dall’insufficienza renale) o situazioni miste.
L’acidosi infatti può essere compensata o scompensata: il nostro organismo mette in atto meccanismi di compenso per cercare di mettere a posto le cose . La formazione di acido quando c’è insufficienza respiratoria dipende dal fatto che quando c’è un accumulo di CO2 questo determina maggiore formazione di acidi, in quanto la CO2 si trasforma in acido carbonico. A questo punto il rene tenderà a trattenere bicarbonato per compensare questo accumulo di acido. L’acidosi è scompensata quando si ha una diminuzione di PH ( livello di acidità del sangue) al di sotto del 7.34 e in tal caso si parla di ACIDOSI CON ACIDEMIA o SCOMPENSATA.
20
b) Pulsossimetria: si fa grazie ad uno strumento detto pulsossimetro (da puls “polso-battito”, “ossimetro” cioè misuratore di ossigeno)che si posiziona ad un dito (esistono forme anche per il lobo dell’orecchio) e serve per monitorizzare in maniera non invasiva la saturazione di O2. Inoltre ci informa sulla FC (per percepire infatti la saturazione di ossigeno c’è bisogno di rilevare l’onda sfigmica:ovvero il fatto che con ciascun battito il sangue raggiunge la periferica). Esistono anche metodi invasivi per monitorizzare la saturazione, usati in ambienti di terapia intensiva e che prevedono l’incanulazione di un’arteria (nel caso ci sia bisogno di frequenti analisi , per non bucare ogni volta il paziente). La cannula è tappata con tappino eparinato per non dare luogo alla formazione di coaguli ed è collegata tramite un tubicino ad un Emogasanalizzatore. Oltre a tali parametri i moderni strumenti hanno anche una sorta di “mini laboratorio” che ci offre informazioni aggiuntive su: LATTATI, ELETTROLITI, GLUCOSIO,ALTRI(informazioni che possono risultare utili in situazioni di urgenza).
c) Capacità di diffusione: metodica attraverso cui si fanno ispirare al soggetto piccole quantità CO (ossido di carbonio) come tracciante che poi si ricercherà nel sangue. In base a quanto ne viene ritrovato nel sangue si può valutare se il processo della diffusione è normale oppure è alterato. Si fa in genere assieme alla SPIROMETRIA. Esempio: in un soggetto che ha ipossiemia (ridotta pressione parziale di O2 nel sangue). Per capire il motivo farò la spirometria valutando se è una forma ostruttiva, restrittiva oppure se è normale mentre la diffusione del CO ci permette di valutare le condizioni della membrana, quindi se c’è un alterata diffusione dei gas tra alveolo e i capillari alveolari. Il CO è usato perché non è presente normalmente nell’aria ispirata. Soprattutto nell’embolia polmonare ma anche nella BPCO ci sono variazioni nell’emogasanalisi diverse che ci aiutano nella diagnosi.
Figura a: Nell’ipoventilazione alveolare il flusso ematico è normale e avremo quindi tali alterazioni: bassi livelli di pressione parziale di ossigeno nel sangue arterioso e alti livelli di CO2 perché c’è poco arrivo di aria ossigenata e si riesce ad espellere poca aria ricca di CO2. Figura b: Shunt destro-sinistro :situazione limite con zero perfusione dell’alveolo o di un gruppo di alveoli. Infatti il sangue dell’arteria polmonare non ossigenato (venoso) in alcune malformazioni cardiache va direttamente nel circolo del cuore sx senza passare dal polmone.
Questo esempio rappresenta un livello estremo di alterazione ma che comunque è molto raro.
21
Figura c: alterazione del rapporto ventilazione/per fusione dove abbiamo alveoli che sono normalmente perfusi e ben ventilati e alveoli poco ventilati e ben per fusi come avviene nella bronco polmonite. In questo caso succede che fino ad un certo grado della patologia avremo iperventilazione ( in seguito alla tachipnea cioè aumento degli atti respiratori nel soggetto)che può supplire la capacità del polmone di eliminare la CO2 ma ciò nonostante non si riesce a supplire la capacità di ossigenare il sangue. In altri casi possiamo aver ridotta pressione parziale di ossigeno ma una pressione parziale di CO2 normale o addirittura, nell’embolia polmonare in cui inizialmente la ventilazione non è alterata una ipossiemia ( riduzione della pressione parziale di ossigeno nel sangue e un’ipocapnia ( ridotta pressione parziale di CO2 nel sangue) questo perché il soggetto sente la ridotta pressione parziale dell’ossigeno e tende a iperventilare in maniera così efficace da eliminare il sovraccarico della CO2 ma da non riuscire a ossigenare il sangue. Figura d: le alterazioni della diffusione: La membrana risulta più spessa e questo significa che lo spazio tra alveolo e il capillare è ingrossato e quindi la diffusione è alterata. Ciò avviene ad esempio nella fibrosi polmonare nella quale tessuto fibroso si va ad inserire nell’interstizio tra alveolo e polmone compromettendo la diffusione dell’ossigeno più che quella della CO2.
22
INSUFFICIENZA RESPIRATORIA
Si definisce insufficienza respiratoria una significativa riduzione della capacità dell’apparato respiratorio di ossigenare il sangue e di rimuovere l’anidride carbonica. Può essere dovuta ad alterazione degli scambi gassosi intrapolmonari o a un’inefficace ventilazione polmonare. Per convenzione, si parla di insufficienza respiratoria quando la PaO2 è inferiore a 60 mmHg (ipossiemia) e la PaCO2 è superiore a 50 mmHg (ipercapnia), per cause respiratorie. Quindi si ha sempre PaO2<60 nell’insufficienza respiratoria. Il fatto che la ridotta PaO2 sia associata o meno all’aumento della PaCO2 dipende dal fatto che se il processo di ventilazione è alterato si ha un eccesso di CO2 e una mancanza di O2. Quando invece il processo alterato è quello a livello alveolo-capillare ci può essere un alterato rapporto ventilazione/perfusione distrettuale in una zona del polmone in cui arriva sangue e non l’aria con l’O2 ( ad esempio in un caso di bronco polmonite) e quindi il sangue che arriva agli alveoli poco ventilati, ripartirà con poco O2 e tanta CO2. Tutto ciò viene percepito a livello dei centri del respiro encefalici che aumenterà allora il drive respiratorio determinando l’iperventilazione in modo che se le altre zone del polmone sono poco compromesse in modo da eliminare la CO2 in eccesso, nel sangue arterioso la CO2 si riporterà a valori normali, ma l’ossigeno rimane basso. Tutto ciò succede perché la diffusibilità dell’anidride carbonica è molto più alta e generalmente più efficiente rispetto a quella dell’ossigeno e quindi l’iperventilazione compensa molto meglio l’alta CO2 che i bassi livelli di ossigeno Cause di insufficienza respiratoria:
1. alterazione del rapporto ventilazione/perfusione (V/Q) 2. ipoventilazione alveolare 3. shunt destro-sinistro 4. riduzione della diffusione dei gas a livello della membrana alveolo-capillare 5. riduzione della pressione parziale di O2 nell’aria inspirata
Le prime due cause ricoprono il ruolo di maggiore importanza e ricorrono con più frequenza. Tutte le cause di insufficienza respiratoria sono in grado di determinare ipossiemia. Cause di ipercapnia sono l’ipoventilazione alveolare e la grave alterazione dei rapporti ventilazione/per fusione da malattie polmonari gravi. Alterazione dl rapporto V/Q: E’ una frequente causa di ipossiemia nella maggior parte delle malattie polmonari, e più comunemente responsabili sono quelle che determinano una ridotta ventilazione di ampie zone polmonari quali le malattie ostruttive, le polmoniti, le atelettasie e l’edema polmonare. L’ipossia alveolare, dovuta alla ridotta ventilazione, provoca una vasocostrizione locale e una ridistribuzione del flusso sanguigno verso le regioni meglio ventilate; grazie a questo meccanismo, le aree ben ventilate sono anche adeguatemente per fuse e l’emoglobina ne esce saturata di ossigeno. Quando tale meccanismo di compenso non è più sufficiente si ha una riduzione della PaO2. Gravi alterazioni del rapporto V/Q possono causare anche ipercapnia.
23
Ipoventilazione alveolare: E’ la causa più comune di ipercapnia, anche molto severa, accompagnata, comunque, sempre da un certo grado di ipossiemia. L’ipoventilazione alveolare può essere dovuta ad alterazione della attività dei centri respiratori, a malattie neuro-muscolari o scheletriche o ad affaticamento dei muscoli respiratori. La funzione del centro del respiro può essere alterata da gravi malattie cerebrali o per intossicazione da farmaci. Importanti malattie neuro-muscolari sono la poliomielite, la distrofia muscolare progressiva o malattie della gabbia toracica. Shunt destro-sinistro: le cause più frequenti di shunt destro-sinistro intrapolmonare sono le malattie polmonari che causano un’estrema alterazione del rapporto ventilazione/perfusione, con alveoli non ventilati, ma perfusi. Il sangue non entra in contatto con l’aria respirata e giunge nelle cavità sinistre del cuore senza essersi ossigenato e senza essersi liberato di anidride carbonica. Mancando il contatto tra aria e sangue in aree polmonari più o meno estese, l’ipossiemia è scarsamente correggibile anche con elevate concentrazioni di ossigeno. Le cause che non riguardano i polmoni possono essere: 1) SNC es. la poliomielite bulbare ove il snc non funziona bene; si altera in tale situazione il processo della respirazione; avremo infatti un’insufficienza respiratoria ipossica e ipercapnica in fase avanzata. 2) MIDOLLO SPINALE nel midollo abbiamo i motoneuroni che controllano i muscoli che permettono l’espansività della gabbia toracica tra cui il diaframma. Le alterazione del midollo potranno essere dovute a traumi della colonna vertebrale, poliomielite, sclerosi multipla. Anche qui c’è deficit ventilatorio. 3) STRUTTURE NEURO MUSCOLARI: non riguardano solo i neuroni ma tutte le strutture che si possono alterare ad esempio per neurite periferica, botulismo ,tetano(malattie muscolari della placca neuro muscolare. ). Queste malattie impediscono al muscolo di contrarsi correttamente, 4) PARETE TORACICA dove si avrà un deficit ventilatorio dove nel caso del pneumotorace siamo nell’ambito di un’insufficienza respiratoria perché interessa anche il polmone. 5) VIE AEREE SUPERIORI O PARENCHIMA riguardano il polmone in prima persona. 6) SISTEMA CARDIO VASCOLARE es. embolia polmonare o edema polmonare cardiogeno perché se il polmone si riempie di liquido avremo un’alterazione respiratoria ma per una causa di origine cardiaca. N.B. L’ OSSIGENOTERAPIA In un soggetto che ha problemi di ventilazione o comunque un’insufficienza respiratoria ipossica e ipercapnica, aumenta la pressione parziale d’ossigeno ma la CO2 rimane comunque alta, vista l’alterazione ventilatoria. Quindi nell’emogasanalisi saremo di fronte a valori adeguati di O2(grazie all’ossigenoterapia), ma la CO2 rimarrà sempre alta. Questo perché miglioro l’ossigenazione ma non agisco sulla ventilazione. In tal caso mi trovo di fronte a un ipercapnia pur non essendoci una ipossiemia che può essere molto dannosa.
25
L’insufficienza respiratoria si divide in: Ipossiemica (ridotta PaO2<60mmHg) Cause:
• Edema polmonare • Embolia polmonare • Asma bronchiale
Forme dove primitivamente è alterata la ventilazione es. soggetto con l’asma e che ha dispnea x ore, avrà ad un certo punto affaticamento dei mm. Respiratori con successivo deficit respiratorio. Ipercapnica (aumentata PaCO2>50mmHg) Cause:
• Patologie del SNC • Patologie neuromuscolari • Disfunzione dei muscoli respiratori
26
CIANOSI
La cianosi è uno dei segni più frequenti dell’ipossia(ma potrebbe non comparire in caso di ipossia es. in pazienti anemici) e compare quando i valori dell’Hb ridotta (non ossigenata) sono uguali o superiori a 5g/dl. Il colorito cianotico, ovvero il colorito bluastro della cute e delle mucose(come letto ungueale, labbra,), si ha quindi in tutti i casi in cui è aumentato a livello dei capillari il contenuto di emoglobina ridotta o per difetto di ossigenazione del sangue o per mescolamento del sangue venoso con l’arterioso La cianosi si distingue in : CENTRALE: (dovuta ad una riduzione di sangue ossigenato perché il legame all’O2 a livello alveolare è stato inefficiente. Quindi si ha una ridotta saturazione dell’Hb) Le cause sono:
1. Ridotta saturazione di ossigeno (situazione di ipossiemia) cioè il sangue a livello delle vene polmonari che arriva al ventricolo è poco ossigeno.
2. Ridotta pressione atmosferica (dovuta per es. all’ altitudine) 3. Alterata funzione polmonare
• Ipoventilazione alveolare • Alterazione del rapporto ventilazione/per fusione • Alterata diffusione dell’ossigeno
2. Shunts anatomici (es dx-sx)
• Alcune cardiopatie congenite • Fistole artero-venose polmonari • Piccoli shunts intrapolmonari
3. Anolamlie dell’emoglobina
• Meteglobinemia (ereditaria, acquisita) • Sulfemoglobinemia (acquisita) • Carbossiemoglobinemia (non vera cianosi): intossicazione da CO (ossido di carbonio):
l’emoglobina satura di CO invece che di O2 e non c’è cianosi bluastra come per l’ossigeno.
PERIFERICA: situazione nella quale i/il tessuti dove arriva il sangue ossigenato necessitano di una quantità maggiore di O2 (forma eccessiva di ossigeno) e quindi si avrà un eccessivo rilascio di O2 rispetto a una situazione normale. Le cause sono:
• Insufficienza cardiaca: il cuore nell’insufficienza cardiaca invia meno sangue e quindi emoglobina(Hb) in periferia. I tessuti aumenteranno perciò l’estrazione di ossigeno dall’Hb che arriva ai tessuti causando cianosi a livello dei tessuti. (periferia)
• Esposizione al freddo: avremo in tal caso una vaso costrizione e il flusso sanguigno sarà rallentato e meno carico di O2.
• Redistribuzione del flusso ematico: il sangue si ridistribuisce in alcune zone rispetto ad altre
27
Tutte queste sono forme di Cianosi simmetrica mentre nel caso di ostruzioni arteriose o venose abbiamo una Cianosi distrettuale:
• Ostruzione arteriosa: (es: embolo a un’arteria femorale che blocca al sangue destinato ai distretti a valle) arriverà meno sangue e avremo una maggiore estrazione di O2 negli altri distretti e una cianosi bluastra, periferica e distrettuale .
• Ostruzione venosa
28
IPOSSIA
Si definisce ipossia una inadeguata disponibilità d’ossigeno per le funzioni metaboliche dei tessuti. Quindi si avrà una riduzione della pressione parziale di ossigeno nel sangue arterioso. L’ipossia ha come stimolo riflesso la costrizione dei vasi arteriosi bronchiali, ogni volta che vi è l’ipossia, un meccanismo è quello di cercare di aumentare la pressione a carico delle arterie polmonari per aumentare la superficie di scambio. La conseguenza dell’ipossia per valori della PaO2 compresi tra 40-60 mmHg è la dispnea, per valori tra 25-40 mmHg si ha una sintomatologia simile all’intossicazione da alcool(es. incordinazione motoria, riflessi rallentati,stato di incoscienza), per valori minori di 20 mmHg si può arrivare al coma e addirittura alla morte Le forme più frequenti sono:
1. Ipossia anemica: l’emoglobina è normalmente saturata quando entra nel circolo sistemico però c’è poca emoglobina
2. Da carbossiemoglobina l’emoglobina legata all’ossido di carbonio nel quale c’è un alterato rilascio di O2 nei tessuti.
3. Respiratoria: sono tutte quelle forme polmonari che attraverso diversi sistemi di alterazioni possono causare ipossiemia.
4. Da elevata altitudine: può essere associata a cianosi 5. Da shunt destro-sinistro: può essere intrapolmonare o extrapolmonare (cardiaco) 6. Circolatoria: nella Cianosi periferica 7. Distrettuale: interessa un solo organo o tessuto. 8. Da aumentata richiesta di O2: in caso di sforzo, quando le necessità dei tessuti non
possono essere soddisfatte si può avere ipossia. 9. Ipossia istotossica o da tossicità dei tessuti: avvelenamento da cianuro, il tessuto
anche se l’O2 c’è non riesce ad utilizzarlo Nel grafico successivo è mostrata la Curva saturazione Emoglobina: in Ascissa c’è la Pressione parziale di O2,(le linee sono tratteggiate perché la curva può essere spostata più verso destra o verso sinistra a seconda di alcune condizioni del tessuto)in ordinata la %di saturazione dell’Hb. In condizioni di acidosi e quindi quando il tessuto lavora in condizioni di ipossia l’estrazione di O2 dall’emoglobina a livello dei tessuti è più elevata. Questo vuol dire che a parità di tensione di O2 a livello del tessuto, se è presente acidosi, la quantità di O2
rilasciata è maggiore. Significa che se siamo in presenza di Ipercapnia (aumento della Pressione parziale di Co2) aumenta l’estrazione dell’O2 dal sangue e questo spiega perché le condizioni associate a ipercapnia danno anche cianosi.
29
ASMA BRONCHIALE
Malattia infiammatoria delle vie aeree caratterizzata da aumentata responsività dell’albero tracheobronchiale a svariati stimoli, che conduce alla riduzione del calibro delle vie aeree a all’ostruzione al passaggio dell’aria. Epidemiologia Malattia molto frequente, che colpisce il 4-7% della popolazione generale. Incremento della mortalità per asma negli ultimi decenni. Classificazione 1. Asma allergico (estrinseco): compare in età giovanile ed è Associato a storia personale e/o familiare di malattie allergiche quali: rinite orticaria eczema L’asma allergico può essere di tipo stagionale, legato a periodi pollinazione delle piante, o di tipo non stagionale o perenne, dovuto ad allergeni costantemente presenti nell’ambiente; quali: Pollini Acari della polvere Forfore di animali Spore fungine L’esposizione agli allergeni provoca una risposta broncocostrittiva nel giro di pochi minuti. 2. Asma intrinseco Si manifesta in soggetti che non presentano caratteristiche di tipo allergico, tende a comparire più tardivamente nel corso della vita, e generalmente si manifesta per la prima volta dopo infezioni virali delle vie respiratorie. 3. Asma professionale Esposizione a sostanze in ambito lavorativo.
31
Patogenesi INFIAMMAZIONE + IPER-REATTIVITA’ BRONCHIALE sono le principali alterazioni fisiopatologiche dell’asma. Oggi si tende ad attribuire un ruolo cruciale nella patogenesi dell’asma alla presenza di un persistente stato infiammatorio delle vie aeree. All’esame istologico la mucosa risulta edematosa e infiltrata da eosinofili, mastociti, macrofagi, neutrofili e linfociti T attivati. Le citochine e i fattori di crescita rilasciati dalle cellule suddette, ma anche della cellule normalmente residenti nelle vie aeree, sono responsabili dell’attivazione e del mantenimento della risposta infiammatoria. Conseguenza all’attivazione dei processi infiammatori è la concetrazione della muscolatura liscia bronchiale, dovuta sia ad alcuni mediatori liberati dalle cellule infiammatorie (istamina, prostaglandine e leucotrieni), sia all’acetilcolina rilasciata dalle fibre afferenti vagali. Lo spasmo della muscolatura bronchiale è la causa principale dell’ostruzione delle vie aeree che, però, è anche diretta conseguenza di altri effetti dell’infiammazione, quali edema della parte, l’aumento della produzione di muco e il danneggiamento dell’epitelio con alterazione del trasporto mucociliare. Cause principali dell’asma:
• Broncocostrizione • Infiammazione • Edema
32
Fisiopatologia
1. Variabile e (generalmente) reversibile ostruzione al flusso aereo → riduzione della VEMS (FEV1)
2. Iperinsufflazione polmonare → aumento della capacità vitale forzata e riduzione del rapporto VEMS/CVF
3. Alterazioni dei gas ematici 4. Iperresponsività bronchiale → modificazioni della VEMS>20% in risposta a vari stimoli
(metacolina, istamina, salina ipertonica, allergeni). Quantificabile in base alla dose necessaria.
Spirometria( confronto tra soggetto normale e soggetto con asma) Nel grafico vediamo in ascissa il tempo in sec, in ordinata il Volume. Nel soggetto che respira normalmente, il volume aumenta e diminuisce in base alla respirazione. Successivamente poi il soggetto viene invitato ad un’inspirazione massimale e con successiva espirazione massimale qundi il volume diminuisce e al 1° sec il volume è uguale a 0,8 L. Nel soggetto con asma si vede che al 1° sec il suo volume è di 1,5 L (VEMS ridotta),e al termine dell’espirazione il volume che rimane all’interno del polmone è più elevato rispetto a quello che rimane in un soggetto sano e quindi si ha il segno dell’iperinsufflazione ovvero il soggetto non riesce a svuotare completamente il polmone. Siccome quest’ultimo parametro(Volume residuo che resta nei polmoni dopo l’espirazione forzata) aumenta in condizioni di asma e il VEMS diminuisce, il rapporto tra questi due parametri è un indice molto importante perché ci consente di distinguere le forme ostruttive da quelle restrittive. Messaggio da portare a casa: la spirometria è importante, i parametri importanti sono il volume espiratorio massimo al 1° sec(VEMS), che correla anche con la gravità della patologia e, il volume residuo al termine dell’espirazione forzata che indice di iperinsufflazione.
33
Forme particolari di asma:
• Asma notturno
• Asma da esercizio fisico
• Asma da reflusso G-E
• Asma da aspirina, il 5-10 % di pazienti asmatici presentano riacutizzazioni in seguito all’assunzione di aspirina, probabilmente a causa dell’inibizione della ciclossigenasi da parte di questi farmaci e della conseguente ridotta produzione di prostglandine ed eccessiva produzione di leucotrieni.
Presentazione clinica La caratteristica sintomatologia dell’asma, che si presenta in modo ascensionale a crisi, è costituita da: - Dispnea - Tosse - Oppressione toracica - Respiro sibilante E.O.: Sibili, fischi, segni di iperinsufflazione Cause Esposizione ad agenti o fattori scatenanti (sensibilizzazione →sintomi):
Esposizioni ad allergeni Infezioni virali delle vie respiratorie Esercizio fisico Assunzione di farmaci (soprattutto acido acetilsalicilico o altri FANS) Esposizione ad irritanti o inquinanti ambientali Assunzione di particolari cibi Stress psichico o emotivo Fattori climatici (aria fredda, nebbia) Reflusso gastroesofageo
Segni di allarme:
• Cianosi • Uso di muscoli respiratori accessori • Tachicardia
34
Diagnosi
• Clinica • Spirometria, durante la crisi asmatica, l’ostruzione delle vie aeree provoca l’aumento
delle resistenze al passaggio dell’aria e tutti gli indici di flusso espiratorio sono marcamenti ridotti. Risulta ridotto il volume espiratorio forzato al primo secondo FEV1.
• Tests provocativi specifici (allergeni) • Tests allergologici cutanei
Terapia - β2-agonisti: hanno azione broncodilatatrice - corticosteroidi - anticolinergici - teofillinici - antagonisti dei leucotrieni - stabilizzatori dei mastociti
35
INFLUENZA
L’influenza è un’infezione virale acuta che interessa prevalentemente le alte vie respiratorie, causata da infezione con virus influenzali. E’ a evoluzione generalmente benigna, ma può anche essere letale in pazienti ad alto rischio (cardiopatici, pneumopatici, anziani e soggetti debilitati). I virus dell’influenza sono virus a RNA, sono classificati in tre tipi: A, B e C in base alla caratteristiche di alcuni antigeni interni. Sulla superficie virale ci sono due tipi di estroflessioni proteiche, l’emoagglutinina , o antigene H, e la neuraminidasi , o antigene N. Epidemiologia Per il virus di tipo A esistono due grandi differenti variazioni. Le variazioni maggiori sono dette shift (varianti antigeniche), possono riguardare solo l’emoagglutinina, o l’emoagglutinina e la neuraminidasi insieme,e portano alla comparsa di nuovi sottotipi virali. Nelle infezioni umane sono state individuate tre varianti dell’emoagglutinina (H1, H2 e H3) e due della neuraminidasi (N1 e N2). Quando compare un nuovo sottotipo virale, evento che si verifica ogni 15 anni, la popolazione non è protetta dell’immunizzazione sviluppata dal contatto con i precedenti virus influenzali, e la malattia colpisce la gran porte della popolazione con diffusione mondiale (pandemia). 1918-19: H1N1 Pandemia “spagnola” 1957-58 H2N2 Pandemia “asiatica” 1968-69 H3N2 1997: è stato isolato un virus H5N1, affine al virus influenzale dei polli e ciò è stato spiegato con l’ipotesi di riarragiamenti genetici tra virus influenzali umani e animali. Le variazioni minori sono dette drift (modificazioni antigeniche), riguardano solo l’antigene H e danno origine a nuovi ceppi nell’ambito del medesimo sottotipo, provocando epidemie limitate dato che tra la popolazione esiste una parziale immunità. Epidemie influenzali durante i mesi invernali Patogenesi L’infezione avviene a livello della mucosa delle prime vie aeree, tramite le secrezioni di un soggetto con infezione acuta, probabilmente per mezzo di goccioline di saliva in forma di aerosol generate dalla tosse o dagli starnuti, ma anche attraverso le mani o il contatto diretto. Il virus penetra nelle cellule dell’ epitelio respiratorio e si replica al loro interno. L’eliminazione del virus con le secrezioni respiratorie cessa, in genere, 2-5 giorni dopo l’inizio dei sintomi. Nella guarigione un importante ruolo è svolto dalla produzione di interferone e dalla risposta cellula-mediata.
36
Manifestazioni cliniche L’esordio, dopo 1-3 giorni di incubazione, è generalmente brusco con la comparsa di:
• Cefalea • Febbre, di tipo continuo-remittente, è generalmente elevata (da 38° fino a 41°) fin dal
primo giorno, poi tende a calare progressivamente nel giro di 2-4 giorni. • Malessere generale, a volte l’esordio conclamato della malattia è preceduto da 24-48
ore di malessere generale. Il quadro clinico può, comunque, essere molto vario e l’influenza può anche manifestarsi con i sintomi del raffreddore senza febbre o con un profondo senso di prostrazione senza sintomi respiratori
• Mialgie (dolore muscolare) • Tosse, inizialmente secca, in seguito può divenire produttiva. A volte possono essre
presenti nausea, vomito, dolori addominali e diarrea. • Rinorrea • Faringodinia • Dolore retrobulbare, fotofobia
- Obiettività scarsa (linfoadenopatie, rumori toracici) - Risoluzione dopo 5-7 giorni, segue un periodo di convalescenza con astenia e, a volte, persistenza della tosse anche per 1-2 settimane. - Sindrome “post-influenzale” Complicanze
• Polmonite (primaria, secondaria, mista)e Broncopolmonite: La POLMONITE può esistere quella da virus influenzale ovvero un infezione che invece di fermarsi nelle prime vie aeree, continua fino alle vie aeree più profonde; questa è definita come POLMONITE PRIMARIA quindi causata del virus dell’influenza. Ci può anche essere una POLMONITE SECONDARIA causata dall’arrivo di germi che non sono correlati all’influenza, ma che siccome c’è un danno a carico delle vie respiratorie trovano un terreno più favorevole per lo sviluppo di broncopolmonite da pneumococco o altri germi.
• Miosite: infiammazione dei muscoli scheletrici che possono dar luogo ad una RABDOMIOLISI (rottura dei muscoli scheletrici). Questo può essere pericoloso perché può dare un’insufficienza renale acuta(perché la mioglobina e altri enzimi che si liberano dalla lesione dei muscoli possono danneggiare il rene ).
• Peggioramento di malattie sistemiche pre-esistenti (Legate allo stesso virus
influenzale o al fatto che l’influenza apre la strada a complicanze infettive di altro genere e che spesso è causa di morte ): avere un soggetto con insufficienza cardiaca oppure un soggetto che soffre di BPCO (bronchite cronica), in cui si ha una situazione cardiologia o respiratoria già compromessa è chiaro che la patologia infettiva come l’influenza aumenterà la richiesta di lavoro cardiaco per la febbre, per l’aumentata richiesta metabolica da parte dei tessuti.
37
Diagnosi • Clinica, il virus può essere isolato tramite tampone faringeo • Sierologica, serve solo da conferma
Terapia
• Di supporto (antipiretici e idratazione il più delle volte) • Gli Antivirali (poco usata nella pratica clinica, infatti si utilizza nelle pandemie)
• Antibatterici per complicanze: sono i così detti antibiotici. Sono sostanze di derivazione
naturale da funghi ect, che hanno un’attività antimicrobica, per cui gli antibatterici andrebbero chiamati chemioterapici. Gli antibatterici non servono nell’ influenza perché non è una malattia causata da batteri, ma da virus. Però si utilizzano in particolari situazioni dove per es. c’è una polmonite (pazienti più a rischio), e quindi si sospetta una sovrapposizione batterica. Ecco perché il soggetto con l’influenza potrà avere anche una terapia con gli antibatterici. Gli antibiotici si danno quando: C’è una complicanza ad esempio: quando il soggetto respira male, diventa cianotico, facendo una radiografia vediamo un inizio di broncopolmonite,ecc Quando la complicanza è probabile o particolarmente Temibile: es. soggetto anziano con insufficienza cardiaca che prende l’influenza- si scompenserà – avrà un edema polmonare e quindi non si può rischiare anche di avere una sovrammissione batterica (quindi se già ci sono li elimino , se non ci sono prevengo la sovrammissione)
• Prevenzione (vaccino antinfluenzali)
38
BRONCOPOLMONITE E POLMONITE
La polmonite è infiammazione del parenchima polmonare, che interessa gli alveoli, le vie aeree distali e l’interstizio, causata da infezione da batteri o altri micro-organismi. La Differenza fra BRONCOPOLMONITE E POLMONITE ( differenza a livello di anatomia patologia):
• POLMONITE colpisce alveoli e polmoni • BRONCOPOLMONITE colpisce anche i bronchi più distali
N.B. per le informazioni riportate di seguito non ci sono differenze tra Broncopolmoniti e Polmoniti . Broncopolmonite e polmonite possono essere classificate in molti modi,ma questo non significa che si parla di broncopolmoniti e polmoniti diverse, ma solamente cambiare il criterio di classificazione per uno stesso gruppo di patologie. I vari tipi di classificazione sono:
1. “CLASSIFICAZIONE “EZIOLOGICA” a seconda del microrganismo che causa la polmonite detti agenti eziologici: virus, batteri, funghi, protozoi. Nell’ambito dei batteri potrebbe esserci una seconda classificazione: GRAM POSITIVI O GRAM NEGATIVI,AEROBE E ANAEROBI().
2. CLASSIFICAZIONE “EPIDEMILOGICA CLINICA” ovvero dove il paziente ha contratto la patologia:Acquisita in comunità,in ospedale,associata ad immunodepressione come quella da HIV+ (essere sieropositivi per HIV non significa avere l’AIDS).
Queste due classificazioni possono essere miscelate tra loro, (e non si escludono tra loro) permettendoci di ipotizzare i germi che hanno causato la patologia scegliendo una terapia più adeguata e specifica per quel tipo di germe. Broncopolmonite Acquisita in comunità (ovvero nella collettività e spesso causata da germi)
Broncopolmonite Acquisita in ospedale
Broncopolmonite associata a immunodepressione (es. HIV(agente eziologico dell’AIDS))
Mycoplasma pneumoniae Streptococcus pneumonite (o pneumococco,G+) Haemophilus influenzae(bacillo,G-) Chlamydia pneumoniae Legionella pneumophila Oral anaerobes(anche in comunità) Moraxella catarrhalis Staphylococcus aureus Nocardia spp. Virusesa Fungib Mycobacterium tuberculosis Chlamydia psittaci
Enteric aerobic gram-negative bacilli Pseudomonas aeruginosa (tipico delle infez.ospedaliere, provoca colorito verdastro all’escreato) S. aureus (raro in comunità) Oral anaerobes
Pneumocystis carinii M. tuberculosis S. pneumoniae H. influenzae Micobatteri atipici Fungib
39
a Virus Influenzali , cytomegalovirus ,virus respiratorio sinciziale (entrambi colpiscono soprattutto gli immunodepressi),virus del morbillo,della varicella-zoster, l’antavirus.bHistoplasmosi, Coccidoidosi, e Blastomicosi spp.
Conoscere l’agente mi permette la terapia antibiotica adeguata per l’agente (più specifica); se faccio terapia antibiotica non adeguata rischio di produrre RESISTENZE ANTIBIOTICHE. Meccanismi di trasmissione - L’aspirazione di micro-organismi che colonizzano l’orofaringe è di gran lunga la causa più frequente di polmonite. Il naso-faringe, infatti, può essere colonizzato da batteri potenzialmente patogeni: Streptococchi Pneumococchi Micoplasma Haemophilus influenzae - Inalazione di particelle di aerosol infetti in sospensione nell’ambiente TBC Influenza Legionellosi - Le infezioni polmonari per via per via ematica sono meno frequenti e spesso dovute a: Stafilococchi - Per trasmissione diretta (contiguità) da focolai infettivi adiacenti Ritornando alla Classificazione Le polmoniti possono essere classificate su base eziologia (batteriche, virali, da protozoi e da miceti), su base anatomo-patologica ed epidemiologica. Classificazione anatomo-patologica: Si possono distinguere tre forme: alveolari, interstiziali e necrotizzanti.
1. Le polmoniti alveolari sono caratterizzate dal prevalente interessamento degli alveoli da parte del processo infiammatorio, con presenza al loro interno di abbondante essudato; possono interessare una regione di un lobo o un intero lobo (polmonite a focolaio), oppure multiple regioni situate in diversi lobi polmonari, con coinvolgimento della parete bronchiale e del parenchima adiacente (broncopolmonite).
2. Le polmoniti interstiziali interessano prevalentemente l’interstizio polmonare in maniera diffusa. E’ minore l’essudato all’interno degli alveoli, e viene alterata la normale elasticità del polmone.
3. Le polmoniti necrotizzanti sono caratterizzate da un’evoluzione verso la necrosi del parenchima polmonare interessato, spesso con la successiva formazione di ascessi.
40
Classificazione epidemiologica: Le polmoniti possono essere divise in due grandi classi: polmoniti acquisite in comunità e polmoniti acquisite in ospedale o nosocomiali:
1. Le polmoniti acquisite in comunità sono contratte fuori dall’ambiente ospedaliero, tramite: Viaggi, Contatti con malati, Contatti con animali o Epidemie.
2. Le polmoniti nosocomiali interessano generalmente soggetti affetti da patologie sistemiche e con un certo grado di compromissione delle difese immunitarie.
Rapporti con l’età e condizioni morbose
• Haemophilus → bambini • Clamidia, Pneumococco →giovani • Legionella, Haemophilus → anziani • Anaerobi → ab ingestis • Neutropenia → Pseudomonas • HIV → Micobatteri, Pneumocystis
Manifestazioni cliniche Le polmoniti vengono distinte in:
1. Polmonite “tipica” Insorgono con: • Febbre • Sintomi respiratori • Tosse produttiva • Espettorato purulento • Dispnea • Dolore toracico da infiammazione pleurica L’esame fisico evidenzia aree di ottusità e rantoli respiratori, la radiografia del torace mostra focolai singoli o multipli. Queste tipi di polmonite sono causate da: Streptococchi, pneumococchi, Haemophilus influenzae
2. Polmonite “atipica”
Insorgono con: • Dispena • Tosse secca • Sintomi extrapolmonari (cefalea, astenia, mialgie, nausea, vomito e diarrea) Le polmoniti atipiche sono più insidiose rispetto a quelle tipiche è sono causate da: Micoplasmi, Legionella, Clamidia, Virus
3. Polmonite nosocomiale
• Spesso afebbrile • Difficile da diagnosticare
41
4. Polmonite ab ingestis Sono causate dall’aspirazione di materiale gastrico e sono frequenti nei soggetti con alterazione del sensorio (uso di droghe o alcol, anestesia generale, malattie del sistema nervoso centrale), con disturbi della deglutizione o sottoposti a intubazione nasogastrica o endotracheale. Queste polmoniti sono quasi sempre causate da batteri anaerobi e possono andare in contro alla formazione di ascessi polmonari. Gli ascessi polmonari sono processi infiammatori suppurativi del parenchima polmonare, che spesso evolvono verso la formazione di vacità neoformate. L’esordio clinico può essere insidioso o acuto, con febbre elevata, tosse produttiva, anoressia e prostazione. Un escreato dall’ odore putrido è caratteristico delle infezioni da aneerobi.
42
Diagnosi
Radiografia: resta sempre uno degli elementi di massima importanza es.una radiografia di un emitorace mostra l'ombra cardiaca e del diaframma. Inoltre si può notare un opacamento dell'emitorace dovuto ad un addensamento che rappresenta la broncopolmonite.
TAC ha sensibilità maggiore: è possibile vedere non solo gli addensamenti, ma anche delle escavazioni
43
Inoltre si può fare anche una diagnosi eziologica mediante: Esame dell’escreato (con metodiche immunonologiche) Tecniche invasive di prelievo :es. toracentesi , lavaggio bronco-alveolare, broncoscopia, biopsia tecniche dirette in cui si effettua l'isolamento diretto del germe che consente di stabilire con precisione la sensibilità agli anti batterici. Sierologia es. emocultura (esame colturale del sangue per individuare l’agente eziologico della broncopolmonite;inoltre questo esame ci consente anche di fare l’antibiogramma mediante il quale si riesce a ricavare l’antibiotico o chemioterapico antimicrobico più efficace per quel germe)
44
TUBERCOLOSI
La Tubercolosi è una malattia contagiosa causata da Mycobacterium tuberculosis complex (definito anche bacillo di Koch, o BK, dal nome dello scopritore). La malattia colpisce generalmente i polmoni, ma in un terzo dei casi interessa altri organi, in particolare, linfonodi, pleura, reni, ossa e meningi. Il “Mycobacterium tubecolosis complex” comprende una serie di germi, come: M. tuberculosis (il quale nella maggior parte dei casi è responsabile dell'infezione) M. bovis (un tempo responsabile di casi di tubercolosi trasmessa dal latte non pastorizzato) M. africanum
45
Epidemiologia
La tubercolosi rappresenta in tutto il mondo un grave problema sanitario, con 8.500.000 di nuovi casi nel 2001 (95% dai Paesi in via di sviluppo). L’incidenza globale è in continuo aumento, non solo nelle aree povere del mondo, ma anche in molti paesi industrializzati, tra cui l’Italia. La recrudescenza della tubercolosi nei paesi occidentali è riconducibile a più fattori, tra i quali l’aumento dell’immigrazione da paesi a elevata endemia, la diffusione dell’infezione da HIV, la scarsa attività di sorveglianza e prevenzione, la comparsa di ceppi batterici multifarmacoresistenti. Dall’esposizione all’infezione L'esposizione avviene quando in un soggetto che ha la tubercolosi, si ha il passaggio del germe nelle prime vie aeree. Quindi tamite manifestazioni di tosse, saliva o anche semplicemente parlando, emette delle micro gocciole, dette “nuclei infettanti” che poi restano sospese nell'aria, con il loro carico di mycobatteri e vengono inalati da un altro soggetto che quindi resta infettato. A questo punto il germe arriva agli alveoli, dove viene inglobato dai macrofagi (fanno parte delle cellule dell'immunità innata).Se i macrofagi catturano questi mycobatteri e li uccidono non si ha l'infezione. Al contrario se i mycobatteri si replicano, cominciando a distruggere i macrofagi,e causano l'infezione primaria. I fattori che condizionano la trasmissione in questo caso: Fattori esogeni
• Contatto con pazienti • Durata del contatto • Ambiente poco ventilato e affollato • Infettività del bacillo
46
Dall’infezione alla malattia Per malattia si intende la comparsa di manifestazioni cliniche. I fattori che condizionano la trasmissione in questo caso sono: Fattori endogeni
• Picco in età giovanile (F>M) • Anche età avanzata (M>F)
Fattori di rischio: (fattori che aumentano la probabilità di contrarre la malattia)per TB attiva in persone infettate con BK (vecchia infezione=1) Es. un Rischio relativo di 2 in un soggetto indica che questo ha una probabilità di sviluppare la malattia 2 volte superiore rispetto ad un soggetto che non presenta quel fattore di rischio Fattori di rischio RR rischio relativo Infezioni recenti < 1 12.9 Lesioni fibrotiche 2–20 Infezioni da HIV 100 Silicosi 30 Insufficienza renale 10–25 Diabete mellito 2–4 Uso di droghe 10–30 Terapia immunosopressiva 10 Gastrectomia 2–5 Periodo di post trapianto di cuore e rene 20–70 Malnutrizione e sovrappeso 2 Jejunoileal bypass 30–60
Nelle condizioni in cui per una serie di ragioni si ha un abbassamento delle difese immunitarie, è più facile che si abbia una tubercolosi attiva, e quindi diventa importante tenere sotto controllo l'infezione e renderla inattiva.
47
Patogenesi La via di trasmissione più comune del M. tuberculosis è quella aerea, tramite inalazione di goccioline contenenti micro-organismi → macrofagi infetti, espulse con la tosse, gli starnuti, la parola e in grado di rimanere in sospensione nell’aria anche per molte ore. Fattori che condizionano la progressione dell’infezione:
Attività battericida dei macrofagi Virulenza del batterio Fattori genetici (es. razza)
Se l’infezione progredisce:
1. Moltiplicazione dei bacilli all’interno dei macrofagi alveolari → Infezione 2. Sensibilizzazione dei linfociti T CD4+ (immunità specifica 2-4 settimane) →
proliferazione e produzione di citochine attivanti i macrofagi → focolaio infiammatorio con formazione di granuli (tubercoli) costituito da cellule giganti multinucleate, di derivazione macrofagica, da linfociti e da necrosi caseosa centrale.
L'infezione può o non può progredire; se essa progredisce i macrofagi vengono distrutti e questo si verifica in caso di infezione primaria; successivamente vengono richiamate altre cellule, altri macrofagi, monociti dal sangue(da fattori chemiotattici) e viene attivata l'immunità specifica ovvero i linfociti.Tutto ciò determina la formazione di granulomi. Da un punto di vista della patologia generale, il granuloma è un agglomerato di cellule(macrofagi, cellule epiteliomi e cellule giganti multinucleate) che si dispongono a formare delle strutture circolari e, nel caso della tubercolosi hanno un diametro di 1-2 mm, (visibili anche ad occhio nudo) e vengono definiti tubercoli. L'evolversi o meno della tubercolosi è dovuto all'efficacia della prima risposta contro il micobatterio, e al tipo di risposta immunitaria: quando i linfociti migrano nella sede dell’infezione, stimolati da una serie di citochine(fattori chemiotattici),questi attivano i macrofagi. Quindi si possono avere sostanzialmente due tipi di risposta immunitaria, che sono diversamente efficaci nel distruggere o nell'inibire la crescita del micobatterio: Tipi di risposta immunitaria antimicobatterica:
o Risposta tipo ipersensibilità ritardata (DTH) → danno del tessuto. La risposta da ipersensibilità ritardata è una risposta in qualche modo sempre efficace, ma che prevede un certo grado di necrosi
o Risposta di attivazione macrofagica è una risposta migliore, determinando con l'attivazione dei macrofagi in maniera ottimale, un inibizione della crescita del micobatterio.
48
La Necrosi caseosa al centro del granuloma è un apetto caratteristico della lesione tubercolare. Nel granuloma ci sono infiltrati macrofagi, pochi linfociti, cellule endoteloidi, e c'è necrosi, che vista microscopicamente sembra avere l'aspetto del formaggio (ricotta). La formazione della necrosi caseosa e la formazione del granuloma, determinano la neutralizzazione dei bacilli, soprattutto se la risposta è di attivazione macrofagica, quindi più efficace. All'interno di questa lesione primaria (granuloma)e dei linfonodi il bacillo resta in sede, vivo ma inattivo; questa è una situazione che può durare anche per tutta al vita.
la risposta immunitaria non è efficace quando c’è: Solo risposta DTH che determina un ulteriore danno.Il danno più importante è la colliquazione a livello polmonare (il polmone diventa liquido) che determina escavazione(un buco).In questo caso si parla di TB aperta infettiva per il fatto che il tessuto collimato viene drenato nei bronchi e con la tosse espulso (questo è uno dei meccanismi grazie al quale avviene la trasmissione)
Nelle fasi iniziali dell’infezione c’è disseminazione ematogena
Guarigione (riattivazione) Tubercolosi miliare
Es.Se un polmone, va incontro a colliquazione ( diventa liquido), si ha in un certo qual modo la distruzione del tessuto: è una vera e propria manifestazione nelle fasi iniziali dell'infezione, che va a raggiungere gli alveoli dove ci sono i macrofagi , i quali portano il germe ai linfonodi dell'ilo polmonare e ai linfonodi del mediastino. Si verifica dunque una disseminazione ematogena, attraverso cui i micobatteri vanno in tutto l'organismo; ai vari livelli l'infezione diventa però inizialmente inattiva. La successiva riattivazione della tubercolosi può avvenire non solo a livello polmonare, ma anche a livello di altri distretti. Un'altra cosa importante è che, già nella fase iniziale dell'infezione, quella chiamata “tubercolosi primaria”, c'è la disseminazione ematogena, che può dar luogo a dei quadri clinici particolari come la tubercolosi miliare e la meningite tubercolare, la quale si può verificare sia in ambito della tubercolosi primaria, sia in ambito della tubercolosi post-primaria
49
Mnifestazioni cliniche
• Tubercolosi Polmonare > 80% dei casi non-HIV Circa il 90% dei soggetti che si infetta con il bacillo tubercolare non va in contro a malattia. Le lesioni polmonari e linfonodiali, rappresentate da un focolaio, rimaste asintomatiche, esitano in fibrosi e calcificazione e possono essere un reperto radiologico accidentale nel corso della vita. Tuttavia, in queste lesioni i micobatteri possono rimanere in uno stato di latenza e riattivarsi a distanza di anni o decenni. Solo il 10% delle persone infettate si ammala. Circa la metà di queste manifesta la malattia nel periodo immediatamente successivo al contagio (soprattutto i bambini al di sotto dei 4 anni) o entro i primi 12-24 mesi (tubercolosi primaria). Nella restante metà dei casi, la malattia si sviluppa a distanza di molto tempo (tubercolosi post-primaria) per riattivazione di un’infezione latente.
1. Primaria Deriva dall’infezione iniziale con il BK Spesso asintomatica Guarisce spontaneamente nella maggior parte dei casi → calcificazione parenchimale e linfonodale Si verifica soprattutto nei bambini o in presenza di alterazioni immunitarie (malnutrizione, HIV), quadro clinico:
o Pleurite o Escavazione primaria o Linfoadenopatie ilo-mediastiniche o TB miliare o Meningite TB
2. Post-primaria
Anche detta “dell’adulto”, “riattivazione TB” o “secondaria” Data da riattivazione di BK, spesso nei lobi superiori
o Infiltrato ha una spiccata tendenza alla col liquazione, cui consegue diffusione dei bacilli e formazione di lesioni satelliti più o meno numerose e confluenti fino al coinvolgimento di uno o più lobi.
o Escavazione → decorso rapido pota a morte → oppure “consunzione” -progressivo scadimento delle condizioni generali Clinicamente il soggetto presenta: Sintomi iniziali non specifici (febbre, sudorazione, anoressia, malessere, astenia(mancanza di forza)) Successivamente il quadro diventa più specifico con : Tosse inizialmente secca ma che diventa poi produttiva e striata di sangue. Inoltre può comparire:Febbre,Anemia,Ippocratismo digitale (un'alterazione della parete distale delle
50
dita, caratterizzata da"dita a bacchetta di tamburo", quindi con la parte distale ingrandita e l'unghia che diventa da poco convessa a molto convessa e che viene definita "unghia a vetrino d'orologio". Non è un segno specifico della tubercolosi, ma rappresenta un segno che richiama patologie respiratorie, cardiorespiratorie croniche, per esempio casi di BPCO).
• Tubercolosi extrapolmonare In ordine di frequenza:
1. TB Linfonodale Ingrandimento non dolente dei Linfonodi laterocervicali e/o sopraclavicolari (scrofola), con tendenza alla formazione di fistole cutanee.
2. TB pleurica Più comunemente è causata dalla penetrazione di pochi bacilli nello spazio pleurico con conseguente coinvolgimento della sierosa e formazione di un versamento con le caratteristiche di un essudato, di entità assai variabile, in alcuni casi asintomatico, in altri responsabile di febbre, dolore toracico, dispnea.
3. Alte vie aeree Laringe, faringe, epiglottide
51
4. TB Genito-urinaria
E’ solitamente dovuta a diffusione ematogena secondaria a infezione primaria ed è caratterizzata da gravi lesioni escavate oppure idronefrosi da restringimento degli ureteri. Il malato può lamentare pollachiuria, disuria, dolore al fianco; l’esame delle urine documenta ematuria, piuria e ph acido. La tubercolosi genitale nelle donne coinvolge più frequentemente salpingi ed endometrio e si manifesta con dolore pelvico e sterilità. Nell’uomo possono essere interessati epididimo (epididimite), testicolo e prostata.
5. TB Ossea La manifestazione più frequente è la spondilite (morbo di Pott), caratterizzata da interessamento di due o più vertebre adiacenti e progressiva distruzione dei corpi e dei dischi intervertebrali fino a deformazione della colonna (gibbo), formazione di ascessi a colata paravertebrali e paraplegia per compressione midollare.
6. Meningite tubercolare Può colpire tutte l’età, ma è più frequente nei giovani e nei soggetti con infezione da HIV. La malattia evolve nell’arco di 1-2 settimane, durante le quali compaiano cefale, cambiamento dell’umore e del carattere, confusione mentale, rigidità nucale, segni di interessamento dei nevi cranici (soprattutto degli oculomotori). La puntura lombare (rachicentesi) è fondamentale per la diagnosi: il liquido cefalorachidiano ha in genere aspetto limpido, la concentrazione di proteine nel liquor è elevata, mentre la concentrazione di glucosio è tipicamente molto bassa.
7. TB Gastrointestinale Può essere causata da M. tuberculosis o M. bivis e interessare qualsiasi tratto del tubo digerente, anche se sono più comunemente coinvolti l’ileo terminale e il cieco. La sintomatologia è caratterizzata da dolore addominale, diarrea, dimagrimento, segni di ostruzione, presenza di sangue nelle feci e febbre.
8. Pericardite costrittiva Pericardite (processo infiammatorio acuto o cronico del pericardio) conseguente a ispessimento e fibrosi del pericardio con formazioni cicatriziali, aderenze e calcificazioni. Comporta un ostacolo alla emodinamica del cuore.
9. TB miliare (disseminata) E’ dovuta alla dffusione ematogena dei bacilli tubercolari in corso di infezione primaria o di riattivazione di vecchi focolai, soprattutto nell’infiammazione e nei soggetti immunodepressi. E’ caratterizzata dalla presenza di lesioni di dimensioni paragonabili ai grani di miglio, ciascuna costituita da pochi tubercoli. Maggiormente colpiti sono polmoni, fegato, rene, milza. Febbre, sudorazione, stenia, inappetenza, calo ponderale del peso e epato-splenomegalia sono i sintomi più comuni e dipendono dalla sede prevalente. La diagnosi si ottiene più frequentemente attraverso l’esame colturale di materiale ottenuto da lavaggio broncoalveolare.
52
Diagnosi Rx torace: infiltrati ed escavazione Pazienti immunodepressi (HIV): quadro atipico Individuazione del bacillo tubercolare tramite:
• Es. batterioscopico • Es. colturale che a causa di una crescita molto lenta dei micobatteri, il risultato
dell’esame culturale è disponibile solo dopo 4-8 settimane • Amplificazione genica attraverso la PCR (reazione di biologia molecolare), si va a
cercare il DNA del germe. Valutazione risposta immunitaria
• Intradermoreazione di Mantoux (tubercolina o purified protein derivative, PPD) (Falsi positivi e falsi negativi) consiste nell’iniezione intradermica di soluzione contenente derivato proteico purificato del micobatterio. La lettura va eseguita a distanza di 42-78 ore misurando in mm il diametro dell’infiltrato cutaneo. La positività al test non è indicativa di malattia in atto, ma testimonia l’avvenuta infezione passata o presente.
• Rilascio di citochine (Quantiferon-TB), sono delle proteine della comunicazione
cellulare, si prende il sangue, si mette a contatto con degli antigeni tubercolari e si misura la produzione di interferone gamma (citochina). Se si supera una certa soglia dell’interferone il test è positivo.
Terapia Isoniazide Rifampicina Pirazinamide Etambutolo E’ raccomandato un trattamento iniziale di 8 settimane con isoniazide, rinfamicina, pirazinamide ed etambutonolo, seguito da una fase di continuazione di 18 settimane con isoniazide e rinfamicina, per la durata complessiva di 6 mesi. Prevenzione Vaccinazione con BCG Trattamento di TB latente
53
TROMBOEMBOLIA POLMONARE Definizione di embolo : presenza di materiale insolubile in circolo . Quella più rilevante è l’ embolia di materiale trombotico in quanto ci sono questi coaguli che vanno in circolo , ma non necessariamente l’ embolia del materiale trombotico. Le embolie interessano per definizione interessano i vasi e il circolo. Ci sono due sistemi: 1 – il sistema del circolo polmonare , 2 – il sistema del circolo sistemico ; per cui avremo: l’ embolia polmonare e l’ embolia del circolo sistemico con effetti diversi: L’ embolia del circolo sistemico è quello che si crea a livello sistemico e comprende : il cuore sx , atrio sx , il ventricolo sinistro, l’ aorta e da questa il sangue arterioso va a finire in tutti i distretti: reni , muscoli cervello ecc. Quindi interessa,il cuore stesso, cioè il miocardio attraverso le coronarie e tutti quei distretti che sono irrorati dal sangue arterioso . Quindi un coagulo che si forma nel circolo sistemico, per esempio si forma nel ventricolo sx perché c’è una fibrillazione atriale (condizione che favorisce la formazione di coaguli nel cuore ) si stacca e percorrerà l’ atrio sx , ventricolo sinistro aorta e da li puo’ andare ovunque ma non nel polmone, perché seguendo la diramazione delle arterie arriverà ad un vaso che sarà più piccolo del trombo e si fermerà. Il quadro che darà questa embolia sistemica è una ischemia, ovvero un ridotta o assente per fusione al distretto irrorato da quell’ arteria ; Es. quindi se va ad una arteria che arriva al cervello avremo un ictus ischemico, se va al rene avremo un infarto renale se va ad un arto inferiore avremo l’ ischemia di un arto . Per quanto riguarda l’ embolia polmonare ,l’embolo si forma a livello delle vene , parliamo sempre di circolo sistemico, ma distretto venoso. Il sangue a livello delle vene si riunisce in vene sempre più grosse riunendosi a livello della vena cava e arriva al cuore dx quindi atrio destro, ventricolo dx poi al tronco dell’ arteria polmonare e quindi, l’ eventuale coagulo, andrà a fermarsi nei rami dell’ arteria polmonare . Parlare di trombo embolia polmonare presuppone il riferimento alla patologia venosa e quindi si ricercano le sedi nelle quali che si e’ formato il trombo che poi si stacca e va nel circolo polmonare. Quindi: L’ embolia polmonare è la presenza di un embolo, cioè materiale insolubile di natura trombotica, quindi si parla di tromboembolia polmonare che si va a localizzare in rami dell’ arteria polmonare. L’ origine del trombo è nelle vene perchè sono queste che nel circolo sistemico lo portano al cuore dx .Quelle più spesso interessate sono : le vene delle gambe , come le illache , la vena cava , le vene addominali ad esclusione di quelle che formano la vena porta(confluenza della mesenterica inferiore,mesenterica superiore e vena splenica) che non possono essere sorgente di embolia polmonare in quanto sfociano nel fegato che ha un circolo capillare , dando luogo ad un ‘ altro quadro che è la trombosi portale . In relazione alla tromboembolia polmonare si parla di trombosi venosa profonda dove: trombosi significa formazione di un coagulo in un vaso , venosa significa formazione di un coagulo in un vaso venoso , profonda per differenziarla dalla tromboflebite superficiale; infatti a livello degli arti inferiori c’è un circolo superficiale che si riunisce a livello della grande safena e della piccola safena e un circolo venoso profondo.
54
Le trombofleviti superficiali sono quelle che si manifestano con arrossamento della pelle , e alla palpazione si localizza un cordone trombizzato nella gamba ma non sono fonte di embolia polmonare ,diversamente le TVP si manifestano a livello degli arti inferiori ( sede piu’ frequente ) con edema , dolore e , se la trombosi è particolarmente estesa si può avere anche cianosi (periferica) e pallore dell’ arto in quanto viene compromesso tutto il flusso . Si deve riconoscere la TVP e i suoi fattori di rischio in quanto prevenire e trattare la TVP , significa prevenire anche l’ embolia polmonare che è una patologia spesso fatale. La formazione di questo trombo a livello delle vene parte dalla triade di wirchow, che ha elaborato 3 fattori che predispongono alla formazione del trombo :
• Stasi venosa • Ipercoagulabilità del sangue • Danno vascolare
Dato che la trombo embolia polmonare è una patologia che può essere grave fino alla morte del paziente, è estremamente importante prevenirne lo sviluppo. Prevenire una malattia significa conoscerne LE CONDIZIONI ASSOCIATE (molte delle quali agiscono non attraverso un solo elemento delle triade di Virchow, ma spesso attraverso 2 o 3 elementi della triade stessa) e I FATTORI DI RISCHIO. L’embolia polmonare è importante in assoluto (sempre ed ovunque) ma soprattutto in ambiente ospedaliero, perché è lì che si accumulano molte delle condizioni associate e dei fattori di rischio. Le Condizioni associate e i fattori di rischio:
Chirurgia (soprattutto Chirurgia Maggiore)
Ortopedica, toracica, addominale, e genito-urinaria può rappresentare una di quelle condizioni in cui ritrovo tutti gli elementi della Triade esempio la chirurgia ortopedica in cui abbiamo un soggetto traumatizzato (= fattore di rischio) che dopo l’intervento chirurgico sarà almeno per qualche ora immobilizzato e per qualche giorno ipomobile( =stasi infatti il meccanismo di pompa muscolare che facilita il ritorno venoso viene a mancare). Il soggetto ha subito con l’intervento una LESIONE VASCOLARE IATROGENA (provocata dal chirurgo) a cui l’organismo risponde con una risposta del tutto uguale a quella dell’infiammazione acuta. Per cui avremo una modificazione della coagulazione dovuta all’attivazione delle proteine di fase acuta che determinano un’ipercoaguabilità del sangue.
55
Pancreas, polmone, ovaie, testicoli, tratto urinario(rene +vie uriarie), seno, stomaco: Ci sono neoplasie particolarmente ANGIOINVASIVE ( che tendono ad invadere i vasi) come quella del rene (che può provocare un’embolia polmonare dovuta a materiale neoplastico)O COMPRESSIVE (che comprimono il vaso). In generale, molte di queste neoplasie determinano un’alterazione del profilo coagulativo in modo tale da facilitare la coagulazione del sangue ( come succede ad esempio nelle neoplasie del pancreas). Se poi la neoplasia come spesso avviene compromette la mobilità della persona ( perché magari è disseminata in più zone dell’organismo) si avrà come fattore di rischio aggiuntivo quello della STASI.
Trauma
Fratture del midollo spinale, pelvico, femore, o tibia; , il traumatizzato è spesso immobilizzato, e a fratture possono essere associati danni vascolari ( aumenta la coaguabilità). Ci sono ovviamente traumi di diversa entità, per cui la frattura di un braccio è di gran lunga diversa da una frattura a livello della colonna vertebrale che costringe il paziente a letto, quindi ad una immobilità pressoché assoluta che facilita la formazione di un trombo.
Immobilizazione
infarto del miocardio acuto, insufficienza cardiaca congestizia, ictus, convalescenza post operatoria
La Gravidanza ha una serie di ragioni per cui aumenta il rischio di embolia P. 1. Nella gravidanza avanzata il feto comprime i vasi venosi dell’addome; La gravidanza
inoltre è associata ad altissimi ( ma cmq fisiologici ) livelli di estrogeni e progesterone che favoriscono la coagulazione del sangue in senso procoagulante.
2. Al momento del parto può esserci un passaggio di materiale placentare in circolo, il quale può essere di per se causa di embolia polmonare ( come anche il liquido amniotico ), o avere un’azione come procoagulante.
Estrogeni (per correzione o contraccettivi) è quindi importante nell’anamnesi evidenziare l’impiego di tali sostanze
Stati di ipercoagulabilità (dovuti a CONDIZIONI EREDITARIE (es.deficit Antitrombina III –deficit proteina C o S)o CONDIZIONI ACQUISITE (la sindrome anticorpi antifosfolipidi, la coagulazione intravascolare disseminata o CID)
Resistenza all’attivazione della proteina C; deficienza di antitrombina III, proteina C, o proteina S; antibiotici antifosfolipidi; malattie mieloproliferative; dsfibrinogenemia; coagulazione intravascolare disseminata. Es. Se abbiamo un soggetto con un deficit di proteina C , piuttosto che proteina S, o con una resistenza alla proteina C attivata in maniera congenita , siamo davanti ad una situazione di stato trombofilico (= predisposizione alla trombosi). Inoltre se lo stesso soggetto in età fertile prende la pillola, aumenterà il rischio per questa donna di embolia polmonare.
Quindi c’è bisogno di prestare maggiore attenzione nei reparti per queste condizioni associate e ttori di rischio connessi con l’embolia polmonare,ma ovviamente l’attenzione maggiore è rivolta in particolar modo alle U.O di Medicina, di Chirurgia,in tutti i reparti dove ci sono
56
malati oncologici ( che non sono solo l’oncologia)e in generale nei reparti in cui troviamo tutti quei pazienti colpiti dalle patologie tipiche dell’età avanzata. Tutto quanto detto fino ad adesso significa molto per l’attività dell’ infermiere!Da qui infatti l’importanza della mobilizzazione, l’importanza di una profilassi antitrombotica, l’importanza di riconoscere precocemente un quadro clinico che può essere soggettivo di embolia polmonare. Storia di TVP Fisiopatologia: Un pezzo di coagulo si stacca da una grossa vena arriva al cuore di destra, e quindi passa all’arteria polmonare bloccandone una diramazione .Quindi il polmone a valle del tratto ostruito riceverà meno sangue, ma ci sarà una normale ventilazione..Classico esempio di alterazione del rapporto ventilazione/perfusione in cui ci saranno aree del polmone poco perfuse ma ben ventilate, ed aree e del polmone ben perfuse ( per meglio dire transitate rapidamente dal sangue) e ben ventilate Quindi la Fisiopatologia sarà caratterizzata da:
• Aumento delle resistenze polmonari : il flusso dipende dalle pressione e dalle resistenze; se un tratto dell’arteria polmonare viene ad essere chiuso le resistenze aumentano.
• Alterato scambio gassoso: Il sangue che riesce a fluire negli altri distretti del polmone scambia sì CO2, ma se l’embolia polmonare è sufficientemente severa, non riuscirà a “caricare” O2 in maniera adeguata…….segue che l’alterazione tipica dell’embolia polmonare è data dall’ IPOSSIEMIA con IPOCAPNIA.
• Iperventilazione alveolare: è quella che determina l’ipocapnia( il fatto che venga percepita una riduzione della pressione parziale di O2 determina come risposta riflessa l’iperventilazione che farà eliminare la CO2 in eccesso, ma che può non essere sufficiente a correggere l’ipossiemia)
• Broncocostrizione o ridotta elasticità polmonare: in alcuni casi l’embolia polmonare, cioè l’improvvisa chiusura di un ramo dell’arteria polmonare, può determinare una broncocostrizione riflessa.
• Disfunzione ventricolare destra: il ventricolo dx avrà infatti un sovraccarico di pressione. (il flusso dipende dalle pressione e dalle resistenze); se un tratto dell’arteria polmonare viene ad essere chiuso le resistenze aumentano. Il ventricolo dx dovrà, per mantenere il flusso, aumentare la pressione. Perché ciò avvenga, il ventricolo dovrà lavorare di più. Il cuore ha dei meccanismi di compenso davanti a situazioni inaspettate, tra cui:
1. IPERTROFIA= aumento delle dimensioni delle fibre muscolari 2. TACHICARDIA= pompa più sangue nell’unità di tempo 3. DILATAZIONE DEL VENTRICOLO
In una situazione come quella dell’embolia polmonare acuta, che si realizza nel giro di secondi, non scatterà il meccanismo dell’ipertrofia (perché non c’è abbastanza tempo) ma avremo tachicardia e dilatazione ventricolare.Quindi ad un sovraccarico acuto della
57
pressione, corrisponderà una dilatazione ventricolare, (nei casi più gravi) e poi una disfunzione del ventricolo dx che non riuscirà a mantenere un flusso adeguato. Questo fatto è importante per capire il quadro clinico dell’embolia polmonare.
Quadri clinici
• EP massiva • EP severa • EP lieve moderata • Infarto polmonare, è dovuto alla formazione di circoli collaterali con le diramazioni
delle arterie bronchiali, rami dell’aorta. L’infarto polmonare, in genere si manifesta con dolore di tipo pleuritico, tosse ed emottisi.
• EP non trombotica, gli emboli possono essere di materiale gassoso e di materiale grasso in conseguenza a fratture ossee.
Segni e sintomi
• Ipotensione • Dispnea • Cianosi • Dolore toracico • Tachicardia • Segni di scompenso del cuore destro (turgore delle giugulari)
• Dolore pleuritico • Tosse segni tipici dell’infarto polmonare • Emottisi
Diagnosi differenziale
• Infarto miocardico • Angina instabile • Polmonite • Asma • Pericardite • Pneumotorace • Dolore muscolare • Ansia – crisi di panico
Diagnosi
Segni tipici di embolia polmonare massiva
58
• D-dimeri (prodotti della degradazione della fibrina e quindi di attivazione dei processi
edogeni trombolitici) • ECG, può evidenziare alterazioni del ritmo, segni di dilatazione striale destra o segni di
sovraccarico ventricolare destro • Emogasanalisi, per verificare ipossiemia e ipercapnia • Rx torace • TC spirale con mdc, serve per evidenziare il trombo • Scintigrafia polmonare perfusionale, rimane la metodica più comunemente usata per la
diagnosi di embolia polmonare, in presenza di ostruzioni vascolari singole o multiple si evidenziano una o più aree polmonari non raggiunte dal tracciante radioattivo (non per fuse)
• Ecocardiogramma, può evidenziare la presenza di trombi nelle cavità cardiache • Angiografia polmonare, viene utilizzata più a scopo terapeutico che diagnostico
attraverso l’iniezione di antitrombotici. ANGIO JET il trombo viene aspirato. Terapia
• Anticoagulanti, eparina non frammentata che viene immessa nell’organismo per via endovenosa deve essere fatto il dosaggio del PTT (tromboplastina parziale) per verificare il dosaggio dell’eparina. Vengono utilizzate le eparine con basso peso molecolare che vengono iniettate per via sottocutanea.
• Trombolisi • Chirurgia • Filtro cavale, ombrello messo nella vena cava per bloccare gli emboli e per non
permettergli di andare al cuore. Profilassi Eparina a basso peso molecolare
60
BRONCOPNEUMOPATIA CRONICA OSTRUTTIVA (BPCO)
Il termine broncopneumopatia cronica ostruttica (BPCO) definisce una condizione di ostruzione cronica delle vie aeree, lentamente progressiva, causata da un’infiammazione cronica delle vie aeree e del parenchima polmonare. La BPCO comprende due distinte entità: la bronchite cronica e l’enfisema, quasi sempre coesistenti, seppure in gradi differenti. L’ostruzione delle vie aeree è, nella sua massima parte, fissa e non reversibile (al contrario di quanto accade nell’asma bronchiale), ma può coesistere una certa quota di reversibilità dell’ostruzione stessa e di iperreattività bronchiale.
• Bronchite cronica: Presenza di tosse produttiva non riferibile ad altre cause per almeno 3 mesi all’anno in almeno due anni consecutivi
• Enfisema polmonare: Ampliamento degli spazi a valle del bronchiolo terminale con
distruzione del parenchima polmonare.
La caratteristica fondamentale della BPCO è l’accelerato declino della VEMS o FEV1 (volume espiratorio massimo al 1° secondo)
Patogenesi Stress ossidativo → La bronchite cronica attraverso l’infiammazione causa → Distruzione Fattori di rischio
• Fumo: il fumo di tabacco è il più importante fattore di rischio per lo sviluppo di BPCO. Il fumo attiva i processi infiammatori a livello delle vie respiratorie, inibisce la motilità ciliare, causa l’ipertrofia delle ghiandole mucosecernenti e provoca lo spasmo della muscolatura liscia bronchiale.
• Inquinamento atmosferico, Fattori professionale, Infezioni respiratorie: sono condizioni che possono essere associate alla comparsa e alla pregressione dell’ostruzione delle vie aeree.
• Deficit di α1- antitripsina: Questa è un inibitore delle proteasi, prodotta dal fegato e da altre cellule del sistema immunitario, che contrasta l’azione delle elastasi prodotte dai neutrofili, proteggendo così l’integrità delle fibre elastiche del tessuto polmonare. Particolari alterazioni genetiche portano alla produzione di una proteina alterata che non svolge correttamente il suo ruolo protettivo, conducendo allo sviluppo precoce di enfisema grave e bronchite cronica.
61
Anatomia patologica I processi infiammatori e le alterazioni strutturali propri della BPCO coinvolgono sia le grandi e le piccole vie aeree, sia le unità respiratorie; un ruolo importante è svolto da macrofagi, neutrofili elinfociti T CD8+. L’ostacolo al flusso dell’aria nella BPCO è dovuto principalmente al restringimento delle piccole vie respiratorie. La caratteristica distintiva della bronchite cronica è l’ipertrofia delle ghiandole mucosecernenti dei grossi bronchi. L’ostruzione delle piccole vie respiratorie è dovuto a una serie di meccanismi concomitanti:
1. Edema e infiltrazione infiammatoria delle pareti bronchiali 2. Iperplasia (aumento del numero delle cellule) delle cellule calciformi 3. Fibrosi peribronchiale 4. Presenza di abbondanti quantità di muco nel lume 5. Ipertrofia (aumento del volume delle cellule) delle cellule muscolari liscie
Nell’enfisema risulta alterata la struttura distale al bronchiolo respiratorio, cioè l’acino ed è ridotta la forza di retrazione elastica polmonare.
1. Enfisema centroacinare: Viene distrutta principalmente la porzione centrale del lobulo, cioè i bronchioli respiratori, mentre rimangono integri i dotti alveolari e gli alveoli. Al centro dell’acino si crea una zona ben ventilata, ma non per fusa, per la distruzione dei capillari. In periferia gli alveoli tendono a chiudersi; viene a crearsi una zona ben per fusa ma poco ventilata. Questo tipo di enfisema si manifesta quasi esclusivamente nei fumatori.
2. Enfisema panacinare: In questo tipo di enfisema risultano alterate entrambe le porzioni globulari, sia centrale sia periferica; la distruzione della regione alveolo-capillare altera anche in questo caso il rapporto V/Q e, quindi, lo scambio gassoso. Può essere dovuto al deficit α1- antitripsina, e si distribuisce prevalentemente alle basi polmonari.
62
Fisiopatologia Ostruzione al flusso di aria → aumento del lavoro respiratorio
• Perdita del ritorno elastico del polmone: (es. da distruzione delle fibre elastiche olmonari dovuta alla danno ai setti alveolari): questo rappresenta un fattore molto importante soprattutto per l’espirazione
• Riduzione del lume dei bronchi: dovuto a edema causato dall’ infiammazione
Tutti questi fattori(perdita del ritorno elastico e riduzione del lume bronchiale )causano: Iperinsufflazione (aumento della capacità funzionale residua) L’iperinsufflazione però determina una stasi di ossigeno(quadro di patologia ostruttiva) nei polmoni a causa di: Alterazioni degli scambi gassosi
Ostruzione: inadeguato rapporto ventilazione/perfusione → ipossiemia Enfisema: distruzione degli alveoli →alta V/Q al centro e bassa V/Q alla periferia
63
Nelle fasi avanzate si ha anche: Deficit ventilatorio: riduzione del drive ventilatorio → ipossiemia + ipocapnia (solo in alcuni pazienti) Circolazione polmonare: Distruzione capillare e vasocostrizione indotta dall’ ipossia. La
vasocostrizione dei vasi polmonari determina un aumento di pressione che si ripercuote sull’atrio e Ventricolo destro del cuore che si ipertrofizza determinando il quadro del cuore polmonare cronico
Eritrocitosi (aumenta la produzione di globuli rossi in rsposta all’ipossia. La produzione da parte del midollo emopoietico è stimolata dall’eritropoietina secreta dal rene in condizioni di ipossiemia) che determina ridotta fluidità del sangue (aumenta quindi l’ematocrito ovvero la % di componente corpuscolata rispetto al volume totale di sangue)
Manifestazioni cliniche La storia clinica della BPCO è segnata da una progressione lenta con una relativa stabilità clinica, alternata a periodiche riacutizzazioni di malattia. Nella maggior parte dei casi le riacutizzazioni sono dovute a intercorrenti infezioni virali o batteriche dell’apparato respiratorio, e si presentano preferenzialmente nella stagione fredda. La BPCO si manifesta in soggetti di 40-50 anni, fumatori da almeno 20 anni di circa 20 sigarette al giorno. La tosse è un sintomo comune e precoce, ma non è indice di BPCO. Sia la bronchite cronica che l’enfisema, infatti, possono essere presenti in assenza di ostruzione bronchiale, mentre questa è sempre presente quando comincia a manifestarsi la dispnea. Lescreato è generalmente mucoso, e può divenire purulento in occasione delle riacutizzazioni, nel corso delle quali può comparire anche respiro sibilante. La dispnea, inizialmente, compare solo durante le riacutizzazioni e in seguito a sforzi fisici, e solo in uno stadio molto avanzato anche a riposo. Nelle fasi più avanzate della malattia il paziente può assumere la posizione “a tripode”, con il collo e il tronco protesi in avanti verso un piano di sostegno, e il peso del corpo appoggiato sulle braccia. Diagnosi
• Rx torace, mette in evidenza l’aumento della trasparenza dei polmoni dovuto all’enfisema
• Test spirometrici, la spirometria documenta una riduzione della VEMS o FEV1 (volume espiratorio massimo al 1° secondo)
• Emogasanalisi
64
Trattamento
• Cessazione del fumo • Broncodilatatori (β2-agonisti, anticolinergici, teofillinici) • Corticosteroidi • Ossigenoterapia
SEVERITA’ DELLA BPCO
Lieve
Moderata
Avanzata
65
VERSAMENTO PLEURICO
Lo spazio pleurico è uno spazio virtuale compreso tra la pleura parietale e la pleura viscerale, e contiene solo una minima quantità di liquido. La pleura parietale ricopre la superficie interna della gabbia toracica, il diaframma e il mediastino; la pleura viscerale, invece, ricopre i p polmoni. Il liquido pleurico ha un basso contenuto di proteine, valori di ph e di glucosio simili a quelli plasmatici e deriva principalmente dai capillari della pleura parietale; il riassorbimento del liquido avviene attraverso i capillari della pleura viscerale e attraverso i linfatici della pleura parietale, per mezzo dei quali viene riassorbita in particolar modo la componente proteica. Si accumula quando è prodotto in eccesso o quando non è assorbito adeguatamente. Versamento pleurico Si definisce versamento pleurico un’eccessiva quantità di liquido nello spazio pleurico rispetto a quella fisiologicamente presente. I versamenti vengono distinti in trasudatizi ed essudatizi in base alle caratteristiche del liquido.
• Il versamento trasudatizio: è dovuto a un aumento della produzione del liquido pleurico per incremento della pressione idrostatica capillare o per riduzione della pressione oncotica intravascolare (cioè della pressione esercitata dalle proteine plasmatiche). La barriera formata dalla parete capillare non è alterata, e il liquido che la attraversa (che trasuda) viene filtrato delle componenti cellulari e delle proteine.
• Il versamento essudatizio: è dovuto all’azione di fattori locali che aumentano alterano
la normale produzione del liquido pleurico e/o no ostacolano il riassorbimento. L’infiammazione della pleura provoca un aumento della permeabilità della parete dei capillari e il conseguente accumulo nello sapzio pleurico di liquido con elevato contenuto proteico e cellulare. Oltre che alle numerose malattie che causano infiammazione pleurica, i versamenti essudatizi possono, più raramente, essere secondari a traumi o ad alterato drenaggio linfatico.
Meccanismi: alterazione delle forze di Starling: Alterazione delle forze di Starling: sono delle pressioni in gioco che determinano la fuoriuscita del liquido interstiziale dalla parete delle arteriole e il ritorno dello stesso nel lume delle venule. Nelle arteriole c’è una pressione pari a 11 MMHg che spinge il liquido fuori dal lume, invece nelle venule c’è una pressione pari a 9 MMHg che richiama il liquido nel proprio lume.
66
Manifestazioni cliniche I piccoli versamenti pleurici possono essere asintomatici, mentre quelli di entità rilevante, soprattutto in presenza di malattie cardio-polmonari, causano dispnea. Possono essere presenti tosse e dolore toracico di tipo pleuritico, generato da coinvolgimento infiammatorio della pleura parietale, tipicamente accentuato dall’inspirazione profonda e dai colpi di tosse. Il dolore di tipo pleuritico indica la presenza di un essudato. Esami diagnostici La toracentesi è necessaria per definire le caratteristiche del liquido pleurico e permette una diagnosi. Può essere attuata a solo scopi diagnostici, o terapeutici (toracentesi evacuativa) in presenza di voluminosi versamenti. L’aspetto del liquido può indirizzare verso precise ipotesi diagnostiche.
67
CUORE POLMONARE
Ingrandimento del ventricolo destro, con o senza scompenso cardiaco, secondari a una malattia primitiva del polmone. Cuore polmonare:
1. Acuto o subacuto – P.es. embolia polmonare
2. Cronico – P.es. BPCO Caratteristiche del cuore destro:
Spessore sottile Lavoro a pressione più bassa (ca.25/10 mmHg, media 15 mmHg)
Cuore polmonare acuto
Embolia polmonare multipla o massiva Insufficienza del cuore destro con pressioni >50 mmHg Aspetti clinici:
• Pallore • Sudorazione • Ipotensione • Tachicardia • Turgore delle vene giugulari
PaO2 bassa, PaCO2 bassa Cuore polmonare cronico Da cause vascolari
• Micro-embolia • Vasculiti • Farmaci o droghe • Ipertensione polmonare primitiva
68
Da malattie polmonari
• Ostruttive (BPCO)
• Restrittive parenchimali (fibrosi polmonare, resezione polmonare)
• Restrittive extraparenchimali (Obesità, malattie neuromuscolari, alterazioni della gabbia toracica)
Aspetti clinici: Reperti della malattia di base Dispnea, tachipnea Turgore giugulari Epatomegalia Reflusso epato-giugulare Diagnosi: Alterazioni emogasanalitiche ECG Rx torace Ecocardiogramma Cateterismo cardiaco dx
69
Edema Aumento della quantità di liquidi negli spazi interstiziali Ascite Idrotorace Anasarca Patogenesi: Forze di Starling Danno capillare Riduzione del volume arterioso efficace Ridotta portata cardiaca Fattori renali Sistemi sodio-ritentivi (RAA, ADH, SNS)
Edema Polmonare
70
Diagnosi differenziale delle cause di edema sulla base delle caratteristiche del liquido (p.es ascitico)
Condizione Aspetto Gradiente S/A
albumina Cellule
Cirrosi Giallastro
>1.1 Scarse
Neoplasia Giallo-Emorragico
<1.1 Variabile
Tubercolosi Torbido <1.1 Linfociti
Peritonite Torbido o Purulento
<1.1 PMN
Scompenso cardiaco
Giallastro
>1.1 Scarse