Verso una terapia genica del cancro - Kataweb
Transcript of Verso una terapia genica del cancro - Kataweb
38 LE SCIENZE 389/ gennaio 2001
Il cancromammario e le suemetastasi possonoessere combattutimediante inibitoridell'angiogenesi; lo
suggeriscono gliesperimenti
condotti suglianimali transgenici
di Maria Grazia Sacco, EnricaMira Catò e Paolo Vezzoni
TUMORE PRIMARIO
SEPARAZIONEDELLE SINGOLE
CELLULE
COLTURADI CELLULETUMORALI
INOCULO IN TOPIIMMUNODEPRESSI
O SINGENICI
PROTOCOLLITERAPEUTICI
PER INIBIRE LA CRESCITATUMORALE VALUTAZIONE
DEI RISULTATI
Verso una terapia genica del cancroG
li animali transgenici sono stati introdotti nella ri-cerca biomedica da oltre venti anni e si sono di-mostrati utili nei settori più svariati, dalla ricerca
di base alla produzione di farmaci, sollevando presso l'opi-nione pubblica una serie di domande e preoccupazioni inparte fondate, ma troppo spesso affrontate con affermazioniimprecise o addirittura volutamente tendenziose.
In ogni campo della vita, costi e benefici vanno sempre pe-sati attentamente. Non discuteremo qui il ruolo degli anima-li nella ricerca biomedica, aspetto già ampiamente trattato suquesta rivista, in particolare nel fascicolo del febbraio 1997.Vorremmo invece proporre un ulteriore esempio dell'utilitàdi queste tecnologie per indagare un problema di grande in-teresse quale la ricerca di nuove terapie contro il cancro.
Gli ultimi anni hanno visto enormi progressi nella com-prensione dei meccanismi alla base della trasformazione edella crescita tumorale. Sono stati identificati geni la cui atti-vazione (nel caso degli oncogèni) o inattivazione (nel caso deisoppressori tumorali) provoca il cancro e altri che contribui-scono alla capacità di dare metastasi. In patologia umana ladiagnosi strumentale permette di evidenziare tumori in faseassai precoce, mentre la classificazione istopatologica è di-ventata altamente precisa e sofisticata. Tuttavia a tali avanza-menti non ha fatto riscontro un corrispondente miglioramen-to della capacità di trattare i tumori, nonostante oggi si di-sponga di tecniche potenzialmente assai promettenti.
Il problema della sperimentazioneQuesto proliferare di nuovi approcci al trattamento dei
tumori non può che essere valutato attraverso modelli ani-mali ai quali si richiede un'elevata affidabilità. Anni fa,quando, presso il nostro laboratorio dell'Istituto di tecnolo-gie biomediche avanzate (ITBA) del CNR di Segrate coordi-nato da Renato Dulbecco, abbiamo iniziato a interessarci al-la possibilità di utilizzare i nuovi dati della genetica moleco-lare per inibire la crescita tumorale, il problema della sceltadel modello ci è subito apparso centrale. (In quegli anni lenostre ricerche rientravano nell'ambito del Progetto finaliz-zato « Oncologia >> del CNR, di un Progetto coordinato dal-l'Associazione italiana per la ricerca sul cancro, ed erano ingran parte finanziate dalla Cariplo.) Sorprendentemente,però, avevamo constatato che tale problema era assoluta-mente ignorato nell'ambito dell'oncologia sperimentale.
La stragrande maggioranza dei modelli utilizzati si basasu sistemi assolutamente artificiali quali i tumori trapianta-bili, cioè linee tumorali coltivate in laboratorio e poi inocu-late in ceppi particolari di animali singenici o immunode-pressi sui quali viene valutata l'efficacia degli interventi tera-peutici. In realtà il modello ha poco o nulla a che fare conquanto accade in patologia umana, dov il processo tumora-le è un processo che avviene attraverso vari passaggi durantei quali il genoma di una o al massimo di poche cellule subi-sce una serie di mutazioni che hanno come risultato finalel'invasione dei tessuti circostanti e la metastatizzazione a di-stanza. Durante questo processo la singola cellula deve adat-tarsi al suo microambiente, eludendo i segnali delle cellule
LE SCIENZE 389/ gennaio 2001
SVILUPPO DI TUMORITRAPIANTATI
La maggior parte degli studi di oncologia viene svolta su ceppi ditopi immunodepressi o immunologicamente compatibili in cuivengono inoculate cellule ottenute da tumori primitivi. Sul tumo-re che si sviluppa vengono poi messe alla prova le varie terapie.L'efficacia del trattamento viene valutata confrontando la cresci-ta dei tumori rispetto a topi controllo. Nella pagina a fronte, inalto, microiniezione di cellule in una blastocisti; in basso, topi ot-tenuti con questa procedura. Quello di sinistra è chiaramentechimerico, cioè derivato in parte dalle cellule iniettate.
39
IL LIPOSOMASI INTEGRAfrogoomenCra3E:A MEMBRANA
.,- ,911//* , CELLULARE
GENETERAPEUTICO
CELLULA
LIPIDI
DNAPLASMIDICO
-.2,*••... •
DNA
PLASMIDICO
atif #(::;P'2) RIBOSOMA
IMPIANTODEGLI EMBRIONIMICROINIETTATI
NELL'UTERODI FEMMINE
PSEUDOGRAVIDE
44010~PROTOCOLLI TERAPEUTICIPER INIBIRE LA CRESCITA
TUMORALE
EMBRIONETRANSGENICO
TOPINOTRANSGENICO
TOPINI NORMALI
SVILUPPODI TUMORISPONTANEI
CELLULE
+bFGF +VEGF
CELLULETUMORALI
ANGIOSTATINAENDOSTATINA
circostanti, aggirare il controllo del si-stema immunitario, superare le barrie-re fornite dai vari strati di tessuti che lacircondano, invadendoli, entrare neicapillari linfatici e sanguigni, viaggiareper lunghi tratti, fermarsi nei vari tes-suti e dare origine alle metastasi con uncomplicato processo che richiede, tral'altro, la formazione di nuovi vasi.
Tutto questo ha poco a che fare conl'inoculo di numerose cellule tumoraligeneralmente in zone, come Io stratosottocutaneo, il peritoneo o il torrentecircolatorio, che non sono l'ambientein cui il tumore cresce normalmente.Inoltre, queste cellule sono state man-tenute in coltura, in vari laboratori, perun tempo indefinito ed è assai dubbioche rappresentino ormai il tumore dacui sono derivate. Infatti, durante lacoltura, avviene una serie di nuoviadattamenti e di alterazioni geneticheimpossibili da tenere sotto controllo.Inoltre, particolare assai importante, lamaggior parte dei tumori di questo ge-nere non dà origine a metastasi.
Si capisce quindi come si possa legit-timamente mettere in dubbio la rile-vanza di questi modelli per la valuta-zione di nuove strategie terapeutiche.Questi sistemi sono sopravvissuti pervia della loro comodità per lo speri-mentatore. Entro limiti ragionevoli, itumori che vengono inoculati negli ani-mali nello stesso esperimento sono ab-bastanza simili tra loro, il che semplifi-ca l'analisi statistica dei dati, mentre itumori spontanei o indotti da cancero-geni sono rari, eterogenei e insorgonogeneralmente in topi più vecchi, il cherichiederebbe tempi di osservazionepiù lunghi e un gran numero di anima-li per la valutazione.
I vantaggi offertidai topi tra nsgenici
L'inadeguatezza di questi sistemi,che pure costituiscono il 99,9 per centodegli esperimenti riportati in letteratu-ra, ci ha indirizzato verso la scelta diun modello diverso. A partire dagli stu-di di Phil Leder, è diventato chiaro cheè possibile far insorgere tumori in ani-mali da esperimento se l'espressione diparticolari geni viene forzata in un par-ticolare tessuto. Il primo topo di Leder portava l'oncogène c-myc sotto il controllo di sequenze regolatrici in grado di far-lo esprimere ad alti livelli nella ghiandola mammaria. Que-sto topo, detto anche topo di Harvard od oncomouse, di-venne famoso in quanto fu il primo organismo transgenicoper cui si chiese e si ottenne il brevetto. In ess però i tumoridella mammella insorgevano in maniera sporadica e conlunga latenza. Per questo abbiamo preferito puntare la no-stra attenzione su un topo transgenico per l'oncogène neu,messo a punto da W. J. Muller nel laboratorio di Leder, e loabbiamo riprodotto nel nostro laboratorio.
PRONUCLEO MASCHILE
MICROINIEZIONE DI DNANEL PRONUCLEO MASCHILE
VALUTAZIONE
DEI RISULTATI
L'oncogène neu sembrerebbe coinvolto nella patogenesidel carcinoma mammario umano e una sua amplificazioneporta a una maggior malignità della neoplasia. In questi topii tumori mammari insorgono nel 100 per cento delle femmi-ne in tutte le ghiandole mammarie, con elevata riproducibi-lità nel tempo e in maniera simmetrica; diventano palpabiligeneralmente verso il secondo mese per crescere poi con unacerta rapidità, fino ad arrivare verso il quinto mese a una di-mensione tale da richiedere il sacrificio dell'animale. Inoltrecrescono nel loro microambiente naturale, cui devono adat-tarsi per superare l'inibizione costituita da altre cellule confi-
Per poter crescere oltre una certa dimen-sione il tumore deve sviluppare nuovi va-si che possano nutrirlo adeguatamente.Questo processo avviene normalmentedurante lo sviluppo e, in condizioni pato-logiche, anche nell'adulto, per esempiodurante la crescita tumorale. Sono statigià identificati molti dei fattori coinvoltiin questo processo, come il bFGF (basic MESODERMICHE
Fibroblast Growth Factor) e il VEGF(Vascular-Endothefial Growth Factor). Siritiene che a un certo punto della sua cre-scita il tumore acquisisca la capacità disecernere questi o simili fattori che stimo-lano la crescita di vasi al suo interno. Gliinibitori della crescita di cellule endotelia-li, come l'angiostatina e l'endostatina,bloccano questo processo impedendo lacrescita di vasi e quindi la crescita neopla-stica. Tale proprietà potrebbe avere gran-di risvolti nella terapia dei tumori.
RNA MESSAGGERO
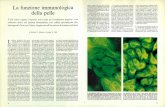
Gran parte dei tentativi di terapia genica nell'uomo fa uso divettori virali, ossia di sistemi che utilizzano virus presenti in na-tura e, dopo averli modificati, fa in modo che questi portino al-l'interno delle cellule il gene che si vuole introdurre. La metodicanon è però del tutto sicura, come ha dimostrato il decesso negliStati Uniti di un paziente trattato con una dose molto elevata diun vettore adenovirale. Per questo i liposomi, collaudati nell'uo-mo da lungo tempo, sono una valida alternativa. Il DNA genicoda trasferire viene associato a particolari vescicole lipidiche chepossono aderire e fondersi con la membrana cellulare, rilascian-do così all'interno delle cellule il DNA in esse contenuto.
NUOVI VASI IRRORANOILTUMORE IN ACCRESCIMENTO
nanti e dalle cellule di altri tessuti nonché dalle cellule del si-stema immunitario. La notevole riproducibilità delle neo-plasie nelle varie generazioni consente di pianificare gli espe-rimenti con una certa facilità e di confrontare tra loro tratta-menti effettuati in tempi diversi. Infine, il tumore dà originea metastasi a distanza, la vera causa di morte per il cancrodella mammella in campo umano. Questo spiega il vantag-gio di disporre di un modello animale in cui valutare l'effet-to delle terapie sulle metastasi.
Come si può arrivare a una terapiagenica dei tumori
Nel corso degli ultimi dieci anni, la terapia genica si è av-valsa di una varietà di approcci che hanno preso in conside-razione diversi aspetti della fisiologia, della biochimica e del-la genetica dei tumori. In generale però, dopo dieci anni ditentativi anche in campi diversi dall'oncologia, i sistemi ditrasferimento (anche i più promettenti quali gli adenovirus)si sono rivelati poco efficaci. Si è visto, infatti, che sono solopoche le cellule che esprimono il gene desiderato per un tem-po sufficientemente lungo e a livelli terapeuticamente utili.
Nel caso del cancro, poi, il problema sembra ancora piùcomplesso per non dire insormontabile. È noto che, con lachemioterapia, si può ottenere la scomparsa del 99,99 percento delle masse tumorali, ma che a distanza di tempo il tu-more può ricrescere. Come è possibile quindi sperare di ot-tenere un effetto duraturo utilizzando procedure che sonoben lontane dal trasformare percentuali di cellule così eleva-te? Se non riusciamo a inserire i geni «terapeutici>' non dicoin tutte ma almeno in una consistente parte delle cellule, cheeffetto potremo mai avere? Malgrado ciò, sono stati effet-tuati nell'uomo numerosi studi di questo genere, con risulta-ti in effetti scarsi.
Tuttavia vi sono due approcci che potenzialmente supera-no il problema. Il primo è quello immunologico, che potreb-be essere in grado di distruggere tutte le cellule tumorali an-che se venisse geneticamente modificata solo una piccolaporzione di cellule, in quanto il sistema immune è in gradodi amplificare la risposta. La speranza riposta in vaccini o al-tre manovre che inducano l'organismo a rigettare il tumorerisale agli albori dell'oncologia moderna. Negli anni settan-ta, molti reagenti che stimolavano aspecificamente il sistemaimmunitario, quali il vaccino antitubercolare (BCG), conob-
PRONUCLEO FEMMIN1
RECUPERODEGLI EMBRIONI
Non sempre i risultati ottenuti con i tumori impiantati nei topi sono applicabili all'uo-mo. Una valida alternativa potrebbe essere fornita dagli animali transgenici che, comemostra lo schema, si ottengono introducendo, mediante microiniezione, un gene parti-colare nell'embrione di topo allo stadio di una cellula. Alcuni degli animali così ottenutipresenteranno questo gene in tutte le cellule dell'organismo adulto. Conoscendo i geniresponsabili della patogenesi dei tumori umani è possibile progettare animali transgeni-ci che sviluppino tumori di un particolare tipo. Per esempio, inserendo l'oncogène neusi ottengono topi che, sviluppando tumori simili al carcinoma della mammella umano,inclusa la capacità di dare metastasi, si prestano bene allo studio di efficaci terapie.
SECREZIONE DI VEGF,bFGF,TGF-B
CELLULEENDOTELIALI
CELLULEMUSCOLARI
LISCE
40 LE SCIENZE 389/ gennaio 2001 LE SCIENZE 389/ gennaio 2001 41
VETTORE VIRALEHSV-TK
•nn•nnn303.=111.3~
iINFEZIONE
SOMMINISTRAZIONEDI GANCICLOVIR
eo
MORTECELLULARE
•'
IL GENE VIRALE SI INTEGRANEL DNA DELLA
CELLULA TUMORALE
La strategia antitumorale che fa uso dei geni suicida si basa sul principio di inserire nel-le cellule tumorali geni tossici per la cellula. Tra questi, il più usato è quello che sfruttaalcune proprietà della timidina chinasi (TK) del virus herpes simplex. Tale enzima è de-putato alla fosforilazione della timidina, il nucleoside da cui si ottiene il TTP (timidinatrifosfato) che viene poi incorporato nel DNA cellulare. In pratica, la TK è uno degli en-zimi che produce i mattoni che la DNA polimerasi usa per replicare il DNA e quindi èindispensabile per la crescita sia delle cellule normali, sia di quelle neoplastiche. Tutta-via, a differenza della TK dei mammiferi, quella virale fosforila non solo la timidina,ma anche alcuni suoi analoghi che provocano gravi alterazioni nel DNA, così che la cel-lula in replicazione viene danneggiata irreparabilmente. Pertanto si possono indurre lecellule tumorali a «suicidarsi» inserendo in esse il gene per la TK virale e poi sommini-strando loro uno di questi analoghi come il ganciclovir, che invece non danneggia le cel-lule normali prive dell'enzima virale.
INSERZIONEDI PLASMIDI
CON CITOCHINE:IL-2, IL-4, IL-12...NELLE CELLULE
TUMORALI
LE CELLULETUMORALI PRODUCONO
CITOCHINE CHE STIMOLANO *D CD
LA RISPOSTAIMMUNITARIA
DISTRUZIONEDEL TUMORE
bero periodi di grande utilizzo, anchese ora sono praticamente abbandonati.Negli anni ottanta Steven A. Rosen-berg e i suoi collaboratori avevano ac-ceso molte speranze con un sistema incui si cercava di attivare le cellulelinfoidi del paziente stesso a reagirecontro il tumore (si veda l'articolo Im-munoterapia adottiva contro il cancrodi S. A. Rosenberg in «Le Scienze» n.263, luglio 1990). Ma le numerosesperimentazioni basate su questa ipote-si e i vari trial clinici non riuscirono adare risultati soddisfacenti.
Il secondo approccio, che potrebbefunzionare anche se il trasferimento ge-nico avvenisse in maniera incompleta,si basa sugli studi ormai trentennali diJudah Folkman (si veda il suo articoloCombattere il cancro attaccandone lavascolarizzazione in «Le Scienze», n.339, novembre 1996). L' ipotesi espo-sta nell'articolo ha avuto un recente ri-lancio in concomitanza con l'isolamen-to dell'angiostatina e dell'endostatina,due molecole prodotte dall'organismostesso a partire dai loro precursori, chesi sono dimostrate in grado di ridurre obloccare la crescita tumorale.
Su che principio si basa l'efficacia diqueste molecole? Secondo il paradigmaufficiale, le prime cellule neoplastiche siformano e si duplicano come le altrecellule del tessuto da cui sono derivate,ma, raggiunta una certa massa critica,devono, per poter crescere ulteriormente, stimolare la cresci-ta di nuovi vasi per avere il necessario nutrimento. Comequesto avvenga costituisce uno dei settori d'indagine più sti-molanti dell'oncologia molecolare. La produzione di nuovivasi sembrerebbe essere il risultato dell'attività di fattori atti-vanti e inibenti la proliferazione delle cellule endoteliali checostituiscono le pareti dei vasi.
Negli studi iniziali Folkman aveva somministrato ad ani-mali con tumori trapiantati queste proteine purificate più omeno come si fa per un normale farmaco, ottenendo la ripe-tuta regressione del tumore fino addirittura al suo controllocompleto anche quando la terapia veniva sospesa.
La notizia, che fece il giro del mondo, non può essere sot-tovalutata. La terapia non risultava per niente tossica, sem-brava avesse un effetto definitivo e il tumore non sviluppavaresistenza, come invece si verifica regolarmente con i che-mioterapici tradizionali. Studi successivi hanno sollevato tut-tavia due problemi: il primo riguarda l'estrema difficoltà diottenere questi farmaci come proteine, che devono essere pu-rificate dagli organismi stessi o venire prodotte con tecnichedi ingegneria genetica. Una possibilità fornita dalla terapiagenica era quella di far produrre le proteine dall'organismostesso portatore di tumore. In effetti, per la somministrazio-ne giornaliera nell'uomo, che pesa oltre 1000 volte un topo,non si sarebbe al momento in grado di disporre di materialesufficiente.
Primi risultati delle terapie genicheRimaneva poi il problema se il modello utilizzato non fos-
se troppo ottimistico per le ragioni che abbiamo già esposto.Negli ultimi cinque anni, abbiamo utilizzato il nostro model-
lo di topo transgenico per l'oncogène neu per provare variestrategie di terapia genica antitumorale. Abbiamo così testa-to i geni suicidi, gli antisenso, le connessine (che rafforzano ilcontatto tra le cellule). In tutti i casi abbiamo osservato unaparziale riduzione della crescita tumorale a livello locale,senza tuttavia ottenere una completa scomparsa del tumoree un effetto sistemico a distanza. Con l'interleuchina 4, unamolecola che stimola il sistema immunitario, abbiamo ipo-tizzato anche un effetto a distanza sul tumore controlateraleo addirittura sulle metastasi. Quest'ultimo parametro è statopertanto valutato, senza che si sia notato un effetto di sicurosignificato sulla crescita delle metastasi polmonari. Questi ri-sultati sono assai simili a quelli riportati per l'uomo, in cuigeneralmente si ottengono solo regressioni parziali.
Il trattamento mediante angiostatina ed endostatina do-vrebbe invece avere un effetto su tutto l'organismo. Questeproteine esercitano infatti la loro azione non all'interno del-la cellula, ma nel torrente circolatorio e quindi possono ve-nir somministrate come un farmaco tradizionale. Inoltre, laloro azione non sarebbe quella di eliminare completamentele cellule tumorali, bensì di impedirne la crescita oltre unacerta dimensione. Pertanto esse potrebbero venire prodotteda un numero limitato di cellule, anche non tumorali, pro-ducendo un effetto che si ripercuoterebbe su tutto il tumoree potenzialmente anche sulle sue metastasi.
Abbiamo così trattato gli animali con un vettore d'espres-sione veicolato da liposomi all'interno delle cellule. La sceltadei liposomi ha alcuni vantaggi nei confronti dell'impiegonell'uomo: essi sono già utilizzati in clinica e cosmesi, nonpresentano alcuna controindicazione medica né effetti colla-terali; inoltre possono essere utilizzati anche in strutture tec-nologicamente non molto avanzate.
I trattamenti degli animali sono iniziati a due mesi di etàinoculando i liposomi all'interno del tumore e l'effetto è sta-to valutato tre mesi dopo. I risultati sono stati positivi ancherispetto a quelli ottenuti nei topi trattati con i precedenti ap-procci di terapia genica.
Bloccare le metastasiMa i risultati più significativi sono stati ottenuti analizzan-
do le metastasi. Circa il 75 per cento dei topi transgenici nontrattati sviluppa metastasi a 5 mesi di età. Al contrario nessu-no dei topi trattati con angiostatina ha presentato metastasiall'autopsia eseguita alla stessa età. Si tratta di un risultatoche dimostra, per la prima volta e in un modello spontaneo,la possibilità di modificare il decorso delle metastasi attraver-so una terapia basata sugli inibitori dell'angiogenesi.
Come sempre nella ricerca, i risultati vanno letti per quel-lo che sono e le generalizzazioni devono essere prudenti.Quello che lo studio ha dimostrato è che in un modello di
PAOLO VEZZONI, MARIA GRAZIA SACCO ed ENRI-CA MIRA CATÒ sono ricercatori presso l'Istituto di tecnolo-gie biomediche avanzate del CNR di Segrate (Milano) nel-l'ambito del Progetto Genoma. Oltre a identificare i geni re-sponsabili di varie malattie, il gruppo dell'I I I3A ha introdottola tecnologia degli animali transgenici in Italia. Tra i risultatiottenuti vi è la produzione di topi transgenici per lo studio dicomposti tossici e la messa a punto di un modello transgenicoper la validazione di procedure di terapia genica del cancro.
È possibile che la proliferazione del tessuto tumorale avvengaquando la sorveglianza normalmente esercitata dal sistema im-munitario viene elusa da alcune caratteristiche delle cellule tu-morali. Gli approcci basati su questa ipotesi fanno in modo distimolare il sistema immunitario affinché reagisca contro i tu-mori. Agli esperimenti condotti da parecchi decenni, si affian-cano ora procedure di terapia genica. I geni che inducono laproduzione di molecole che stimolano la risposta immunitaria,le citochine, vengono introdotti nelle cellule tumorali che cosìrichiamano le cellule coinvolte nella distruzione di cellule tu-morali, quali linfociti, macrofagi ed eosinofili. Si spera in talmodo o di distruggere in maniera generica le cellule tumorali odi «smascherare» gli antigeni tumorali in modo che, a loro vol-ta, provochino una forte risposta immunitaria selettiva.
carcinoma mammario relativamente simile a quello umanoun trattamento abbastanza precoce con angiostatina ha ral-lentato la comparsa di metastasi. Ciò non vuol dire che la te-rapia sia in grado di eliminare o rallentare il decorso di meta-stasi già stabilite. Al contrario, gli studi finora pubblicatimostrano che angiostatina ed endostatina sono tanto più ef-ficaci quanto più somministrate precocemente.
In base a questi dati, pertanto, sembra che la terapia possadimostrarsi utile, in un contesto umano, come terapia adiu-vante dopo la rimozione del tumore. Attualmente, la mag-gior parte delle neoplasie mammarie nella donna viene dia-gnosticata quando esse sono circoscritte al seno, e per questomotivo il tumore viene escisso in maniera apparentementeradicale. Tuttavia si sa che in una certa percentuale di casi, adistanza di qualche anno, si manifesteranno metastasi in or-gani vitali per l'organismo. Oggi le pazienti che hanno unaprobabilità maggiore di recidiva sono trattate con la chemio-terapia «preventiva», somministrando cioè farmaci antitu-morali prima che le metastasi si manifestino, nella speranzadi eliminare tutte le cellule potenzialmente già in circolo.
Tali composti presentano un certo numero di effetti colla-terali, oltre a essere per loro stessa natura potenzialmentecancerogeni. Al contrario, la terapia con angiostatina sembrafinora ben tollerata, anche se non è detto che con un uso piùdiffuso non si rivelino problemi diversi. Tuttavia, agendo sumeccanismi differenti, questi inibitori potrebbero rappresen-tare un ulteriore presidio terapeutico i cui benefici andrebbe-ro a sommarsi a quelli forniti dalle terapie tradizionali.
Nella scienza ogni piccolo passo va documentato conprecisione ed esattezza. Per questo motivo stiamo cercandodi migliorare il modello animale transgenico attualmentedisponibile per renderlo ancora più simile a quello umanoper studi preclinici. L'aumento delle nostre conoscenze nel-la genetica della trasformazione tumorale ci consentirà sem-pre più di riprodurre nel roditore gli stessi meccanismi pa-togenetici che avvengono nell'uomo, così da ottenere mo-delli che più si avvicinino a quelli che sono realmente i tu-mori umani.
DULBECCO R., RAINERI P. , VEZZONI P., FARIELLO R., Cl-nazione: problemi etici e prospettive, supplemento a «LeScienze», n. 345, maggio 1997.
SACCO M.G., CANIATTI M., MIRA CATO E., FRATTINI A.,CHIESA G., CERUTI R., ADORNI F., ZECCA L., SCANZIANI E. eVEZZONI P., Liposome-Delivered Angiostatin StronglyInhibits Tumor Growth and Metastatization in a Transge-nic Model of Spontaneous Breast Cancer, in « Cancer Re-search», 60, pp. 2660-2665, 2000.
42 LE SCIENZE 389/ gennaio 2001 43LE SCIENZE 389/ gen na io 2001