Uso delle cellule staminali embrionali come strategia terapeutica per il trapianto renale e la...
-
Upload
crispino-lazzari -
Category
Documents
-
view
216 -
download
2
Transcript of Uso delle cellule staminali embrionali come strategia terapeutica per il trapianto renale e la...

Facoltà di Scienze Matematiche Fisiche e NaturaliCorso di laurea triennale in Scienze Biologiche
Curriculum Biosanitario
Uso delle cellule staminali embrionali come strategia terapeutica per il trapianto renale e la limitazione (risoluzione) del rigetto d'organo
Candidato Relatore Daniela De Rosa Loretta Tuosto
2014/2015

Fisiologia e funzione renale
GLOMERULO: Rete densa di capillari che filtrano il sangue.CAPSULA DI BOWMAN: Cattura il fluido che è stato filtrato fuori dalla circolazione sanguigna e lo trasferisce nei tubuli.TUBULO: Circondato da un singolo strato di cellule specializzate il cui compito è riassorbire acqua ed elettroliti nel sangue
FUNZIONE OMEOSTATI
CA
FUNZIONE ENDOCRIN
A
FUNZIONE ESCRETIVA
Il nefrone è l’unità funzionale del rene

Il trapianto renale CLASSIFICAZIONE
DEI TRAPIANTI
• Trapianto ortotopico• Trapianto eterotopico• Autotrapianto• Isotrapianto• Allotrapianto• Xenotrapianto

Compatibilità dei tessuti
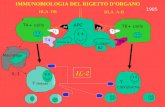
CLASSE I: espresse sulla superficie di tutte le cellule nucleate, fisiologicamente deputate alla presentazione di peptidi antigenici ai linfociti T citotossici CD8+. CLASSE II: espresse sulla membrana di APC (cellule dendritiche, macrofagi, cellule B). Le APC sono fisiologicamente deputate alla presentazione di peptidi antigenici ai linfociti T helper CD4+.
• ANTIGENI ABO• ANTIGENI HLA
I classe HLA-A, HLA-B, HLA-CII classe HLA-DR, -DP-, DQ

Alloriconoscimento
b) INDIRETTA: I frammenti peptidici delle molecole MHC del donatore presentati da MHC II dell’ospite sono riconosciuti come estranei.
a) DIRETTA: I linfociti T del ricevente riconoscono l’MHC intatto del donatore come estraneo.

Il rigetto d’organo
RIGETTO IPERACUTO
RIGETTO ACUTO
RIGETTO CRONICO

Prevenzione e trattamento del rigetto
RIDUZIONE DELL’IMMUNOGENICITA’ Tipizzazione tissutale HLA Tipizzazione del gruppo sanguigno ABO Screening per la presenza di anticorpi preformati Reazione mista linfocitariaIMMUNOSOPPRESSIONE Ciclosporina Tacrolimus Azatiopirina Farmaci antiinfiammatori (corticosteroidi)INDUZIONE DI TOLLERANZA Anergia clonale Apoptosi indotta Sviluppo di linfociti T soppressori / regolatori

• INDIFFERENZIATE • CAPACI DI AUTO RIGENERARSI (self-renewal)• CAPACI DI DIFFERENZIARSI IN TIPI CELLULARI SPECIFICI• CAPACI DI RIPOPOLARE UN TESSUTO in vivo
Cellule staminali
A - le cellule staminali; B - cellule progenitrici; C - cellula differenziata;1 - divisione simmetrica delle cellule staminali; 2 - divisione asimmetrica delle cellule staminali; 3 - divisione progenitore; 4 - terminale di differenziazione
La possibilità di generare organi e tessuti da sostituire a quelli malati a partire da cellule staminali proprie del paziente rappresenta uno dei più recenti obiettivi della medicina rigenerativa.

Classificazione delle staminali

Cellule staminali embrionali
VANTAGGI • Originano cellule
provenienti da tutti e tre i foglietti embrionali.
• Crescita in vitro senza cambiarne fenotipo o cariotipo le rende promettenti per la rigenerazione e per la riparazione dei tessuti.
• Ridotta immunogenicità, piccole quantità di molecole HLA I e nessuna molecola HLA II.
SVANTAGGI • Evoluzione in teratomi.
ICM Oct4, Foxd3
PluripotenzaECTODERMA(tes.nervoso, epiteli e ghiandole, capelli, unghie , cristallino)
MESODERMA(t.osseo, t.muscolare, cuore, vasi ,t. connettivo, pleure, peritoneo, sistema urogenitale)
ENDODERMA(app.digerente, respiratorio, tiroide, paratiroide)

Sviluppo del reneIl rene è un organo di origine
mesodermica
Il MM specificato da Hoxa11, Hoxc11, Hoxd1 , Wt1, per mezzo del rilascio di GDNF promuove l’evaginazione della gemma ureterica, che attraverso FGF2 e BMP7, promuove l’addensamento delle cellule mesenchimali attorno ad essa. GDNF, TGFβ1, BMP4, collagene VIII permettono la ramificazione dell’epitelio Foxb2 permette l’ddensamento pretubulare e il differenziamento in nefroni. Le cellule del cappuccio convertono la vitamina A in acido retinoico per mantenere l’espressione di Ret (recettore GDNF) nella gemma ureterica.

M. Takasato, H. Little et al, mostrano un protocollo che riesce a far differenziare le cellule staminali embrionali umane in tutte quelle necessarie a formare un "mini-organo renale”.
Un rene dalle staminali
MESODERMA IM Hesc ENDODERMA
Reporter “Green Fluorescent Protein”
MIXL1 (segnalatore forte della striscia primitiva)
• Agonista della segnalazione Wnt canonica CHIR99021• Conc.elevate di
BMP4/ATTIVINA a
STRISCIAPRIMITIV
A
I FASE

Analisi di classificazione delle cellule attivate da fluorescenza mostra più del 90 % di cellule GFP -MIXL1+ indotte con alte conc. di BMP4 su basse conc. di attivina A e con alte conc. di CHIR99021.
Livelli di espressione comparativa relativi a SOX17, Brachiury T, e MIXL1 al 3 gg per
proporzioni di BMP4/Attivina A e CHIR99021

II FASE
LPM STRISCIA PRIMITIVA MESODERMA
PM
IM
La prima struttura a formarsi è il dotto nefrico lungo il quale appaiono tre paia di organi escretori: PRONEFRO, MESONEFRO, METANEFRO.
MM GERMOGLIO URETERICO EU
FGF9 GDNFWnt
NEFRONE
FGF FGF9

Co-localizzazione di PAX2 e LHX1
• INDUZIONE BMP/ATTIVINA A • AGONISTA Wnt CHIR99021 +FGF9

MIXL1, LHX1 SPOSR1, PAX2, LHX1 IMSIX2, WT1, GDNF, HOXD11 MMPAX2, CRET, HOXB7 EU
BMP4/ Attivina A + FGF9 + RA + BMP7
Inducono espressione transiente SIX2 e nessuna prova mesenchimale di PAX2.

Agonista della segnalazione canonica Wnt (CHIR99021) e FGF9 inducono espressione
prolungata SIX2 nel MM , espressione PAX2 nel MM e nell’EU.
MIXL1, LHX1 SPOSR1, PAX2, LHX1 IMSIX2, WT1, GDNF, HOXD11 MMGATA3 co-espresso con EU PAX2+

JAG1 CDH6
Prove per l’induzione del nefrone dopo differenziazione CHIR99021 + FGF9 diretta.
Primi nefroni/ vescicole renali

Integrazione ed auto-organizzazione di cellule derivate da hESC indotte con protocollo
CHIR99021 e FGF9.
ECAD⁺, PAX2, AQP2 EUAQP1, SLC3A1, WT1, PAX2⁺ TP circondava l’EU (ECAD ⁺)JAG1 ⁺, ECAD⁺ vescicole renali

Lo studio dei ricercatori M. Takasato, H. Little et al., mostra per la prima volta l’utilizzo di FGF9, dimostratosi cruciale per la sopravvivenza e lo sviluppo in continuo del MM.
La creazione di un rene tramite l’uso di cellule staminali rende risolutivi (ed in ogni caso limitativi) i problemi connessi ai trapianti d’organo.
RIGETTO D’ORGANO LISTE D’ATTESA
DURATA LIMITATAUSO DI IMMUNOSOPRESSIVI MANCANZA D’ORGANI