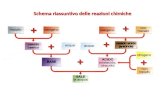
IL BILANCIAMENTO DELLE REAZIONI (EQUAZIONI) CHIMICHE
20
IL BILANCIAMENTO DELLE REAZIONI (EQUAZIONI) CHIMICHE
Transcript of IL BILANCIAMENTO DELLE REAZIONI (EQUAZIONI) CHIMICHE
I composti che in acqua dissociano in IONI si chiamano ELETTROLITI:
Elettroliti FORTI: completamente dissociati a = 1
Elettroliti DEBOLI: parzialmente dissociati 0 < a < 1
Non elettroliti: indissociati a = 0
GLI ELETTROLITI
LE REAZIONI DI OSSIDORIDUZIONE (REDOX)
Zn(s) + H+(aq) Zn2+
(aq) + H2(g)
La semireazione di ossidazione
Zn(s) Zn2+(aq) + 2 e-
La semireazione di riduzione
2 H+(aq) + 2 e- H2(g)
La reazione redox
Zn(s) + 2 H+(aq) Zn2+
(aq) + H2(g)
La reazione redox bilanciata