Ghiandole surrenali
-
Upload
dario -
Category
Health & Medicine
-
view
4.211 -
download
1
Transcript of Ghiandole surrenali
1
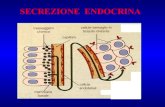
Le ghiandole surrenali
Le ghiandole surrenali
• I surreni sono localizzati al disopra deireni.
• Si tratta di complesse ghiandoleendocrine che svolgono funzionimultiple e sono essenziali per la vita.
• Sono altamente vascolarizzati, con unnotevole flusso ematico/grammo ditessuto
• Sono composti da due aree, lacorticale e la midollare, chedifferiscono dal punto di vistaembriologico e anatomo-funzionale
Corticale del surrene
Struttura e funzione
Zona Glomerulosa
Mineralcorticoidi - Aldosterone
Zona Fasciculata
Glucocorticoidi - Cortisolo
Zona Reticularis - Androgeni
Midollare – Adrenalina Noradrenalina
[K+] AII
ACTH
StimoliSistemasimpatico
Corticale 80%
Midollare 20%
Ormoni prodotti dai surreni
• Mineralocorticoidi (aldosterone)– Controllo del bilancio di Na+ e K+.
• Androgeni (DHEA, DHEA-S,androstenedione)– Caratteri sessuali secondari
• Catecholamine (adrenalina,noradrenalina, dopamina)
Steroidogenesi
• Gli ormoni steroidei sono tutti sintetizzati a partire dalcolesterolo.– Il colesterolo deriva dal circolo sanguigno ed é prodotto nei
surreni dall’acetil-CoA
– Ognuna delle tappe della biosintesi degli ormoni steroidei écontrollata da uno specifico enzima. Alterazioni negli enzimipossono essere causa di significative variazioni nellaproduzione ormonale.
• La reazione limitante é la conversione del colesteroloa pregnenolone
• Avviene nel mitocondrio ad opera degli enzimi delcomplesso citocromo P450
2
Biosintesi degli ormoni steroidei
Colesterolo
Deidroandrostenedione Androstenedione Estrano
Androstenediolo Testosterone Estradiolo
Pregnenolone Progesterone 11-deossi-corticosterone Corticosterone
17OH-Pregnenolone 17OH-Progesterone 11-deossicortisolo Cortisolo
Aldosterone
SSC enzyme
17 idrossilasi
17,20 desmolasi
17KS reduttasi
3b-idrossisteroidodeidrogenasi
Aromatasi
21 idrossilasi
11 idrossilasi
18 idrossilasi
Steroidogenesi
• Gli ormoni steroidei sono in genere secretiappena sintetizzati piuttosto che essereaccumulati nelle cellule
• Le situazioni di iperproduzione sono ingenere associate ad iperplasia piuttosto che aipertrofia cellulare
• Gli ormoni steroidei sono veicolati da proteineplasmatiche che ne prolungano l’emivita
Trasporto degli ormoni surrenalici
Corticosteroid-BindingGlobulin (CBG)
• Proteina prodotta dalfegato
• Elevata affinità mabassa capacità percortisolo
• Legame anche conalbumina
• 90% cortisolo legato,3-10% libero
Sex-Hormone BindingGlobulin (SHBG)
• Lega gli androgeni• Modesto legame con
albumina• Affinità: DHT > Testo >
Androstenediolo >estradiolo > estrone >androstenedione
Meccanismo di azione degli ormoni steroidei
Controllo a feedback sulla sintesi di cortisolo
Ipotalamo
Ipofisi
Surreni
Cortisolo
Stimoli• Stress• Infezioni
CRH
ACTH
(-)
(-)
Ritmo circadiano nella produzione di cortisolo
3
Ormoni prodotti dai surreniFunzioni dei glucocorticoidi (Cortisolo)
• Regolazione del metabolismo energetico– Carboidrati– Grassi– Proteine
• Resistenza allostress
• Anti-infiammatori
↓ Glucose Utilization
↓ Insulin Sensitivity
↑ Lipolysis
↓ ProteinSynthesis
↑ ProteinDegradation
↓ InsulinSensitivity
↓ GlucoseUtilization
↑ Glycogen Storage
↑ Gluconeogenesis
↓ Insulin Sensitivity
↑ Amino Acids
↑ Glucose
↑ FFA & Glycerol
Muscle
Liver
Adipose Tissue
=Anti Insulin Effects
Regolazione dell’aldosterone
• Renina:–stimola aldosterone attarverso il
pattern dell’angiotensina (principaleregolatore)
• Elevato K+:–stimola aldosterone
• ACTH:–stimola, ma non rappresenta il
principale regolatore (pazienti conipopit. hanno normali livelli e funzionedell’aldosterone)
Controllo dulla sintesi di aldosterone
Cellule J-G
Angiotensina I
Tessuti bersaglio(reni)
Aldosterone
Stimoli• Ipotensione• Ipovolemia
Renina
(-)
Surreni
Angiotensinogeno
Angiotensina II
Enzima diconversione
Azioni dell’aldosterone
• Aumento del riassorbimento di sodio daparte del tubulo contorto distale
• Azioni secondarie– Costrizione della muscolatura liscia vasale– Rilascio di noradrenalina dai nervi del
Sistema Nervoso Simpatico– Rilascio di adrenalina dalla midollare del
surrene– Rilascio di vasopressina
Diagnostica della corticale del surreneEsami di laboratorio: Test basali
• Determinazione del cortisolo basale– h 8:00, 16:00, 24:00
• Determinazione del CLU• Cortisolo salivare• Determinazione degli androgeni plasmatici
– DHEA, DHEA-S, Testosterone totale e libero
• Determinazione degli altri steroidi surrenalici– Pregnenolone, 17a-pregnenolone, progesterone,
17OH-progesterone, DOC
• Determinazione dell’ACTH• Determinazione degli auto-anticorpi
Diagnostica della corticale del surreneEsami di laboratorio: Test dinamici
• Test di soppressione con desametasone
• Test di stimolo con ACTH
4
Diagnostica della corticale del surreneDiagnostica per immagini e strumentale
• TC• RMN• Scintigrafia con 131I-
iodiometilnorcolesterolo• Ecografia surrenalica
• RMN ipofisaria• Cateterismo dei seni petrosi
Malattie del corticosurrene
Ipocorticosurrenalismi
Ipocorticosurrenalismo
• Definizione: insufficiente produzionesurrenale e/o insufficienze presenza,a livello dei tessuti periferici, diormoni corticosurrenalici
• Differenziazione in forme acute eforme croniche
Insufficienza corticosurrenalica acutaSegni e sintomi
Ipocorticosurrenalismo:classificazione
• Primario– Forme organiche
• Autoimmune• Infettivo• Emorragico• Infiltrativo• Invasivo
– Forme iatrogene• Post-chirurgico• Terapia con inibitori enzimatici• Terapia con agenti citotossici
– Forme congenite• Difetti della steroidogenesi surrenalica• Deficit familiare di glucocorticoidi• Ipoplasia surrenalica congenita• Adrenoleucodistrofia
• Secondario– Forme organiche
• Malattia ipotalamo-ipofisaria
• Inibizione asse IIS doporimozione tumorisecernenti glucocorticoidi
– Forme iatrogene• Terapia steroidea
• Resistenza aiglucocorticoidi
5
Insufficienza corticosurrenalica primaria(Morbo di Addison)
• Definzione: ipocorticosurrenalismo dadistruzione della corteccia surrenalica
• Epidemiologia: 40-60 casi/milione di abitanti,massima incidenza 30-40 anni.Se autoimmune F/M = 2.5/1Se post-TBC M/F = 1.25/1
• Eziopatogenesi: 80-90% Autoimmune10-20% TBC~ 1% Altre
Eziopatogenesi del morbo di Addison
• Forme autoimmuni: Spesso parte delle sindromi poliendocrineautoimmuni– PAS I: almeno due tra ipoparatiroidismo, m. di Addison,
candidosi mucocutanea– PAS II: m. di Addison, tireopatia autoimmune e/o diabete tipo 1
(± ipogonadismo, anemia perniciosa, vitiligine, miastenai gravis,morbo celiaco)
– PAS III: tireopatia autoimmune e una o più tra gastrite atrofica,anemia perniciosa, diabete tipo 1, vitiligine, alopecia
• Malattie infettive:– TBC (necrosi caseosa dei surreni)– Infezioni da funghi– AIDS
• Malattie ivasivo-infiltrative: metastasi, amiloidosi,emocromatosi, sarcoidosi
• Da vasculopatie: emorragia bilaterale– Bambini: setticemia da meningococco o pseudomonas– Adulti: terapia con anticoagulanti
• Cause erediatrie
Segni del morbo di Addison
Segni % pazientiIperpigmentazione 91Ipotensione 81Iponatriemia 67Ipercalemia 55Anticorpi anti-surrene 52Cartilagini auricolari calcifiche 12Ipoglicemia 19Eosinofilia 17
Sintomi del morbo di Addison
Sintomi % pazientiDebolezza/affaticabilitá 94Calo ponderale 90Anoressia 86Nausea, vomito 66Disturbi GI vaghi 61Dolore addominale 28Dolore muscolare 16Letargia 12
Deficit di ACTH
• ACTH inappropriatamente basso• Cortisolo basso• Normali livelli di Renina, Aldosterone, e K• Tendenza a basse [Na] a causa della
ritenzione idrica dovuta agli effetti dellebasse concentrazioni di cortisolo sui reni,e al lieve aumento dei livelli di ADH
6
Insufficenza corticosurrenale:primaria vs. secondaria
• I pazienti con ipocorticosurrenalismo primitivopresentano aumento dei livelli circolanti di ACTH(causa di iperpigmentazione) e basso aldosterone(causa di iperkalemia, riduzone del volumeplasmatico e aumento della renina)
• I pazienti con ipocorticosurrenalismo secondario(ridotto ACTH) possono avere ipotensione oiponatriemia, ma normale volume extracellulare enormale [K]
Ipercorticosurrenalismi
Ipercorticosurrenalismo
• Definizione: Quadro clinico causato da eccesso diglucocorticoidi e caratterizzato da obesitá, pletorafacciale, ipertensione arteriosa, osteoporosi,intolleranza al glucosio, irsutismo e/ooligomenorrea
• Differenziazione in sindrome di Cushing(ipercortisolismo indipendentemente dalla causa)e malattia di Cushing (ipercortisolismo daipersecrezione di ACTH)
Epidemiologia dellasindrome di Cushing
20-408/110/20 ogni1000000/anno
Malattia di Cushing
40-602/1 - Carcinoma surrenale
40-603/1 - Adenoma surrenale
40-601/3 - S. da ACTH ectopico
300-350 ogni1000000/anno
Sindrome di Cushing
Età(anni)
RapportoF/M
Incidenza
Segni e sintomi nellaSindrome di Cushing (%)
• Obesitá centrale 79-97• Pletora facciale 50-94• Intoll. glucosio 39-90• Miopatia prossimale 29-90• Ipertensione 74-87• Problemi pschiatrici 31-86• Faciltá bruciature 23-84• Irsutismo 64-81
• Problemi mestruali 55-80• Impotenza 55-80• Acne, cute grassa 26-80• Strie addominali 51-71• Edemi 28-60• Problemi ossei,
fratture vertebrali 40-50• Polidipsia/poliuria 25-44
Indiagini per la diagnosidella sindrome di Cushing
• Diagnosi di ipercortisolismo– CLU– Test di soppressione con basse dosi DMX– Ritmo circadiano di cortisolemia
• Diagnosi eziologica• ACTH plasmatico• Test di soppressione con alte dosi di DMX• Test di stimolo con CRH• Localizzazione
– TC o RMN• Addome• Sella turcica• Torace
• Cateterismo dei seni petrosi
7
Possibili sedi di produzione diACTH ectopico
• Carcinoidi bronchiali• Carcinoidi del timo• Microcitoma polmonare• Ca midollare della tiroide• Feocromocitoma• Adenocarcinoma• Vari e sconosciuti
Terapia dellasindrome di Cushing
ConvenzionaleChemioterapiaSpesso palliativaS. Da ACTH ectopico
-MitoatneSurrenectomiabilaterale
Carcinoma surrenale
--Surrenectomiamono o bilaterale
Adenoma surrenale
ConvenzionaleCon particellepesanti
CiproeptadinaBromocriptinaKetoconazolo
Ipofisectomiatransfenoidale
Malattia di Cushing
RadianteMedicaChirurgica
Iperaldosteronismo
Iperaldosteronismo
• Epidemiologia:– Primo caso riportato nel 1954– Prevalenza: 0.05-14.4%
dei soggetti con ipertensione– Recentemente, aumento
della diagnosi delle formesecondarie legate a problemidi vascolarizzazione renale
Sindrome caratterizzata da ipertensione, ipokalemia ealcalosi metabolica per aumento dell’aldosterone
IperaldosteronismoQuadro clinico
• Ipertensione arteriosa di grado variabile• Ipokaliemia (fino al 50-70% [K] normale)
• Ipervolemia con assenza di edemi• Alcalosi metabolica
IperaldosteronismoQuadro clinico: effetti secondari
• Conseguenze dell’ipertensione– Cefalea– Retinopatia (rara)
• Conseguenze dell’ipokalemia– Astenia muscolare, facile stancabilità– Sintomi neuromuscolari (crampi, parestesie, lcalosi ipokaliemica
(tetania)– Diabete insipido nefrogeno (poliuria da danno tubulare)– Aritmie cardiache (alterazioni onda T, comparsa onda U)
• Conseguenze dell’azione dell’aldosterone sul cuore– Ipetrofia cardiaca, fibrosi– Ipetrofia della muscolatura liscia vasale
8
IperaldosteronismoClassificazione
• Iperaldosteronismo primario– Secrezione autonoma di aldosterone
da parte del surrene con inibizionedella PRA
– Aumento del rapporto PA/PRA• Iperaldosteronismo secondario
– Iperaldosteronismo associato ad elevatilivelli di PRA
Eccesso di mineralcorticoidicon bassa PRA
• Iperaldosteronismo primitivo– Adenoma producente aldosterone– Iperplasia surrenalica bilaterale idiopatica– Iperplasia surrenalica unilaterale– Iperaldosteronismo sopprimibile con glucocorticoidi (forma
familiare tipo I)– Carcinoma producente aldosterone
• Iperplasia surrenalica congenita da deficit di 11β-idrossilasi o 17α-idrossilasi
• Apparente eccesso di mineralcorticoidi (AME)• Sindrome di Liddle
Cause di iperaldosteronismo primitivo
RaraAssociazione a MEN I(F. familiare II)
RaroSecrezione ectopica di aldosterone
1-3%Iperaldosteronismo sopprimibile con glucocorticoidi(F. familiare I)
30-40%Iperaldosteronismo idiopatico(iperplasia bilaterale semplice, micro o macronodulare)
65%Adenoma aldosterone-secernente(raramente carcinoma)
Neoplasie surrenaliche
• Causa più frequente diiperaldosteronismo primitivo(65%)
• In genere benigne e di modestedimensioni (<2 cm)
• Se maligne, spesso dimensioni >4 cm
• F > M• FNAB non sufficiente a
differenziare adenoma dacarcinoma
Iperplasia surrenalicamono o bilaterale, macro o micronodulare
• Patogenesi:– In genere idiopatica– Possibile ruolo di una maggiore sensibilità
all’angiotensina II– Mutazioni del gene aldosterone sintetasi
• Forme unilaterali differenziate sulla basedel cateterismo
GLOMERULOSA FASCICOLATA
Iperaldosteronismo familiare di tipo Isopprimibile con desametasone
Patogenesi
9
Aldosterone sintetasi11-β-idrossilasi
Formazione chimera di un gene chimericoCromosoma 8
Chimera dellaAldosterone Sintetasi
Formazione chimera aldosterone sintetasi
Aldosterone sintetasiPromotore11-β-idrossilasi
Sindrome da apparente eccessodi mineralcortcoidi (AME)
• Uso di farmaci o sostanze esogene adattività mineralcorticoide– acido glicirrizico (liquirizia)– Carbenoxolone, fluoroidrocortisone, spray nasali o creme
dermatologiche contenenti sostanze con attivitàmineralcorticoide
• Deficit di 11β-HSD2(mutazione del gene che codifica l’enzima)
Iperaldosteronismo secondario
• Patologia che si caratterizza per l’iper-secrezione di aldosterone inconseguenza di un aumento dei livelli direnina
• Più frequenti patologie secondarie amalattie (renali)
Iperaldosteronismo secondarioClassificazione
• Senza ipertensione arteriosa– scompenso cardiaco– sindrome nefrosica– cirrosi epatica– tubulopatie renali– diarrea e vomito– abuso di diuretici e/o lassativi– sindrome di Gitelman– sindrome di Bartter
• Con ipertensione arteriosa– ipertensione nefrovascolare– ipertensione maligna– trattamento estrogenico– reninoma
IperaldosteronismoDiagnosi
• Iperaldosteronismo primitivo– Sospettare nei pazienti con ipertensione ed
ipokalemia– Sospettare in presenza di masse surrenaliche
• Iperaldosteronismo secondario– Sospettare in pazienti con progressivo
peggioramento di ipertensione– Sospettare in donne < 35 anni con ipertensione– Sospettare in presenza di patologie associate
10
IperaldosteronismoIndagare i soggetti con:
• Ipopotassiemia (senza causaapparente)
• Incidentaloma srrenalico• Giovani (<50 anni)• Con familiarità per
ipertensione giovanile• Con ipertensione resistente
(> 2 farmaci)
• Escludere uso di sostanze ad azionemineralcorticoide– liquirizia, farmaci
• Sospendere farmaci interferenti (≥2settimane)– diuretici, β-bloccanti, ACE-inibitori,
inibitori recettore angiotesiona 2– Eventuale uso di Ca-antagonisti o α-
bloccanti• Normalizzare i livelli di Na e K
Approccio diagnostico nel sospetto diiperaldosteronismo primitivo
Premesse
Approccio diagnostico nel sospetto diiperaldosteronismo primitivo
Test di screening (PA/PRA)
Test di localizzazione (TAC)
Test di conferma
Test di lateralizzazione
Mantero et Al., L’endocrinologo vol 6 n..4, 2005
• Dosaggio di aldosterone (PA) e attivitàreninica plasmatica (PRA) in clino e in orto.
• PA (ng/dl) /PRA (ng/ml/ora) in orostatismo:– < 25 normale;– > 25 suggestivo;– >50 diagnosi di iperaldosteronismo primario
Approccio diagnostico nel sospetto diiperaldosteronismo primitivo
Test di screening
Algoritmo diagnosticoin caso diipertensione ed ipokalemia (I)
PA/PRA
Ipertensione essenziale;Iperaldosteronismo secondario
Ipertensione arteriosaessenziale
Probabile iperaldosteronismoprimario
Iperaldosteronismoprimitivo confermato
Test di soppressione
>25 <25
Aldosterone soppresso
Aldosterone nonsoppresso
Test di soppressionecon infusione salina
• In soggetti normali, l’aumento della volemia determinariduzione dell’aldosterone.
• Non effettuare in pazienti con compromissione dellafunzione cardiaca
• 2-3 litri di NaCl 0.9% in 4-6 ore• Valutazione dell’aldosterone
– Risposta normale: PA < 6 ng/dl– Adenoma surrenalico: PA > 10 ng/dl– Valori sospetti: PA tra 6 e 10 ng/dl
11
Test di localizzazionenell’iperaldosteronismo primitivo
CT surrene
Iperaldosteronismo idiopaticoprimitivo
Probabile iperaldosteronismoprimario
Iperaldosteronismo primitivo confermato
Scintigrafia surrenalica con I131-colesterolo
Cateterismo venoso per dosaggi aldosterone
Risultati discordanti
positivo negativo
Mezzi per la diagnosi differenziale fra le diverseforme di iperaldosteronismo primario
TAC/RMN• Quando la valutazione per immagini evidenzia un solitario
macroadenoma (> 1 cm) con normale quadro contro laterale ladiagnosi di APA è fortemente probabile.
• Spesso indagine dubbia con modeste alterazioni di forma,microadenomi (< 1 cm) monolaterali o macronoduli bilaterali.
Mezzi per la diagnosi differenziale fra lediverse forme di iperaldosteronismo primario
• Scintigrafia surrenalica coniodocolesterolo
• Cateterismo seletivo dellevene surrenaliche
Diagnsi di iperaldosteronismosecondario
• Diagnosi da porre in presenza di:– Anomalie strutturali (identificazione di
significativa ostruzione dele arterie renali)– Anomalie funzionali (evidenza di
ipersecrezione di renina)
Trattamento dell’iperaldosteronismo
• Adenoma surrenalico singolo➥ Surrenectomia
• Carcinoma surrenalico➥ Surrenectomia + chemioterapia
• Iperplasia idiopatica➥ Antaldosteroici (spironolattone, canrenoato, eprenolone),
antiipertensivi
• Iperaldosteronismo glucocorticoide-sopprimibile➥Glucocorticoidi a basse dosi
• Iperaldosteronismo secondario➥Angioplastica
Iperplasia surrenale congenitao sindromi adreno-genitali
12
Iperplasia surrenalica congenita
• Aumento dei livelli di ACTH in conseguenza dellaridotta sintesi di cortisolo.
• Questo é causa– Iperplasia surrenalica,– Maggiore produzione di precursori degli steroidi,– Sintesi preferenziale di alcuni di questi, quali gli androgeni.
• Il quadro di virilizzazione si ha sia nel maschio chenella femmina
• Possibile deficit dei mineraloattivi con perdita di Saliin relazione alla sede del blocco
Iperplasia surrenale congenitaclassificazione
• Deficit della 21-idrossilasi (93-94%)– Forma classica: 1/10000– Forma non classiche: 1/1000
• Deficit 11β-idrossilasi (5%)• Deficit 3β-idrossisteroidodeidrogenasi (1%)• Deficit 17α-idrossilasi (rara)• Deficit 20,22 desomoalsi (rara)
Iperplasia surrenale congenita:eziopatogenesi
• Trasmissione come carattere autosomico-recessivo• Cause: delezioni, conversioni o mutazioni puntiformi
• 21-idrossilasi: cromosoma 6p (P450c21B)• 11β-idrossilasi: cromosoma 8p• 17α-idrossilasi: cromosoma 10q• 3β-idrossisteroidodeidrogenasi: cromosoma 1, 2 geni, uno
espresso nei tessuti periferici e placenta, il secondo insurreni e gonadi
• 20,22 desomoalsi: cromosoma 15, sospette mutazionidella proteina StAR
Deficit di 21-idrossilasi
• Rappresenta la forma più frequente di iperplasiasurrenalica congenita (93-94%), con un incidenza di1/10000 nella forma classica e 1/1000 nelle formenon-classiche
• Nelle femmine causa virilizzazione, nei maschipubertá precoce e bassa statura
• I pazienti con blocchi parziali possono avere unquadro clinico lieve e a sviluppo tardivo
• La diagnosi si basa sulla presenza di elevati livelli di17-OH progesterone (basale e dopo stimolo conACTH)
• Trattamento: cortisolo per inibire la secrezione diACTH
Biosintesi degli ormoni steroideiDeficit 21-idrossilasi
Colesterolo
DHEA-S Androstenedione Estrano
Androstenediolo Testosterone Estradiolo
Pregnenolone Progesterone 11-deossi-corticosterone Corticosterone
17OH-Pregnenolone 17OH-Progesterone 11-deossicortisolo Cortisolo
Aldosterone
21 idrossilasi
Nomogram relating baseline to ACTH-stimulated serum concentrations of 17-OHP
New, M. I. J Clin Endocrinol Metab 2006;91:4205-4214
13
Deficit di 21-idrossilasiMutazioni più frequenti nella popolazione italiana
1 2 3 4 5 6 7 8 9 10
P30L P453SI172N
a656gI236NV237EM239K
R356W
D8nt Q318X+1nt
34%
11%
0%
Carrera et al. Hum.Genet, 1996
10%V281L 58% (NC)
Sindromi adrenogenitaliQuadro clinico
Sindromi adrenogenitaliQuadro clinico forme non classiche
• Ipertensione– da aumento DOC in deficit di 11β-idrossilasi e
17α-idrossilasi• Acne irsutismo, raramente virilizzazione• Bassa statura• Infertilitá
Incidentalomi surrenalici
Incidentalomi
• Definizione: presenza di una massa surrenalica,clinicamente silente, identificata in caso diinterventi chirurgici o diagnostici per patologie noncorrelate con i surreni
• Epidemiologia: frequenza in aumento (maggioreuso indagini strumentali). 4% esami TC.Frequenza aumenta con l’età
• Eziopatogenesi: in genere adenomicorticosurrenalici silenti. Carcinomi nel 4,7% deicasi
Catecolamine eMidollare del surrene
14
Midollare del surrene• Estensione funzionale del
sistema nervoso
• Rilascia adrenalina enoradrenalina (catecolamine)
• Generalmente attivata inconcerto con l’attivazione delsistema simpatico.
• Determina rapidiaggiustamenti nelmetabolismo e nl sistemacardio-vascolare in risposta aparticolari circostanze: caldo,freddo, stress, ipoglicemia,ecc.
• Coinvolta in situazionipartcolari quali emorragie,shock, traumi, ecc.
Midollare del surrene
• La midollare è esposta aelevate concentrazioni diglucocorticoidi.
• La corticale agisce diconcerto con la midollare.
• La midollare è innervata dafibre colinergiche del midollosinale.
• La midollare può essereconsiderata un gangliosimpatico specializzato.
Controllo del rilascio delle catecolamine
• La sintesi viene attivata con il resto del sistemanervoso a ne amplifica gli effetti
– Traumi, dolore, ansia, nervosismo, ipovolemia,ipotensione, anossia, temperature estreme, eserciziofisico
• Rilasciate in circostanze di emergenza(“fight or flight”)
• L’ipoglicemia è un potente stimolo al rilascio.
Attivazione della via delle catecolamine
Ipotermia
Ipoglicemia
Ipovolemia
Traumi
Dolore
Ansia
Acetilcolina
Adrenalina
Nervi
SimpaticiAcetilcolina
Noradrenalina
GangliSimpaticiMidollare
Surrene
Effetti sulle cellulebersaglio locali
Effetti sulle cellulebersaglio a distanza
Ipotalamo
MidolloPonte
Midollo spinale
Esercizio Ipossia
Nervi
Simpatici
Risposta delle catecolamine all’ipoglicemia
Insulina
Metabolismo delle catecolamine
• Tutta l’adrenalina circolante viene prodotta dallamidollare del surrene.
• La noradrenalina in circolo deriva dalla midollaredel surrene e dalle terminazioni nervose delsistema simpatico.
• Adrenalina e noradrenalina in circolo sono attiveper 20-30”, quindi l’attività diminuisce nel giro dialcuni minuti (catabolismo prevalentementeepatico).
15
Eliminazione delle catecolamine
dopamina
noradrenalina
adrenalina
acido omovanillico
acido manilvandelico
catecol-O-metiltransferasi (COMT) monoamine ossidasi (MAO)
Azioni delle Catecolamine
Effetti delle catecolamine sul metabolismo
Stimolo alla produzione di glucosio.Riduzione utilizzo del glucosio.Riduzione secrezione insulina.Stimolo lipolisi e chetogenesi
Effetto globale – aumento glucosio, acidi grassi eketoacidosi nel plasma.
Aumento metabolismo basale e produzione di calore
Potenza: adrenalina > noradrenalina.
Effetti delle catecolamine sul sistema cardiovascolare
• Aumento frequenza cardiaca e contrattilità, maggioreoutput cardiaco, aumento PA.
• Costrizione dei vasi a livello renale, dell’apparato GI,delle mucose e della cute.
• Aumento flusso ematico a muscoli, cuore e cervello– Garantiscono un maggior subtrato energetico negli organi
implicati nella risposta alle situazioni di “fight or flight”
Effetti delle catecolamine sugli altri apparati
• Riduzione motilità stomaco ed intestino.• Rilasciamento muscolatura bronchiale.• Dilatazione pupille.• Orripilazione.• Aumentata secrezione di renina.• Aumentata tensione muscolare.• Aumentata sudorazione.• Aumentata aggregazione piastrinica.
“Fight or Flight Response”
• Definizione. Rappresenta la reazione globaledell’organismo alle situazioni di emergenza.L’attivazione dei sistemi utili nel combattere ("fight") opercepire il pericolo ("flight") è stimolata dal rilascio dicatecolamine con:– Aumento PA e frequenza cardiaca– Aumento del flusso ematico ai muscoli e riduzione ai visceri– Aumento metabolismo cellulare– Aumento consumo glucosio e FFA– Auemnto tensione muscolare– Aumento attività mentali– Dilatazione pupillare e orripilazione– Aumento coagulazione
• Nell’insieme permettono al soggetto di effettuare attività inmaniera più energica
16
Utilizzata per la prima voltanel 1895 da CesareLombroso.
Nel 1921 John Larsonperfezionò uno strumento inggrado di misurarecostantemente frequenzacardiaca, pressionearteriosa e frequenzarespiratoria.
Nel 1926 venne creatodaLeonarde Keeler ilpoligrafo.
La macchina della verità
Feocromocitoma
Tumori secernenti catecolamine
• Da sospettare in caso di:– Ipertensione labile, intermittente e refrattaria
al trattamento– Cefalea, sudorazioni e palpitazioni– Presenza di ipotensione posturale– Familiarità per MENII / VHL– Aumento paradosso della PA in seguito
all’assunzione di beta-bloccanti– “Coincidentaloma” surrenalico
Feocromocitoma
• 90% Sporadico• 90% Monolaterale (10% bilaterale)• 10% Sporadico bilaterale• Forma familiare: 50% bilaterale• Raro nel’infanzia• nel 90% dei casi è di origine surrenale
(10% dei casi extra-surrenalico)
tumore delle cellule cromaffini caratterizzato da:• ipertensione arteriosa,• aumento delle catecolamine sieriche e/o urinarie• alterazioni del metabolismo glicidico
• 0.1 - 0.5% dei casi• M = F• picco di incidenza tra
i 30 - 40 anni
Epidemiologia
Manifestazioni cliniche delfeocromocitoma
• Classica triade:• ipertensione con episodi
di cefalea• Sudorazione• palpitazioni
Altre manifestazioni difeocromocitoma
• Ipotensione ortostatica,• pallore,• edema della papilla,• calo ponderale,• poliuria e polidipsia
(infanzia)• cardiomiopatia,
• Pseudo-ostruzioniintestinali,
• infarto acuto delmiocardio,
• emorragie cerebrali,• gangrena delle dita,• disordini psichiatrici
17
Feocromocitoma:Regola delle H
• Hypertension [Ipertensione]• Hyperhydrosis [Ipersudorazione]• Hypomotility of gut [Ipomotilità intestinale]• Headache [Cefalea]• Hypermetabolism [Ipermetabolismo]• Hyperglycaemia [Iperglicemia]
Feocromocitoma:Regola del 10
• 10% familiare• 10 % bilaterale• 10% malignani• 10% extra-addominali• 10% multipli
Feocromocitoma:Regola del 10
• 10% familiare• 10 % bilaterale• 10% malignani• 10% extra-addominali• 10% multipli
Feocromocitoma familiare
• MEN II(solo il 33% sono sintomatici)
• Associati a malattia di Von Hippel Lindau(35% sintomatici)
• Neurofibromatosi(Incidenza del 0.6-5%)
• Casi familiari isolati
Feocromocitoma:Regola del 10
• 10% familiare• 10 % bilaterale• 10% malignani• 10% extra-addominali• 10% multipli
Feocromocitoma malignoE’ maligno quando sono presenti metastasi in organi che normalmente
non contengono cellule cromaffine.
• Ha un’incidenza rara e rappresenta il 10% di tutti i feocromocitomi• Diagnosi certa solo in caso di di invasione linfonodale o di metastasi
epatiche ed ossee
• Sintomi più frequenti sono:• ipertensione persistente o parossistica;• cefalea;• palpitazioni;• dolori addominali;• nausea;• vomito;• iperidrosi;• dolore toracico;• astenia;• tremori.
• A questa sintomatologia può associarsi quella dipendente dallalocalizzazione metastatica.
18
Localizzazioni secondarie delfeocromocitoma maligno
• Le localizzazioni metastatiche più frequenti sono:• osso 45%;• linfonodi e fegato 35%;• polmone 25%
• La terapia di prima scelta è l’asportazione chirurgica.• La terapia medica si distingue in pre-intraoperatoria e post-
operatoria.
Diagnosi biochimica
• Catecolamine nelle urine delle 24hr(95% sensibilità) (interferenza del labetalolo)
• Metanefrine nelle urine delle 24hr(90-95% sensibilità)
• Noradrenalina plasmatica>11.8 nmol/l = diagnostica>5.6 nmol/l = suggestiva
Diagnosi• catecolamine plasmatiche ⇒ > 1000 pg/mL• A urinaria ⇒ >25 mg/24h• NA urinaria ⇒ >150 mg/24h• acido vanilmandelico ⇒ >8 mg/24h• metanefrine ⇒ 300 mg/24h
Trattamento
• Resezione chirurgica