Elettroliti Lacqua non conduce la corrente elettrica (isolante). Soluzioni acquose di sali, composti...
-
Upload
bernardetta-testa -
Category
Documents
-
view
216 -
download
1
Transcript of Elettroliti Lacqua non conduce la corrente elettrica (isolante). Soluzioni acquose di sali, composti...

Elettroliti
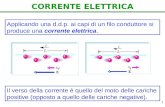
L’acqua non conduce la corrente elettrica (isolante). Soluzioni acquose di sali, composti costituiti da ioni, conducono la corrente elettrica.
Le sostanze, come i sali, che in soluzione acquosa esistono in forma ionica sono detti elettroliti.
Forti esclusivamente sotto forma di ioni ( sali come NaCl , K2CO3, etc.. e acidi forti o basi forti come HCl , HNO3 , NaOH )
Deboli parzialmente in forma ionica, parzialmente in forma di molecoleneutre ( acidi deboli o basi deboli come HF, CH3COOH , NH3 )
Non elettroliti esistono solo sotto forma di molecole neutre (glucosio)
!,0 M NaCl 1,0 M NaF
1,0 M KF 1,0 M KCl
=Na+ Cl-
K+ F-
Na+ Cl-
K+ F-
Le due soluzioni sono identiche
In entrambe le concentrazioni
di Na+ , Cl- , K+ , F-
sono identiche ( 1,0 M )


Unitàformula
Molecola del composto Unità formula ( NaCl ) del compostomolecolare metano, CH4 ionico Cloruro di Sodio
La molecola esiste come entità separata, mentre l’unità formula consiste in una coppia di ioni enucleata dal grande insieme ordinato di tutti gli ioni nel cristallo




Soluzione acquose di un sale ( Na+ Br- )
Na + Br -





Soluzioni di sali
• NaCl(s) → Na+(aq) + Cl -(aq)
• KNO3(s) → K+(aq) + NO3
-(aq)
• Na+ K+ Cl - NO3-
• KCl(s) → K+(aq) + Cl -(aq)
• NaNO3(s) → Na+(aq) + NO3
-(aq)

Equazioni ioniche nette
(a) Ad una soluzione limpida di nitrato di piombo in una beuta si aggiunge una soluzione limpida di ioduro di potassio.
(b) Si forma un precipitato giallo di ioduro di piombo. Gli ioni potassio e nitrato restano in soluzione
(a) (b)
Pb(NO3)2(aq) + 2 KI(aq) PbI2(s) + 2 KNO3(aq)
Pb2+ + 2 NO3- + 2 K+ + 2 I- PbI2 + 2 K+ + 2 NO3
-
Pb2+(aq) + 2 I-(aq) PbI2(s)