(Degenerazione idropica) -...
Transcript of (Degenerazione idropica) -...

(Degenerazione idropica)


Degenerazione idropica

• Degenerazione grassa (Steatosi)
– Fegato (principalmente)
• aumento di peso, colorito giallastro
• vacuoli nel citoplasma degli epatociti

Fegato e metabolismo dei lipidi e delle lipoproteine
-ruolo centrale nel metabolismo di lipidi /lipoproteine, omeostasi del
colesterolo
Caratteristiche dei lipidi
> insolubili in acqua.
> costituiti da acidi grassi insaturi o saturi a seconda della presenza o
meno di doppi legami fra atomi di carbonio adiacenti
Acidi grassi essenziali: Ac Arachidonico, linolenico e linoleico
Acidi grassi in forma libera: NEFA o FFA oppure Esterificata
(es. legati a glicerolo)
forma di deposito o di accumulo: trigliceridi o grassi neutri

Shorthand (line) formula for a typical example molecule of Fat Triglycerides in native fat or oil left part: glycerol right part from top to bottom: palmitic acid, oleic acid, alpha-linolenic acid chemical formula: C55H98O6

1) lipidi strutturali:
Fanno parte di tutte le membrane plasmatiche e intracellulari
(fosfolipidi, colesterolo, glicolipidi)
2) fonte di energia per il metabolismo intermedio di fegato, cuore e
tessuto muscolare:
(trigliceridi e a. grassi; 1g: circa 9 cal)
3) lipidi che prendono origine dal nucleo steroideo:
-colesterolo (presente nel sangue sia in forma libera che di
estere)
-steroidi (ormoni steroidei surrenalici, ovarici e testicolari)
4) A. grassi essenziali (acido arachidonico in particolare) precursori
di sostanze chiave modulatrici delle risposte infiammatorie (es.
prostaglandine e leucotrieni)
Ruolo principale dei lipidi


Le “gocce” visibili sono immagini negative dei grassi che sono allontanati dai
solventi impiegati nel processo di inclusione in paraffina (preparati istologici di
routine).
Per conservare i grassi e poterli evidenziare con coloranti specifici (oil red,
sudan III) occorre allestire il preparato usando il congelamento al posto della
inclusione e appositi microtomi (criostato)


Steatosi epatica Aumentato ingresso di
acidi grassi negli
epatociti (provenienti
dalla dieta o dai depositi, diabete, obesità )
Aumentata sintesi di trigliceridi da
parte degli epatociti (etanolo)
Diminuita ossidazione di acidi
grassi negli epatociti (ipossia
ipossica, anemica, stagnante, istotossica)
Diminuita secrezione di trigliceridi, sotto
forma di VLDL, da parte degli epatociti (digiuno prolungato, kwashorkor, sostanze inibenti la sintesi proteica, variazioni qualitative dei lipidi di membrana, CCl4, alterazioni funzionali del citoscheletro)
STEATOSI =
Accumulo negli epatociti di TRIGLICERIDI (glicerolo + 3 catene di acidi grassi) perché si instaura uno squilibrio fra
quantità presente e capacità di smaltimento

Core idrofobico, coperto da un singolo
strato di molecole anfipatiche (fosfolipidi,
colesterolo, apoproteine)
Lipidi presenti nel plasma (come lipoproteine) Colesterolo
Esteri del colesterolo
Trigliceridi
Fosfolipidi
Classificazione delle lipoproteine Chilomicroni
LDL: low density lipoprotein
VLDL: very low density lipoprotein
HDL: high density lipoprotein


Apoproteine:
sintetizzate nel RER
Componenti delle
lipoproteine:
assemblati nel SER
Lipoproteine:
rimaneggiate nel
Golgi e racchiuse
in vescicole
Lipoproteine impacchettate
spedite
alla membrana
Lipoproteine: secrete nel
sinusoide
sinusoide
VLDL
nascenti Vescicole
secretorie
GOLGI SER RER
NUCLEO
apoproteine
lipidi
carboidrati

(trascrizione)

Metabolismo dell’etanolo
CYP2E1: CYtochrome p450, famiglia 2, sottogruppo E1 MEOS:sistema microsomiale di ossidazione dell’etanolo ADH: alcohol dehydrogenase; ALDH: aldeide deidrogenasi
fegato
(MEOS)
mucosa
gastrica
e fegato
fegato



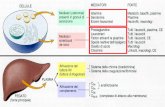
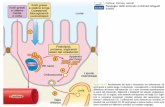
Tutti gli enzimi dei lisosomi sono idrolasi acide, attive al pH acido dei lisosomi (circa 5.0) ,ma non al pH neutro del citoplasma (7,2). Questo meccanismo protegge la cellula dalla eventuale rottura della membrana del lisosoma. Infatti le idrolasi rilasciate sarebbero inattive al pH neutro del citosol
IDROLASI ACIDE:
Nucleasi Proteasi Glicosidasi Lipasi Fosfatasi Solfolipasi Fosfolipasi

ATP ADP
pH 7
pH 5
H+
LISOSOMA
CITOSOL
Per mantenere acido il ph al loro interno i lisosomi devono attivamente concentrare ioni H+. Ciò è assicurato dalla presenza nella membrana di una pompa protonica, che trasporta attivamente protoni dal citosol nei lisosomi. L’attività di questa pompa richiede consumo di energia che è fornita da idrolisi di ATP per mantenere nei lisosomi una concentrazione di H+ circa 100 volte più alta rispetto al citosol
H+
Idrolasi acide

La Patologia lisosomiale -responsabile di alterazioni cellulari-
può estrinsecarsi funzionalmente con:
1) Attività litica dannosa
liberazione intracellulare di idrolasi (es. silicosi)
aumento patologico dei processi autofagici (es. digiuno)
rilascio extracellulare di enzimi lisosomiali (es. alteraz.fagocitosi)
2) Attività litica inadeguata
incapacità digestive nei confronti di alcuni microorganismi
substrati: inerti-anomali-eccessivi
stati di congestione/ingombro
enzimi: poco attivi-inibiti-deficienti*
* per carenza primaria genetica--> tesaurismosi lisosomiali

A • Inibizione degli enzimi digestivi lisosomiali
B • Incongruità di substrati inerti o poco digeribili
C
• Eccesso di materiale rispetto alle capacità digestive della cellula
Accumulo intracellulare di materiale indigesto si può avere in soggetti normali per insufficienze lisosomiali che possono originare:

Numerosi antibiotici, fra cui la streptomicina e la kanamicina,
inibiscono gli enzimi lisosomiali provocando accumulo di materiale
autofagico non digerito, responsabile di fenomeni di
organotossicità. Il farmaco più tipicamente lisosomotropo è
l’antimalarico clorochina, che provoca tesaurismosi lipidiche o
proteolipidiche in numerosi organi. Questo fatto va tenuto
presente poiché oggi la clorochina viene proposta come farmaco
attivo contro il virus HIV.

Substrati normali, specialmente lipidi, vengono resi
difficilmente digeribili per azione di farmaci anfipatici (ne
troviamo tra psicofarmaci e anti-anginosi usati in terapia),
che si accumulano nei lisosomi sotto forma di complessi
farmaco-lipidi; questi complessi si dissociano lentamente
solo dopo cessazione del trattamento, rilasciando così il
substrato che può finalmente essere digerito





Il ferro e’ indispensabile per: - la respirazione
• Sangue: come gruppo prostetico dell’emoglobina che lega
l’ossigeno
• Cellula: come trasportatore di elettroni secondo la reazione:
2Fe+++ + 2e- 2 Fe++
2Fe+++ + 2e- + O2 O2-- + 2H+ H2O
- la proliferazione cellulare
• componente essenziale della ribonucleotide riduttasi, enzima chiave
della sintesi del DNA.
• duplicazione mitocondriale (citocromi e proteine Fe/S)

DISTRIBUZIONE DEL FERRO NELL’ORGANISMO
POOL FUNZIONALE
POOL DI TRASPORTO
POOL DI DEPOSITO
Emoglobina 2600 mg
Mioglobina 200 mg
Citocromi
eme-enzimi 200 mg
pool labile
3 mg
1000 mg

La quantità di ferro assorbito dipende da diversi fattori:
• Quantità di ferro presente negli alimenti
• Forma chimica del ferro alimentare
• (Fe ++ o Fe +++)
• Meccanismo di regolazione a “feedback” esercitato dal pool di ferro presente nell’organismo




APOFERRITINA (“guscio” proteico di 24 subunità)
FERRITINA (Fe-APOFERRITINA)
•Ogni molecola di Ferritina ingloba al suo interno circa 4500 atomi di Fe+++ (in forma cristallina SIDERITE)

FERRITINA
•Presente nelle cellule del Sistema Reticolo Endoteliale (macrofagi) soprattutto milza, midollo, fegato (nel fegato anche negli epatociti) TOTALE FERRO DI DEPOSITO CIRCA 1000 MG •Se il Fe è presente in concentrazioni molto elevate la Ferritina polimerizza formando granuli insolubili di EMOSIDERINA nella quale la •apoferritina è parzialmente degradata


FERRITINA
NORMALMENTE LA FERRITINA E’ UN INDICATORE
FEDELE DEI DEPOSITI DI FERRO
1 g/L di FERRITINA 8 mg (o 120g/Kg)
di FERRO DI DEPOSITO Es: 100g/l =
800 mg deposito

Sovraccarico di ferro può essere dovuto a varie
cause:
cause generali, es.
-maggiore assorbimento intestinale (dieta ricca di ferro
e/o alterazioni dell’assorbimento
-trasfusioni ripetute (ad es. in soggetti con anemie su
base ereditaria come le talassemie)
cause locali, es.
emorragia all’interno di un tessuto

A Prussian blue reaction is seen in this iron stain of the liver to demonstrate large amounts of
hemosiderin that are present within the cytoplasm of the hepatocytes and Kupffer cells.
Ordinarily, only a small amount of hemosiderin would be present in the fixed macrophage-like
cells in liver, the Kupffer cells, as part of iron recycling.
emosiderina

These renal tubules contain large amounts of hemosiderin, as demonstrated by the Prussian
blue iron stain. This patient had chronic hematuria.
emosiderina


L’eccesso di ferro e’ tossico perché può portare alla formazione di radicali liberi
Il meccanismo della reazione è uguale a quello
della catena respiratoria, ma con una riduzione solo parziale dell’ O2
Fe++ Fe+++ + e- + O2 O2°-
porta alla formazione di anione superossido
(O2°-) che è il capostipite di tutta una serie di radicali
liberi


Colorazione gialla della cute, delle sclere e di altri tessuti, causata da un
eccesso di bilirubina in circolo.
Comincia a manifestarsi quando la bilirubinemia supera 2-2.5 mg per 100 ml. La bilirubina può essere coniugata (b. diretta) o non coniugata (b. indiretta) Si distinguono itteri pre-epatici (es. i. emolitici), epatici (es. i. da danno epatocellulare) e post-epatici (i. ostruttivi) Alcuni itteri dipendono da cause genetiche
N.B. l’aggettivo “diretta” o “indiretta” si riferiscono alla determinazione laboratoristica
Della concentrazione di bilirubina nel sangue


(ITTERO NUCLEARE)
Chandrasoma Taylor, Concise Pathology

Patogenesi dell’ittero nucleare
• 1) emolisi marcata, ad es. per incompatibilità materno-fetale per il sistema Rh
• 2) aumento di bilirubina non coniugata
• 3) insufficiente coniugazione della bilirubina per immaturità del fegato del neonato
• 4) insufficiente produzione di albumina da parte del fegato del neonato
• 5) insufficiente sviluppo della “barriera ematoencefalica” nel neonato
passaggio della bilirubina non coniugata e libera (non legata all’albumina) attraverso la barriera ematoencefalica con produzione di danno neuronale nei nuclei della base cerebrale


The yellow-brown granular pigment seen in the hepatocytes here is lipochrome (lipofuscin) which
accumulates over time in cells (particularly liver and heart) as a result of "wear and tear" with aging.
It is of no major consequence, but illustrates the end result of the process of autophagocytosis in
which intracellular debris is sequestered and turned into these residual bodies of lipochrome within
the cell cytoplasm.