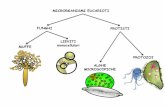
Controllo biologico dei microrganismi
Transcript of Controllo biologico dei microrganismi
Controllo biologico dei microrganismi:
sterilizzazione & disinfezione
Giovanni Di Bonaventura, PhD
CI «Microbiologia e Microbiologia Clinica»
CdS Medicina e Chirurgia
AA 2019-2020
Controllo dei microrganismi
«Dove» e «perché» è necessario
MICROBIOTA AMBIENTALE
Ambiente
MICROBIOTA
UMANO
Agricoltura
Industria
Zootecnia
Cibo, farmaceutici,
carburante, cosmetici
Animali, pollame,
(conservazione, produzione), etc
Sanitizzazione delle aree
Malattie (alberi, raccolto,
piante, etc)
Prevenzione di infezioni iatrogene,
infezioni chirurgiche, infezioni
crociate, diffusione di microrganismi
e geni associati ad antibiotico-R, etc
Controllo biologico
Tecniche
Il controllo biologico è finalizzato alla decontaminazione, ossia alla rimozione od alla inattivazione dei microrganismi mediante un trattamento che rende un oggetto od una superficie «sicuri», ossia tali da poter essere maneggiati o toccati senza rischio di contaminazioni.
Pulizia
Disinfezione
▪ metodi fisici
▪ metodi chimici
Sterilizzazione
▪ metodi fisici
▪ metodi chimici
▪ metodi chimico-fisici
DECONTAMINAZIONE
Il concetto di decontaminazione è relativo.
La tecnica per decontaminare viene scelta sulla
base della pericolosità e della concentrazione del
microrganismo.
Controllo biologico
Pulizia
PULIZIA = rimozione di materiale organico dal prodotto (strumentazione, attrezzature, etc.)
1. sciacquare l’oggetto con acqua fredda
2. applicare il detergente e rimuovere meccanicamente il materiale organico
3. risciacquare l’oggetto con acqua tiepida
4. asciugare l’oggetto (quindi disinfettare / sterilizzare)
Una corretta pulizia rende più efficace la decontaminazione (disinfezione/sterilizzazione). La materia organica, infatti, può proteggere i microrganismi dal trattamento:
▪ riducendo la penetrazione dell’agente (calore, sostanza chimica)
▪ neutralizzando l’agente (sostanza chimica)
Controllo biologico
Sterilizzazione vs Disinfezione
STERILIZZAZIONE = impiego di procedure chimiche, fisiche e/o chimico-fisiche per la eliminazione o
distruzione di qualsiasi forma di vita microbica, incluse le spore batteriche (forme di resistenza).
▪ Concetto assoluto, sebbene influenzato dalla capacità tecnica di rimuovere/distruggere i
microrganismi. Ad esempio, una soluzione filtrata non è tecnicamente sterile, poiché non in grado
di rimuovere la componente virale a causa delle esigue dimensioni.
DISINFEZIONE = processo che riduce il numero dei microrganismi patogeni a livelli di sicurezza per
l’uomo. Non è attiva nei confronti delle spore, ma soltanto sulle forme vegetative.
▪ Disinfezione: trattamento di superfici o sostanze inanimate (abiotiche)
▪ disinfettante: agente chimico in grado di uccidere microrganismi; dotato di diversi livelli di efficacia
▪ Antisepsi: applicazione topica a mucose, cute od altri tessuti
▪ antisettico: disinfettante usato su tessuti viventi
Are they dead or not ?
Definizioni
▪ Biocida: composto che uccide tutti i microrganismi viventi (patogeni e non-) incluse le spore
- battericida, fungicida, virucida, sporicida
▪ Biostatico: composto che impedisce la crescita dei microrganismi, non necessariamente uccidendoli
- batteriostatico, fungistatico, virustatico
▪ Sepsi: contaminazione microbica
▪ Antisepsi: procedura atta a prevenire una contaminazione (riduzione/inibizione microbica)
▪ Asepsi: assenza di contaminazione microbica
Sterilizzazione
da: Murray et al. Medical Microbiology 3rd ed., Mosby, 1998
La sterilizzazione di un prodotto può essere ottenuta mediante
l’impiego di tecniche:
▪ FISICHE
▪ CHIMICHE
▪ CHIMICO-FISICHE
Sterilizzazione - LAS
Quando il concetto di sterilità viene applicato su larga scala, nessuna tecnica dà assoluta certezza di
ottenere la sterilità ma ragionevole certezza.
Un materiale è infatti considerato sterile quando la probabilità di trovarvi un microrganismo è inferiore
ad uno su un milione.
In altri termini c’è la probabilità che sia sopravvissuto non più di un microrganismo vivente in 106 unità
sottoposte a sterilizzazione. Questo concetto è espresso in termini di LAS (livello di assicurazione di
sterilità).
Nelle attività farmaceutiche (preparazione di iniettabili, colliri e nella preparazione di materiali di
medicazione), un dato prodotto è considerato sterile quando la probabilità di trovare una unità non
sterile in un lotto sterilizzato sia di 10-6, quando cioè una unità su un milione può non essere sterile.
Sterilizzazione
Tecniche FISICHE
▪ Calore
▪ umido
▪ secco
▪ Filtrazione
▪ Onde elettromagnetiche
▪ radiazioni UV
▪ radiazioni ionizzanti
▪ Ultrasuoni
Sterilizzazione
Tecniche FISICHE - calore
▪ Sterilizzante maggiormente utilizzato in ambito ospedaliero: tecnica indicata per la maggior
parte dei materiali, eccetto i termosensibili, le sostanze chimiche tossiche o volatili
▪ Esistenza di una temperatura massima di crescita specie/ceppo-specifica
▪ L’effetto letale indotto dal calore consiste nella DENATURAZIONE (alterazione strutturale e
funzionale) delle macromolecole (proteine enzimatiche):
▪ ossidazione (calore secco)
▪ coagulazione (calore umido)
▪ Letalità = k x temperatura
Sterilizzazione
Sensibilità dei microrganismi al calore
Parametri che caratterizzano la termosensibilità di un microrganismo:
▪ Punto di inattivazione termica (Thermal Death Point, TDP):
la più bassa temperatura alla quale tutti i batteri in coltura liquida
vengono uccisi entro 10 minuti.
▪ Tempo di inattivazione termica (Thermal Death Time, TDT):
tempo richiesto per l’uccisione, ad una data temperatura, della totalità
dei batteri in coltura liquida.
▪ Tempo di riduzione decimale (Decimal Reduction Time, DRT):
tempo richiesto per l’uccisione, ad una data temperatura, del 90% della
popolazione batterica (utile soprattutto nell’industria alimentare).
Sterilizzazione
Sensibilità dei microrganismi al calore
Tempo di riduzione decimale (Decimal Reduction Time, DRT)riduzione pari
ad 1 log10
(http://www.ceaedizioni.it/pdf/13217anteprima.pdf)
Sterilizzazione
Tecniche FISICHE – calore umido: autoclave
▪ Autoclave: camera a pressione che utilizza vapore saturo (privo di aria) al quale si applica una pressione
per ottenere elevate temperature. L’aria può essere rimossa dalla camera per gravità o tramite prevuoto.
▪ Meccanismo di azione: coagulazione irreversibile e denaturazione delle proteine.
▪ Tecnica di sterilizzazione di uso più frequente: rapida, dotata di elevata capacità di penetrazione
(prodotti confezionati, lume di strumenti cavi), scarsamente influenzata dalla presenza di materiale
organico/inorganico.
▪ Impiego:
▪ adatta per: materiali termostabili e resistenti al vapore (es. attrezzatura per terapia respiratoria ed
anestesia), terreni di coltura, rifiuti infettivi, contenitori di oggetti pungenti/taglienti
▪ non adatta per: chimici tox e/o volatili, radioisotopi, agenti antineoplastici
Sterilizzazione
Tecniche FISICHE – calore umido: autoclave
Autoclave «gravity displacement»: struttura e funzionamento
All’interno della camera, l’aria può essere rimossa per:
▪ gravità: vapore immesso nella parta alta della camera;
poichè vapore più leggero dell’aria, questa viene rimossa
nel fondo della camera attraverso uno scarico. Utilizzata
primariamente per terreni di coltura, acqua, prodotti
farmaceutici, rifiuti medicali, oggetti non porosi (la cui
superficie entra a diretto contatto con il vapore); nel caso
di oggetti porosi, bisogna aumentare il tempo a causa
della incompleta eliminazione di aria.
▪ pre-vuoto: dotata di una pompa a vuoto (eiettore) che
garantisce la rimozione dell’aria dalla camera prima che il
vapore venga immesso. Il principale vantaggio consiste
nella istantanea penetrazione del vapore anche in oggetti
porosi o carichi che possano creare “sacche” d’aria.
Sterilizzazione
Tecniche FISICHE – calore umido: autoclave
Il ciclo di sterilizzazione «classico» di un trattamento in
autoclave prevede: 121°C, 15 min, 1 atm.
Tuttavia, il ciclo può essere personalizzato in base alla
tipologia di materiale, al «carico» (quantità di materiale in
autoclave) ed alla tecnica utilizzata (gravity vs dynamic).
Guideline for Disinfection and Sterilization in Healthcare Facilities (CDC, 2008)
Sterilizzazione
Tecniche FISICHE – calore umido: autoclave
Autoclave da banco
Autoclave da pavimento
Sterilizzazione
Tecniche FISICHE – calore umido: autoclave
La autoclave è generalmente dotata di un sistema di controllo real-time per la
temperatura, il tempo e la pressione.
Tuttavia, l’efficacia del ciclo di sterilizzazione viene monitorata mediante
indicatori chimici o biologici:
▪ indicatori chimici, vengono applicati alla superficie della confezione del
prodotto oppure si trovano integrate nella confezione stessa, per monitorare
la temperatura.
▪ indicatori biologici, sospensioni di spore di Geobacillus stearothermophilus
consentono di monitorare il raggiungimento dei 3 parametri.
Sterilizzazione
Tecniche FISICHE – calore secco
▪ Forno Pasteur, becco Bunsen, inceneritore
▪ Distruzione ossidativa delle proteine
▪ Tecnica non tossica per l’operatore e per l’ambiente
▪ Meno efficace del calore umido e richiede tempi e temperature maggiori (maggiore tempo
per trasferimento stessa quantità di calore da aria a prodotto vs quanto accade in autoclave)
▪ Utilizzabile per materiali termostabili, quelli danneggiati dal vapore (formazione di ruggine
e perdita del «filo» di taglio) o ad esso impermeabili:
▪ olii, polveri, oggetti taglienti, vetreria
▪ rifiuti infettivi (alternativa all’autoclave)
Sterilizzazione
Tecniche FISICHE – calore secco
Forno Pasteur, cicli di sterilizzazione:
▪ 180°C, 30 min
▪ 171°C, 60 min
▪ 160°C, 120 min
▪ 149°C, 150 min
▪ 141°C, 180 min
▪ 121°C, 12 h[processo meno efficace vs
autoclave: 121°C, 15 min]
Sterilizzazione
Tecniche FISICHE – filtrazione
Generalmente considerata una tecnica di sterilizzazione, la filtrazione è in realtà una tecnica
di decontaminazione in quanto:
▪ rimuove “meccanicamente” i microrganismi da soluzioni e gas (aria), non uccidendoli;
▪ non è in grado di rimuovere i microrganismi di piccolissime dimensioni (virus, micoplasmi)
Nella filtrazione si utilizzano filtri (nitrato od acetato di cellulosa) i cui pori hanno un
diametro (0.22 µm) inferiore alle dimensioni medie di gran parte dei microrganismi, eccetto
quelli di dimensioni assai ridotte (d<0.22 µm), quali virus e micoplasmi.
Utilizzata per prodotti termolabili che non possono essere sterilizzati in altro modo:
▪ terreni e supplementi (enzimi, siero, antibiotici) per crescita microbica e colture cellulari
▪ filtri HEPA (cabine biohazard, camere bianche o cleanroom) nel laboratorio biomedico,
nell’industria alimentare e farmaceutica (farmaci, vaccini)
▪ purificazione H2O
Sterilizzazione
Tecniche FISICHE – filtrazione di liquidi
Filtrazione di piccoli volumiFiltrazione di grandi volumi
filtrazione
Sterilizzazione
Tecniche FISICHE – filtrazione di gas
«High-efficiency particulate air» (HEPA) filter
Sterilizzazione
Tecniche FISICHE – onde elettromagnetiche
Tipologia di radiazioni utilizzata per il controllo dei microrganismi:
▪ Radiazioni IONIZZANTI (raggi γ, raggi X)
▪ Radiazioni NON IONIZZANTI (raggi UV)
Sterilizzazione
Tecniche FISICHE – onde elettromagnetiche
RADIAZIONI IONIZZANTI = radiazioni elettromagnetiche a corta λ (alta energia): raggi γ (Cobalto-60), raggi X,
elettroni (acceleratori elettronici).
Meccanismo di azione: effetto letale per azione ionizzante (dislocazione di e- da atomi) sulla molecola bersaglio:
▪ diretta: trasferimento di energia a biopolimeri (DNA, proteine), causandone la rottura
▪ indiretta: diffusione di radicali liberi (OH•, e-, H•), denaturanti il DNA
Applicazioni: i costi elevati ne limitano l’utilizzo a processi industriali (su «larga scala»):
▪ strumentazione (chirurgica) e dispositivi medicali monouso (aghi, siringhe, cateteri, guanti)
▪ industria farmaceutica: antibiotici, vaccini, pomate
▪ tessuti per trapianto (valvola cardiaca, tendine, pelle)
▪ rifiuti sanitari (fascio elettronico)
▪ industria alimentare: carne fresca (OMS) o carne tritata (FDA)
Svantaggi:
▪ costi elevati
▪ penetrano nei tessuti
▪ mutagene per l’uomo
Sterilizzazione
Tecniche FISICHE – onde elettromagnetiche
Sensibilità alle radiazioni di alcuni microrganismi e funzioni biologiche:
D10: quantità di radiazioni necessaria per ridurre di 10 volte la popolazione (o l’attività) iniziale.
Gray (Gy): dose di radiazione assorbita (1 Gy = 100 rad), dove: 1 rad = 100 erg/g.
Dose letale = 12 x D10
Specie/funzioni Tipologia D10 (Gy)
Clostridium botulinum Gram+, sporigeno 3.300
Salmonella typhimurium Gram- 200
Aspergillus niger Muffa 500
Saccharomyces cerevisiae Lievito 500
Herpes simplex virus-I (afta) Virus 13.000
Inattivazione enzimatica 20.000-50.000
Sterilizzazione
Tecniche FISICHE – onde elettromagnetiche
RADIAZIONI ULTRAVIOLETTE (UV):
▪ onde elettromagnetiche (λ=220-300 nm) prodotte dal passaggio di corrente elettrica attraverso vapori a
bassa pressione di Hg contenuti all’interno di speciali tubi in vetro.
▪ assorbiti dagli acidi nucleici (Amax=269 nm) e dalle proteine (Amax=280 nm).
Meccanismo di azione: danno cellulare (letale) per formazione di dimeri pirimidinici (T-T) che interferiscono
con la replicazione del DNA (effetto mutageno). Max effetto letale a 260 nm.
Applicazioni:
▪ decontaminazione di superfici, aria, acqua in ambienti confinati
▪ limita la quantità di amplificati (PCR) sulle superfici
▪ sterilizzazione “a freddo” di composti chimici, materiali plastici ad uso farmaceutico, siero per colture cellulari
Fattori critici:
▪ scarsa penetrazione (non penetra carta, vetro, indumenti), distanza minima sorgente UV – materiale trattato
▪ intensità della luce (sostituzione ogni 8.000 h)
▪ dipendenza da ambiente (umidità relativa) e specie microbica
▪ mutagena per l’uomo (cute, occhi)
Sterilizzazione
Tecniche FISICHE – onde elettromagnetiche
Sterilizzazione mediante UV di:
A) superfici confinate (interno di una cabina di
sicurezza biologica);
B) strumentazione chirurgica;
C) aria in ambienti confinati;
D) prodotti farmaceutici/di laboratorio.
A B
C D
Sterilizzazione
Tecniche FISICHE – onde elettromagnetiche
INFRAROSSI: onde di lunghezza d'onda compresa tra 700 nm e 1 mm
▪ Tecnica rapida, a basso consumo energetico, non produce residui tossici per l’ambiente.
▪ Possibile impiego per la sterilizzazione di strumenti termoresistenti, ma ad oggi non
esiste un sistema approvato per l’utilizzo in ambito sanitario.
MICROONDE: onde a frequenza radio (λ = 2450 MHz)
▪ Meccanismo di azione: producono attrito tra molecole di H2O in un campo elettrico
alternato; l’attrito produce calore con conseguente effetto letale.
▪ Applicazioni:
▪ disinfezione di prodotti termoresistenti: strumentazione odontoiatrica, lenti a
contatto, dentiere, latte, cateteri urinari (autocateterismo intermittente).
Sterilizzazione
Tecniche FISICHE – ultrasuoni
Energia ultrasonica a bassa frequenza ed energia in grado di inattivare, per cavitazione, i microrganismi
in sospensioni acquose
▪ I sonicatori non vengono considerati alla stregua di sterilizzatori, tuttavia:
▪ la combinazione ultrasuoni + trattamento chimico può avere effetto letale
Sterilizzazione
Tecniche CHIMICHE
ACIDO PERACETICO (perossido di idrogeno)
▪ agente ossidante
▪ immersione (0.2% per 15 min a 50°C)
▪ micronizzato: industria alimentare, strumenti chirurgici
▪ efficace in presenza di materiale organico
▪ produce prodotti finali non tox (acido acetico + O2)
GLUTARALDEIDE
▪ agente alchilante (aggiunta di –CH3, -CH2CH3)
▪ immersione (soluzione al 2%), tempi lunghi (90 min; 20°C)
▪ impiegata per materiale medico-chirurgico e preparazione di vaccini
▪ efficace in presenza di materiale organico
▪ il suo impiego è associato a rischio occupazionale (irritazione mucose respiratorie, dermatite da contatto)
Guideline for Disinfection and Sterilization in Healthcare Facilities (CDC, 2008)
Caratteristiche dei principali sterilizzanti chimici
Sterilizzazione
Tecniche CHIMICO-FISICHE
OSSIDO DI ETILENE (ETO)
▪ Alchilazione di gruppi funzionali (amminici, carbossilici, fenolici, idrossilici) di proteine,
DNA, RNA
▪ Sterilizzazione di materiale/strumentazione sensibile ad alte temperature o calore umido
▪ 12% ETO + 88% Freon (oppure CO2, N2)
▪ L’utilizzo deve essere regolamentato: ETO è infiammabile/esplosivo, carcinogeno e
mutageno
FORMALDEIDE
▪ Agente alchilante
▪ Vaporizzazione 2-5% formaldeide in presenza di vapor acqueo a 60-80°C
▪ Impiegata per sterilizzare filtri HEPA
▪ Irrita le mucose, carcinogena
▪ “Tracce” residue in materiale polimerico (cellulosa, gomma): richiede lavaggio post-
trattamento
Sterilizzazione
Tecniche CHIMICO-FISICHE
PLASMA GAS
▪ Applicazione di energia (radio-frequenza) ad una camera contenente vapori
di H2O2. La temperatura non eccede i 40°C, ma la necessità di vuoto può
deformare la superficie del materiale
▪ La produzione di radicali liberi causa inattivazione microbica
▪ Applicata ad apparecchiature mediche (quando calore o ETO non
appropriati)
▪ Necessita di un’accurata pulizia del materiale da trattare
▪ Non efficace su metalli, cellulosa
Tecniche di sterilizzazione
Pros & cons
Guideline for Disinfection and Sterilization in Healthcare Facilities (CDC, 2008)
Sterilizzazione
Fattori critici per l’efficacia
Guideline for Disinfection and Sterilization in Healthcare Facilities (CDC, 2008)
Sterilizzazione
Caratteristiche di una tecnica «ideale»
Attività: battericida, tubercolicida, fungicida, sporicida, virucida
Rapidità di azione: sterilizzazione raggiunta in breve tempo
Penetrazione: capacità di penetrare nel materiale trattato o nella confezione in cui esso è contenuto
Compatibilità: non causa rilevanti cambiamenti strutturali o funzionali del materiale in seguito a
ripetuti trattamenti
Atossicità: sicuro per l’operatore e l’ambiente
Resistenza a materiale organico: efficacia invariata in presenza di materiale organico
Costo-efficacia: costi ragionevoli per attrezzatura, installazione ed utilizzo
Disinfezione
da: Murray et al. Medical Microbiology 3rd ed., Mosby, 1998
La disinfezione di un prodotto o di una superficie può essere
ottenuta mediante l’impiego di tecniche:
▪ FISICHE
▪ CHIMICHE
Disinfezione
Meccanismo di azione
I disinfettanti causano la morte dei microrganismi mediante differenti meccanismi:
▪ Denaturazione delle proteine (formaldeide, glutaraldeide, ossido di etilene, propriolattone)
▪ Ossidazione di enzimi (perossidi, permanganati, cloro, ipocloriti, iodio)
▪ Alterazione delle membrane (alcooli, fenoli, composti dell’ammonio quaternario, clorexidina)
Disinfezione
Tecniche FISICHE
CALORE UMIDO
Ebollizione (100° C): inattivazione delle forme vegetative e virali entro 10 minuti.
Pastorizzazione:
▪ tecnica ideata da Pasteur per conservare il vino previo riscaldamento a 60°C.
▪ riduce la carica microbica (Salmonella typhi, Escherichia coli O157:H7, Mycobacterium tuberculosis,
Brucella spp, Coxiella burnetii) presente nel latte (ed in altri alimenti deperibili) senza alterarne le
caratteristiche organolettiche:
▪ pastorizzazione di massa: 63-66°C, 30 min
▪ pastorizzazione istantanea (HTST): 71°C, 15 sec
▪ pastorizzazione “ultra-high-temperature” (UHT): 140°C, 1-3 sec
Disinfezione
Tecniche CHIMICHE
ALDEIDI (formaldeide, glutaraldeide).
Dotate di rilevante attività mediante alchilazione dei gruppi polari funzionali
(amminici, idrossilici, fenolici) delle proteine.
Formaldeide:
▪ 37% (formalina), utilizzato come sterilizzante: per fissazione campioni biologici
e preparazione di vaccini.
▪ 3-8%, usato come disinfettante.
▪ irrita le mucose, cancerogeno, forte odore.
Glutaraldeide:
▪ 2% (Cydex): battericida, tubercolicida, fungicida, virucida (10 minuti); sporicida
(3 - 10 ore).
▪ disinfezione strumentazione ospedaliera (termosensibile: endoscopi, superfici
abiotiche).
▪ meno irritante e più efficace della formaldeide.
Disinfezione
Tecniche CHIMICHE
AGENTI OSSIDANTI (perossido di idrogeno, acido peracetico).
Formazione di radicali ossidrilici (OH•) in grado di ossidare sistemi enzimatici “critici” per il microrganismo.
Battericidi, fungicidi, virucidi, sporicidi:
▪ H2O2 (come antisettico, non per ferite aperte).
▪ acido peracetico (come sterilizzante di strumentazione e matrici alimentari): battericida e fungicida (5
min), virucida e sporicida (30 min).
Disinfezione
Tecniche CHIMICHE
ALCOOLI (etanolo, isopropanolo).
Ad alte concentrazioni, danneggiano la membrana citoplasmatica mediante:
▪ denaturazione (coagulazione) delle proteine.
▪ solubilizzazione dei lipidi.
Battericidi, fungicidi, tubercolicidi, virucidi:
▪ attività influenzata dalla presenza di materiale organico
▪ particolarmente attivi verso virus dotati di peplos (involucro di natura lipidica)
▪ isopropanolo più efficace dell’etanolo
Utilizzati in soluzione acquosa al 60-85% come:
▪ antisettici (non per ferite aperte), sebbene alto potere disidratante
▪ disinfettanti (soluzione acquosa): superfici ben ventilate e lontane da fiamme.
Disinfezione
Tecniche CHIMICHE
FENOLI e DERIVATI FENOLICI (fenolo, fenilfenolo, esaclorofene).
Lord Joseph Lister (1827 - 1912), medico e professore di chirurgia inglese, fu l'inventore
e il propugnatore del metodo dell'antisepsi rivoluzionando l'atteggiamento e l'approccio
dei chirurghi alla pratica operatoria.
Fenolo (Lister): tossico, corrosivo, carcinogenico.
Derivati fenolici con gruppo funzionale (cloro, bromo, alchil, benzil, phenyl, amil) a
sostituzione di un H dell’anello aromatico.
Distruzione della membrana plasmatica mediante denaturazione proteica.
Battericidi, fungicidi, tubercolicidi, virucidi:
▪ 2-5% (0.5%, HIV; 2%, funghi).
▪ attività persistente e non influenzata dalla presenza di materiale organico.
▪ O-phenylphenol (Lysol), Irgasan.
▪ esaclorofene (Phisohex): elevata efficacia vs cocchi Gram+, strumenti chirurgici.
Disinfezione
Tecniche CHIMICHE
ALOGENI (ioduri, cloruri, bromuri, fluoruri).
Eliminazione di gruppi S-H per:
▪ ossidazione: formazione di ponti di-sulfidrilici inattivi
▪ combinazione: ione metallico “sottrae” SH liberi
Battericidi, fungicidi, virucidi, si usano in combinazione con metalli per ridurne la
tossicità, instabilità e corrosività.
Ioduri:
▪ soluzione alcolica: tintura di iodio
▪ iodofori: PVP-J (Betadine) per uso cutaneo e chirurgico
Cloruri:
▪ disinfezione di acqua, piscine, acque di scarico
▪ Cl + p-toluene-sulfonamide (cloramina T)
▪ 1:10 sodio-ipoclorito (NaOCl) 5.25% per rischio ematogeni
Disinfezione
Tecniche CHIMICHE
COMPOSTI DELL’AMMONIO QUATERNARIO (QUATs: benzalconio cloruro, cetrimide, clorexidina).
Detergenti cationici, derivati da modificazioni di NH4+.
Distruzione di membrana cellulare, inattivazione enzimatica, denaturazione (coagulazione) proteica.
Batteriostatico (-cida ad elevate concentrazioni), sporostatico, fungistatico, virustatico:
▪ scarsamente attivi vs Gram-: frequenti infezioni da Pseudomonas spp QUATs-resistenti
▪ neutralizzati da materiale organico, saponi e detergenti anionici
▪ non corrosivi, non tossici, stabili, inodori.
Zephiran (benzalconio cloruro), cetrimide, clorexidina.
Disinfezione
Tecniche CHIMICHE
METALLI PESANTI (Ag, Hg, Se, Zn).
Eliminazione di gruppi S-H (in combinazione con un alogeno)
L’impiego è fortemente limitato per tossicità ed inquinamento ambientale:
▪ 1% nitrato di Argento (preparati oftalmici, utilizzati negli infanti per prevenzione gonorrea
oftalmica).
▪ composti organici del Mercurio: mercurocromo, mertiolato (disinfezione cutanea).
▪ Selenio: vs fungi e spore fungine.
▪ Zinco: cloruro- (collutori per la disinfezione del cavo orale) e ossido- (antifungino).
▪ solfato di Rame (piscine e laghi)
Disinfezione
Corretta igiene delle mani
Il Ministero della Salute stima che in Italia ogni anno si verificano 450.000 - 700.000 infezioni in pazienti ricoverati
(complessivamente il 4,5-7% dei ricoveri), il 30% circa delle quali prevenibili.
La cute ed i guanti possono essere veicolo di contaminazione per batteri (stafilococchi, enterococchi, clostridi, P.
aeruginosa, enterobatteri, etc.) e virus (rhinovirus, virus parainfluenzale, virus respiratorio sinciziale, etc.).
IL LAVAGGIO DELLE MANI RAPPRESENTA LA PRINCIPALE MISURA DI CONTROLLO DELLA DIFFUSIONE
DELLE INFEZIONI IN AMBITO SANITARIO.
“Un rigoroso intervento sul lavaggio delle mani è in grado di prevenire circa il 40% di tutte le infezioni nosocomiali”
(Center for Diseases Control – Atlanta, USA)
L’igiene delle mani deve essere altresì intesa anche quale misura di protezione dell’operatore.
Igiene delle mani in ambito sanitario
Le mani: efficace «veicolo» di infezioni
La associazione tra igiene delle mani e la trasmissione delle malattie venne stabilita dagli studi di
Ignaz Semmelweis, a Vienna, e di Oliver Wendell Holmes, a Boston.
Semmelweis nel 1847 dimostrò che il tasso di mortalità (febbre puerperale da streptococchi) tra le
madri che partorivano alla Prima Clinica Ostetrica dell'Ospedale Generale di Vienna era
significativamente inferiore quando il personale effettuava il lavaggio delle mani con un agente
antisettico (cloruro di calcio) rispetto ai lavaggi delle mani con acqua e sapone semplice.
Igiene delle mani in ambito sanitario
Le mani: efficace «veicolo» di infezioni
Nel 1938 Price stabilì che i batteri delle mani possono essere suddivisi in due categorie: residenti o transitori. La
composizione quali/quantitativa della flora transitoria e residente variano notevolmente da un soggetto all'altro.
Flo
ra R
ES
IDEN
TE
• Microrganismi residenti sotto lo strato corneo; si
trovano anche alla superficie cutanea
• Composta da batteri (stafilococchi, corineformi
(corinebatteri, propiobatteri, micrococchi) e
funghi (Pityrosporum)
• Duplice funzione protettiva: antagonismo
microbico e competizione per le sostanze
nutrienti nell’ecosistema
• Può provocare infezioni in cavità sterili, occhi o
cute non intatta
Flo
ra T
RA
NS
ITO
RIA
• Colonizza gli strati superficiali della cute
• I microrganismi non si replicano ma
sopravvivono. Pertanto, vengono rimossi più
facilmente con i lavaggi routinari delle mani.
• Causa di infezioni associate all’assistenza:
contratti dal personale sanitario tramite
contatto con i pazienti e/o superfici ambientali
contaminate.
• Le mani di alcuni operatori possono essere
costantemente colonizzate da MRSA, Gram-
negativi o lieviti (Candida)
• La trasmissibilità dipende da: numero
microrganismi, specie, umidità della cute.
Igiene delle mani in ambito sanitario
Le mani: efficace «veicolo» di infezioni
FLORA BATTERICA PRESENTE SULLA CUTE
La cute umana normale è colonizzata da batteri, con conte totali di batteri aerobi
variabili:
▪ 1.000.000 cellule/cm2 sul cuoio capelluto
▪ 500.000 cellule/cm2 nell'ascella
▪ 40.000 cellule/cm2 sull'addome
▪ 10.000 cellule/cm2 sull'avambraccio.
Le conte batteriche totali sulle mani del personale ospedaliero oscillano tra 40.000 a 4.600.000 cellule/cm2
Igiene delle mani in ambito sanitario
Le mani: efficace «veicolo» di infezioni
TRASFERIMENTI DURANTE LA ATTIVITA’ LAVORATIVA
Le mani degli operatori sanitari vengono contaminate nel corso di attività
"pulite", quali sollevare i pazienti, misurare il polso, la pressione sanguigna o la
temperatura, oppure toccando la mano, la spalla o l'inguine del paziente.
I guanti risultano essere altamente colonizzati a seguito di contatto con
differenti siti corporei, in particolare l’area inguinale.
Studi relativi alla contaminazione delle mani del personale sanitario prima e dopo il contatto diretto con il paziente,
la medicazione di ferite, la gestione di cateteri intravascolari, l’assistenza respiratoria o la manipolazione delle
secrezioni dei pazienti, hanno evidenziato che il contatto diretto con il paziente e l’assistenza respiratoria sono
risultate essere le attività che provocavano la più elevata contaminazione delle dita degli operatori.
Igiene delle mani in ambito sanitario
Tecniche per la disinfezione delle mani
1. LAVAGGIO NORMALE = azione di igienizzazione delle mani al fine di rimuovere
fisicamente o meccanicamente lipidi, sporco aderente, terra e varie sostanze organiche.
Si effettua mediante utilizzo di detergenti, composti (tensioattivi) che presentano un'azione
detergente. Generalmente indicati con il termine "sapone semplice», non sono dotati per se di
attività antimicrobica, ma facilitano la rimozione meccanica (per sfregamento) della flora
transiente (circa 80%). Degradano la pellicola idrolipidica sopracutanea (emulsificazione).
Occasionalmente, i saponi semplici possono contaminarsi, provocando la colonizzazione
delle mani degli operatori sanitari con bacilli Gram-negativi. E’ consigliabile l’impiego di
dispenser. Tuttavia, il pericolo concreto di trasmettere microrganismi tramite il lavaggio con
saponette già utilizzate è irrilevante.
La decontaminazione delle mani può essere ottenuta mediante lavaggio normale oppure lavaggio antisettico
Igiene delle mani in ambito sanitario
Tecniche per la disinfezione delle mani
2. LAVAGGIO ANTISETTICO = si utilizza una soluzione/gel per frizioni ad azione antisettica,
oppure il lavaggio con acqua e antisettico, al fine di ridurre la flora transitoria e con minimo
effetto su quella residente.
A. La frizione antisettica si effettua mediante prodotti a base alcolica (60-80% etanolo od
isopropanolo in formulazione liquida, gel o schiuma). Non richiede l'utilizzo di fonti idriche
esogene. Dopo l'applicazione, si procede a strofinare le mani l'una contro l'altra fino a che
l'agente non sia asciutto.
Grazie alla loro azione denaturante sulle proteine, gli alcoli presentano un'eccellente attività
verso batteri (inclusi i patogeni antibiotico-resistenti MRSA e VRE), M. tuberculosis, virus
(herpes simplex, HIV, influenza, RSV) e diversi funghi.
Non presentano, tuttavia, alcuna attività rispetto alle spore batteriche od alle cisti dei
protozoi, ed un'attività ridotta sui virus privi di involucro (rotavirus, adenovirus, enterovirus).
Gli alcoli non sono buoni agenti detergenti e se ne sconsiglia l'uso in caso di mani sporche o
visibilmente contaminate con materiali proteici (es. sangue). E’ possibile, sebbene rara, la
contaminazione delle soluzioni a base alcolica (spore di Bacillus cereus).
Igiene delle mani in ambito sanitario
Tecniche per la disinfezione delle mani
B. Il lavaggio antisettico si avvale dell’impiego dei un sapone contenente un agente antisettico, sostanza
antimicrobica che riduce o inibisce la crescita dei microrganismi sui tessuti viventi (alcool, gluconato di clorexidina,
derivati del cloro, iodio, cloroxilenolo, composti dell’ammonio quaternario, triclosan).
Clorexidina: attività antimicrobica (attribuibile alla rottura delle membrane citoplasmatiche) inferiore a quella degli
alcoli. Dimostra una buona attività contro i batteri Gram-positivi, inferiore contro i batteri Gram-negativi e i funghi,
ed un'attività minima contro i micobatteri. La clorexidina non è sporicida. Ha invece un'attività in vitro rispetto ai
virus lipofili, ma meno marcata rispetto ai virus privi di involucro. L'attività non viene compromessa dalla presenza
di materiale organico, come il sangue.
Composti dell’ammonio quaternario (alchil-benzalconio cloruro): principalmente batteriostatici e fungistatici, sono
più attivi contro i batteri Gram-positivi rispetto ai bacilli Gram-negativi. Hanno un'attività relativamente debole
verso micobatteri e funghi, e presentano un'attività superiore contro i virus lipofili. La loro attività antimicrobica
viene influenzata negativamente dalla presenza di materiale organico. Causa la ridotta attività contro i batteri Gram-
negativi, sono frequentemente soggetti a contaminazione.
Igiene delle mani in ambito sanitario
Tecnica di lavaggio delle mani
bagnare
uniformemente le
mani
erogare sulle mani il
prodotto antisettico,
premendo con il
gomito la leva del
dispenser
sfregare
vigorosamente le
mani l’una con l’altra
sfregare il palmo
destro sul dorso della
mano sinistra e
viceversa
sfregare i palmi tra di
loro con le dita
intrecciate
lavare gli spazi sub-
ungueali, utilizzando
uno spazzolino
preventivamente
bagnato e cosparso di
una dose di
antisettico
assicurarsi che i pollici
tocchino i polsi
dell’una e dell’altra
mano
decontaminare la
punta delle dita,
sfregandole contro il
palmo dell’altra mano
massaggiare
vigorosamente la
parte superiore delle
dita nel palmo
dell’altra mano con le
dita intrecciate
risciacquare, avendo
cura di evitare il
ruscellamento di
acqua dagli
avambracci alle mani
chiudere il rubinetto
(pedale, gomito o
punta delle dita)
asciugare, con
movimenti circolari, le
singole dita, quindi le
restanti porzioni delle
mani
Il lavaggio completo richiede circa 60 secondi
La frizione antisettica richiede circa 30 secondi
Igiene delle mani in ambito sanitario
Sapone: meccanismo di azione
▪ I saponi agiscono alla stregua di surfattanti, molecole polari
con estremità idrofobiche ed idrofiliche.
▪ Possono legarsi al doppio strato lidico, distruggendolo,
aumentando in tal modo la permeabilità di membrana.
Igiene delle mani in ambito sanitario
«Inadeguato» lavaggio delle mani
Il lavaggio delle mani viene spesso effettuato in maniera inadeguata: ridotto tempo di lavaggio, utilizzo di prodotti
inadatti, tecnica errata.
Pertanto, a seguito di un lavaggio «inadeguato» numerosi siti possono risultare ancora contaminati e, quindi,
ancora potenzialmente «utili» al trasferimento di microrganismi.
Disinfezione
Fattori critici
Ambiente:
▪ temperatura: optimum: 20-37°C. Una diminuzione della temperatura riduce l’efficacia. Un aumento pari a 10°C
determina un aumento 2x della velocità di azione
▪ pH del mezzo in cui deve agire il disinfettante
Materiale:
▪ natura del materiale (porosità)
▪ presenza di materiale organico (sangue, pus, vomito, feci)
▪ inattivazione principio attivo
▪ rivestimento della superficie batterica
▪ adsorbimento (eliminazione) del principio attivo
Disinfettante:
▪ concentrazione del principio attivo
▪ tempo di applicazione (contatto con materiale)
▪ qualità acqua per diluizione disinfettante
Disinfezione
Fattori critici
Microrganismo:
▪ tipologia
▪ i batteri Gram-negativi (presenza della membrana esterna) sono generalmente più resistenti dei Gram-
positivi ai disinfettanti ed antisettici.
▪ micobatteri, endospore e cisti protozoarie sono molto resistenti ai disinfettanti ed antisettici.
▪ i virus sprovvisti di envelope (rivestimento di natura lipidica) sono generalmente più resistenti a
disinfettanti ed antisettici rispetto ai virus con envelope.
▪ carica microbica: la attività di un disinfettante è inversamente proporzionale alla concentrazione microbica.
▪ organizzazione
▪ presenza di biofilm: comunità cellulare multistratificata sessile in cui gli elementi cellulari sono immersi in
una matrice polisaccaridica (slime) di derivazione batterica. La matrice potrebbe influenzare l’attività del
disinfettante o inattivandolo interagendo chimicamente con esso o rallentandone la diffusione attraverso
gli strati cellulari più profondi.
Disinfezione
Caratteristiche «ideali» di un disinfettante
▪ Attività: esteso spettro di azione (battericida, fungicida, sporicida, tubercolicida, viricida)
▪ Rapidità di azione: breve “tempo minimo di applicazione” (1-10 minuti)
▪ Atossicità: non irritante per occhi, mucose, cute
▪ Non deve possedere capacità tintoriali
▪ Non corrosivo
▪ Stabilità: per diluizioni e tempi consigliati (anche in presenza di materiale organico)
▪ Buona capacità di penetrazione e detersione
▪ Costi: ragionevoli (economicità)
Tecniche di sterilizzazione/disinfezione
Criteri per la scelta
Un approccio conveniente è quello suggerito da
Spaulding, applicato nelle linee-guida U.S.
Gli oggetti sono classificati, sulla base del loro impiego,
come:
▪ critici
▪ semi-critici
▪ non critici
I relativi livelli di disinfezione sono:
▪ elevato (High Level of Disinfection, HLD)
▪ intermedio (Intermediate Level of Disinfection, ILD)
▪ basso (Low Level of Disinfection, LLD)
ele
va
ta S
ba
ssa
S Alto livello di
disinfezione
Basso livello di
disinfezione
Livello intermedio
di disinfezione
Tecniche di sterilizzazione/disinfezione
Criteri per la scelta – trattamento di oggetti «critici»
Oggetti “critici” = quelli collegati ad un alto rischio di trasmettere infezione, qualora vengano contaminati da
microrganismi, ivi incluse le spore batteriche:
▪ a contatto con tessuti viventi fisiologicamente sterili
▪ inseriti nel sistema vascolare (strumentazione chirurgica, protesi, aghi, cateteri urinari/cardiaci,
artroscopi, etc).
Obiettivo: inattivazione forme vegetative e sporali (sterilità).
Metodo: sterilizzante
▪ fisico (vapore)
▪ chimico (glutaraldeide 2%, perossido di idrogeno 6%, acido peracetico)
▪ chimico-fisico (ETO, plasma gas)
Tecniche di sterilizzazione/disinfezione
Criteri per la scelta – trattamento di oggetti «semi-critici»
Oggetti “semi-critici” = quelli che vengono a contatto con le mucose o con la cute integra (endoscopi,
termometri, vasche per idroterapia, attrezzatura per terapia respiratoria/anestesiologica).
Obiettivo: Inattivazione delle forme vegetative. E’ tollerabile la presenza di spore in quanto le mucose intatte
sono generalmente resistenti all’infezione.
Metodo: High or Intermediate Level of Disinfection (HLD, ILD)
▪ glutaraldeide
▪ perossido di idrogeno
▪ perossido di idrogeno + acido peracetico
▪ cloro
▪ composti fenolici
▪ iodofori
Tecniche di sterilizzazione/disinfezione
Criteri per la scelta – trattamento di oggetti «non critici»
Oggetti “non critici” = quelli che vengono a contatto con la cute intatta ma non con le mucose
(strumentazioni mediche, superfici ambientali, suppellettili del paziente: padelle, bracciali per la misurazione
della pressione sanguigna, stetoscopi, stampelle, sbarre per i letti, biancheria, alcuni tipi di posate o stoviglie,
comodini e arredi dell’unità del paziente).
Obiettivo = basso grado di contaminazione; la cute intatta, infatti, agisce come un’efficace barriera contro la
maggior parte dei microrganismi, e la sterilità di questi oggetti non è richiesta.
Metodo: Low Level of Disinfection (ILD, LLD)
▪ alcool etilico
▪ ioduri
▪ composti dell’ammonio quaternario
▪ fenoli
Tecniche di sterilizzazione/disinfezione
Criteri per la scelta
http://www.asl.pavia.it/webasl/UffEdSan.nsf/risRicDom/29979FA2AB0E7B00C1256E14004F2A6D/$File/Protocollo%20Disinfettanti%20.pdf
Questo materiale non può essere distribuito, modificato o pubblicato né in forma cartacea, né su un sito, né utilizzato per motivi pubblici o commerciali.
E’ possibile utilizzare il materiale solo per motivi personali e non commerciali, purché ogni copia di questo materiale preservi tutti i diritti di copyright e di proprietà intellettuale, sempre a seguito di formale richiesta rivolta all’Autore (Prof. Giovanni Di Bonaventura; [email protected])