Citogene1ca e biologia molecolare delle MDS - Siematologia · Citogenetica nella MDS •Risultati...
Transcript of Citogene1ca e biologia molecolare delle MDS - Siematologia · Citogenetica nella MDS •Risultati...

GiuseppeCalabreseOspedaleSpiritoSanto,PescaraUniversitàdiChie7
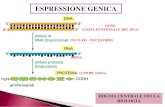
Citogene1caebiologiamolecolaredelleMDS

Definizione
Le sindromi mielodisplastiche sono ungruppo di malattie clonali delle cellulestaminali emopoietiche caratterizzate da
• ematopoiesi inefficace• dismorfismi delle varie filiere maturative• citopenie nel sangue periferico• Variabile tendenza alla evoluzione in
leucemia acuta mieloide

MPD MDS AMLRA
RARS
RA mult.
Dyspl
RAEB
sind. 5q-
t MDS
AML con
displ. Multilin
(con o senzaMDS preced)
AML ther.rel.
(Alchil, epipod.
altro)
con alt. citogen
t(8;21)
t(15;17)
inv(16)
alt. 11q23
Non ult
categoriz.
M0-M7 bifen,bas
MPDMDSJMML
aCML
CMML
CML Ph+
CNL
CEL
MI
PV
TE

Citogenetica nella MDS
• Delezioni o monosomie– Forme de novo 40-60%– Forme secondarie 70-80%
• Traslocazioni cromosomiche 2-5%

anomalie citogeneticheAlter. non bilanciate Alter. StrutturaliPerdite Acquisizioni
t(3;3)-5/5q- +8 inv(3)-7/7q- +11 t(3;5), t(3;21)11q- +21 t(5;12), t(5;17)-17/17p- i(17)-Y t(10;12)
complesse (>2 cromosomio >3 breakpoits)

• Alterazioni citogenetiche presenti nel 30-70% dei pazientiaffetti da MDS (t-MDS 95%)
• Nelle MDS primitive prevalgono le alterazioni singolecui possono aggiungersi altre alterazioni; ogni cromosomapuò essere interessato
• Nelle t-MDS le anomalie singole sono limitate per lo piùai cromosomi 5, 7 e 12. Spesso cariotipi complessi concospicue alterazioni qualitative, variazioni da metafase ametafase e cromosomi ad anello o dicentrici.
• Alterazioni condivise con le LAM (tranne pocheeccezioni)
anomalie citogenetiche

Valutazione prognostica
Low risk
low risk
int-1/low
high risk
int-2/high High risk
IPSS
Blasti midollari <10%
Blasti midollari >10%
Sistema prognostico internazionale per le SMD basato su numero diblasti, citogenetica e grado di citopenia

Citogenetica nella MDS
Rischio da anomaliacitogenetica (frequenzain MDS)
Anomalie citogenetiche Rischio di progressionein LMA (anni)*
Sopravvivenza mediana(anni)
Basso (51%) Cariotipo normaledel(5q) isolatadel(20q) isolata-Y isolata
5,6 3,8
Intermedio (32%) +81 o 2 anomaliemiscellanee noncomuni
1,6 2,4
Alto (17%) -7 o del(7q)Cariotipo complesso(<2 anomalie)
0,9 0,8
Significato prognostico delle anomalie cromosomiche nell’IPSS
* Intervallo di tempo necessario perché il 25% dei pazienti progredisca in LMA (Olney & LeBeau 2007)

Citogenetica nella MDSAnomalie crom. in FAB Anomalie crom. in WHO Anomalie crom. in IPSS
% % %
RARS 43 RARS 33 Basso 26
RA 53 RA 44 Intermedio 1 56
RAEB 71 MDS del(5q) 100 Intermedio 2 75
RAEB-t 81 RCMDS 75 Alto 94
RCMD 47
RAEB-1 66
RAEB-2 67
MDS-U 57

Citogenetica nella MDS
0,0
5,0
10,0
15,0
20,0
25,0
30,0
35,0
40,0
45,0
normale
1 anomalia
2 anomalie
car. complex
anomalia Singola%
Associata%
+1q 1,2
anom. 3q 2,6
del(5q) 8,7 20
-7 2,7 10
del(7q)(q31q35) 4,1
+8 4,5 10
del(11)(q14q23) 1,0
del(12p) 3,4
del(17p) 1,2 7
del(20q) 3,0 5
-Y 1,0 10
Miscellanee 5,5

Citogenetica nella MDS• Riarrangiamenti cromosomici ricorrenti rari
anomalia geni coinvolti correlazione clinica

La sindrome del 5q-: un sottotipo distinto• Descritta per la prima volta da Van den Berghe (1974) e
successivamente da Sokal (1975)• Clinicamente:
– anemia macrocitica– piastrine normali o aumentate– Prevalente sesso femminile– Eritropoiesi ipoplasica, aumentato numero di megacariociti, molti
con nuclei ipolobati (micromegacariociti)– blasti midollari <5%
• delezione isolata in 5q• lunga sopravvivenza e prognosi simile ai pazienti con RA (criteri
WHO)• Necessari ulteriori studi citogenetici e molecolari per individuare il (i)
gene (i) responsabili.• Terapia con Lenalidomide


Difetti cromosomici che non individuanoentità biologico-cliniche specifiche
Anomalia Diagnosi Filiere cellulari coinvolte
20q- MDS/PV Mieloide e linfoide B
-7 MDS/MPS Mieloide e linfoide B
7q- MDS/AML ----------
+8 MDS/AML/MPS Mieloide
+1q MDS/ALL/MPS -----------

5q− (n=59) − 7 /7q− (n=38) trisomy8(n=44)
Addi%onalanomaly % Addi%onalanomaly % Addi%onalanomaly %
+8 17 +21 10 5q− 23+21 13 5q− 10 +21 11
−2 0/20q− 8 +8 10 der(3q21/q26) 7
−7 7 inv(3q) 5 +11 7
der/del(12p) 7 del(12p) 5 −7 5
der/del(3p) 5 t(11q23) 5 del(12p) 5
der/t(21q) 5 iso(17)(q10) 5 +13 5
t(11q23) 3 Others 50 +14 5Others 35 +8* 5
del(1p) 5Others 22
Frequencies (in percent of all cases with the respective primaryabnormality) of accompanying abnormalities (Haase et al 2007;2008)

Citogenetica nella MDS• Sono stati condotti finora pochi studi con l’utilizzo
dell’M-FISH/SKY nelle MDS;• Nel nostro laboratorio abbiamo analizzato 31 pazienti
(13M/11F) con MDS;• Provenienza: ospedale di Pescara, Napoli e Reggio
Calabria;• Età media: 65 aa (range 16-81);• Sottogruppi FAB: RA: 1; RAEB: 5; RAEBt: 7; MDS
con pancitopenia: 1; MDS con gammopatia: 1;MDS non classificati 14; MDS secondaria a LLC: 1;MDS secondaria a LMMC: 1.
• Sopravvivenza media: 37 mesi (range 1-108 mesi).Pazienti viventi 10.

Citogenetica nella MDS
• Risultati 1.• L’analisi in SKY ha permesso di:• ridefinire il cariotipo in 17/18 casi con >3
breakpoint (91%);• confermare il cariotipo osservato in
citogenetica convenzionale nei 13 casi con <3cromosomi rimaneggiati.

Citogenetica nella MDS• Risultati 2.• Sono stati classificati mediante SKY:
• 17 cromosomi marker;
• 8 cromosomi citogeneticamente identificati soloparzialmente (add);
• 4 cromosomi dicentrici;• 10 traslocazioni parzialmente non definite.
• 3 traslocazioni criptiche;

Citogenetica nella MDS
• delezione diTEL/ETV6 in 7pazienti
• delezione di TP53in 6 pazienti
11
11
12
12
• Risultati 3.• Sono così stati individuati riarrangiati geni specifici:• Amplificazione di
MLL in 3 pazienti

Riarrangiamenti dei cromosomi 5, 7 e 11nelle MDS
• L’analisi in FISH con sonde locus- o gene-specifiche el’analisi SKY consentono di migliorare notevolmente ladefinizione del cariotipo nei disordini ematologici anchecon campioni critici (Veldman et al 1997; Kazuka et al1999; Calabrese et al 2000; Van Limbergen et al 2002).
• Tuttavia nei riarrangiamenti complessi intracromosomici lacaratterizzazione di cromosomi anomali rimane di difficileesecuzione (Rowley, 1999; Nietzel et al 2002; Heller et al2004).

Citogenetica nella MDSL’analisi con bandeggiatura multicolor (MCB) ha permesso di definireulteriormente i riarrangiamenti in 8/11 pazienti con >3 breakpoint giàriclassificati mediante SKY
Paz.10
Paz. 15

Citogenetica nella MDS• Conclusioni.• L’analisi citogenetica è necessaria per la caratterizzazione dei pazienti.
Il cariotipo da midollo osseo è importante alla diagnosi. Durante il followup esso può essere affiancato dalla FISH;
• L’analisi in SKY ha ridefinito il cariotipo nel 91% dei pazienti con MDSanalizzati alla diagnosi;
• Sono state identificate 13 traslocazioni criptiche o parzialmente criptiche.Una anomalia cromosomica non specifica ricorrente identificatadall’analisi in SKY [t(1;16)(q11;q11)] in 2 pazienti potrebbe rappresentareun nuovo marker della malattia;
• Le metodologie SKY e MCB hanno consentito di svelare ilriarrangiamento di geni coinvolti nella progressione della MDS fornendoinformazioni sulle basi biologiche della malattia.

-5/del(5q)
-5 -5
del(5q)
FISH

-7
del(7)(q33)
del(7)(q25)
del(7)(q33)
-7 / del(7q)

+8

Cariotipo o FISH?Major implications for monitoring myelodysplastic syndrome patients withdel(5q) treated by lenalidomide (Gohring et al 2011):1.the del(5q) clone is detected with significantly greater sensitivity by karyotyping than byFISH, thus making the diagnosis of non-remission and cytogenetic relapse possible only bykaryotyping in a significant number of patients.2.without prior knowledge of the additional chromosome aberrations, clonal evolution canonly be identified by karyotyping. At the time point of clonal evolution, even del(5q) isdetected only by karyotyping in a significant number of patients.3.detection of the del(5q) clone is sometimes only possible by FISH, making the diagnosis ofnon-remission and cytogenetic relapse in these patients only possible by FISH analysis.
Thus, all cytogenetic follow-up investigations must include karyotyping.FISH analysis should be performed if karyotyping gives no sufficient results,e.g. due to poor chromosome morphology or due to a low number of metaphases(< 25 metaphases).

Citogenetica delle MDS
• Ulteriori indagini:• verifica del coinvolgimento di sequenze
responsabili dell’insorgenza del breakpointin 5q (LCRs)
• arrayCGH

2011-Mutazioni geniche in SMD : >16 target%
Bejar & Ebert 2011

Loss of function
Gain of function
Loss/Gain of function
Targets of point mutations and deletions in MDS (Bejar et al 2011)

Galm et al 2006
Epigenetica nella MDS
MBP: proteina legante metilcitosina
HDAC: deacetilasi istonica
A: attivatore trascrizionale
R: repressore trascrizionale
CpG metilata
CpG demetilata
HAT: acetiltransferasi istonica
TF: fattore di trascriz.

Hanno collaborato:Genetica Medica Chieti/PescaraG. PalkaP. Guanciali Franchi D. Fantasia R. Di GianfilippoE. MorizioD. Romagno
Genetica Medica, Reggio Calabria Genetica Medica Napoli ASL01C. Laganà A. Zatterale
Ematologia PescaraR. Di LorenzoT. SpadanoG. Fioritoni














![I quaderni del MdS - Il mestiere di scrivere · Vita da editor [post dal MdS: 2003-2010] di Luisa Carrada agosto 2010. ... Meghnagi in italiano. È stata una bella idea, anche se](https://static.fdocumenti.com/doc/165x107/5c69e4bf09d3f2310b8bca6c/i-quaderni-del-mds-il-mestiere-di-vita-da-editor-post-dal-mds-2003-2010.jpg)