ANNO ACCADEMICO 2012/2013 - padis.uniroma1.itpadis.uniroma1.it/bitstream/10805/1894/1/Trattamento...
Transcript of ANNO ACCADEMICO 2012/2013 - padis.uniroma1.itpadis.uniroma1.it/bitstream/10805/1894/1/Trattamento...

1
UNIVERSITÀ DEGLI STUDI DI ROMA
“SAPIENZA”
TRATTAMENTO CHIRURGICO
DELL’ERNIA GASTRICA IATALE
RReellaattoorree:: DDoottttoorraannddoo::
PPrrooff.. GGiioorrggiioo PPaallaazzzziinnii GGaabbrriieellee LLaa GGiiooiiaa
MMaattrr::.. 668822227700
ANNO ACCADEMICO 2012/2013

2

3
INDICE
CCaappiittoolloo II
3-a Anatomia del Giunto Esofago-Gastrico
3-b Fisiologia del giunto esofago-gastrico
CCaappiittoolloo IIII
Fisiopatologia dell’ernia Gastrica Iatale
CCaappiittoolloo IIIIII
Presentazione clinica
CCaappiittoolloo IIVV
Complicanze
CCaappiittoolloo VV
Diagnostica Clinico-Strumentale
Rx esofago-baritato
Manometria
pH-metria
EGDS

4
CCaappiittoolloo VVII
Terapia Medica della Malattia dell’Ernia gastrica iatale
CCaappiittoolloo VVIIII
Terapia Endoscopica
CCaappiittoolloo VVIIIIII
Terapia chirurgica
Indicazioni al trattamento chirurgico
Cenni Storici e Tecniche Chirurgiche
Tecnica secondo Nissen-Rossetti
Tecnica secondo Dor e Toupet
CCaappiittoolloo IIXX
Complicanze della terapia chirurgica
CCaappiittoolloo XX
Casistica
CCaappiittoolloo XXII
Risultati

5
CCaappiittoolloo XXIIII
Discussione e conclusioni
BBIIBBLLIIOOGGRRAAFFIIAA
IINNTTRROODDUUZZIIOONNEE

6

7
CCAAPPIITTOOLLOO II
AANNAATTOOMMIIAA EE FFIISSIIOOLLOOGGIIAA

8
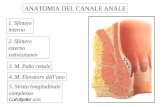
ANATOMIA DEL GIUNTO ESOFAGO-GASTRICO
La giunzione esofago-gastrica risulta essere una zona anatomica di particolare
importanza per la patogenesi della Malattia da Reflusso GastroEsofageo.
Cardias e Giunzione Esofago-Gastrica: LINEA Z (quadro endoscopico
normale)
I confini anatomici e fisiologici tra esofago e stomaco non sono sovrapponibili,
in quanto il passaggio dalla mucosa squamo-cellulare a quella gastrica,
facilmente riconoscibile e individuabile nella Linea Z posta ad un centimetro
circa al di sopra del cardias, non coincide con quello funzionale posto nello

9
Sfintere Esofageo Inferiore. In ogni caso, le diverse componenti anatomiche-
funzionali contribuiscono in modo unitario al regolare transito del cibo in senso
oro-distale, alla prevenzione del reflusso di materiale gastrico in esofago, a
permettere l’eruttazione e, quando necessario, il vomito.
L’esofago è un condotto muscolo- membranoso che si estende dal faringe allo
stomaco per una lunghezza di circa 24 cm, scorrendo nella loggia mediastinica
sino al diaframma. Esso si trova interposto nella sua parte terminale tra due
cavità, di sui una a pressione negativa (quella toracica), e l’altra positiva (quella
addominale). L’esofago giunge in addome insieme ai nervi vaghi attraversando
il diaframma in corrispondenza dello iato esofageo, il quale, il più delle volte, è
costituito da uno sdoppiamento del solo pilastro diaframmatico mediale destro,
le cui fibre partono dalla II, III e IV vertebra lombare, formando una sorta di
fionda. Questa zona è situata radiologicamente a livello della X-XI vertebra
toracica.
L’esofago si estende per altri 4-5 cm, per poi unirsi allo stomaco, un po’ al di
sotto del fondo gastrico, col quale viene a formare un angolo acuto, detto Angolo
di His. La giunzione esofago-gastrica, vista all’interno dello stomaco, viene ad
assumere un aspetto a becco di flauto, il cui margine superiore costituisce una
vera valvola mucosa, la Valvola di Von Gubaroff, la cui struttura è rinforzata
dalle fibre arciformi della muscolatura gastrica che si dispongono a collare
attorno alla regione cardiale (collare di Helvetius). L’angolo di His viene
costantemente mantenuto acuto dal gioco delle contrazioni del pilastro destro

10
diaframmatico, detto anche Laccio di Allison, che circonda l’esofago terminale.
È, dunque, proprio in corrispondenza della giunzione esofago-gastrica, che esiste
un insieme di strutture anatomiche e funzionali costituenti la cosidetta barriera
anti-reflusso. La continenza è sicuramente legata all’esistenza dello Sfintere
Esofageo Inferiore (SEI). Le strutture che costituiscono le barriere anti-reflusso
sono:
Sfintere Esofageo Inferiore (SEI):
separa la pressione negativa intraesofagea, da quella positiva intragastrica. E’
anatomicamente costituito da fibre muscolari lisce del tratto terminale del corpo
esofageo che si continuano senza interruzione nella muscolatura dello stomaco.
Sebbene a questo livello non sia stata mai individuata una vera e propria
struttura anatomica sfinteriale, studi manometrci hanno evidenziato una zona ad
alta pressione, situata all’estremo distale dell’esofago.Ricerche evidenziano che
non esiste una pressione dello sfintere, ma un intero range ad alta pressione,
distribuito in senso radiale e in senso assiale e che riguarda una zona di
lunghezza di circa 3-4 cm situata nella parte terminale dell’esofago al di sopra
della giunzione Squamo-Colonnare.
Esofago Addominale:
L’esistenza di un esofago addominale sottomesso alle variazioni di pressioni
esistenti in addome è indispensabile; la mancanza di questo segmento esofageo
(mal posizione cardio-tuberositaria, ernia iatale da scivolamento), rappresenta un

11
elemento anatomico che potrebbe determinare la genesi del Reflusso Gastro-
Esofageo.
La lunghezza di questo segmento è in media di 4-5 cm e comprende: una
porzione sovra diaframmatica con una terminazione un po’ dilatata a fuso
dell’esofago toracico, una porzione diaframmatica ristretta di 2 cm ed una
porzione sotto-diaframmatica addominale di 3 cm circa.
Angolo di His:
Il cardias, giunzione esofago-gastrica, è posto in un piano obliquo diretto verso il
basso e verso destra a formare un angolo di 30°-45° sul piano orizzontale; il

12
margine destro dell’esofago prosegue con la piccola curva gastrica, mentre il
margine sinistro risulta addossato alla grande tuberosità, formando con essa un
angolo (l’angolo di His). L’ampiezza di tale angolo varia al variare del
riempimento gastrico: angolo acuto quando lo stomaco è pieno, angolo retto
quando lo stomaco è vuoto.
Questa incisura esterna solleva una piega mucosa all’interno dello stomaco, detta
Valvola di Von Gubaroff, frutto dell’addossamento delle mucose che tappezzano
esofago e stomaco. L’assenza o la scomparsa dell’angolo di His viene osservata
in occasione di mal posizioni cardio-tuberositarie e di ernie iatali da
scivolamento; essa può favorire la comparsa di un reflusso gastro-esofageo.
Bretella di Laimer
È un foglietto di fibre provenienti dallo stomaco che avvolgono l’esofago distale.
Contribuisce a mantenere acuto l’angolo di His.
Diaframma:
I pilastri del diaframma delimitano lo iato esofageo. Di forma ovalare (3x1.5
cm), con asse maggiore verso l’alto, anteriormente e verso sinistra; è mobile con
la respirazione. Nella formazione dello iato, la predominanza delle fibre
provenienti dal pilastro destro è pressoché la regola; esse, si dispongono intorno
all’esofago formando una sorta di laccio.

13
I pilastri del diaframma rappresentano la muscolatura estrinseca dello iato; non
rappresentano un mezzo di ancoraggio dell’esofago, ma intervengono in
occasione di movimenti respiratori.
L’allontanamento dei pilastri permette la formazione di un’ernia iatale da
scivolamento.
Membrana freno-esofagea:
E’ una lamina elastico-connettivale, costituita dalla fusione della fascia
diaframmatica endo-toracica con quella endo-addominale, con qualche
fibrocellula muscolare a provenienza dal diaframma, si presenta con l’aspetto di
due tronchi di cono, uniti alle basi, uno superiore ed uno inferiore. Questa,
penetrando nella parete della porzione intraiatale esofagea fino alla tonaca
muscolare, costituisce un’altra importante struttura di fissazione del viscere e fa
si che l’esofago distale (gli ultimi 3 cm), sia in sede endoaddominale,
rappresentando uno dei meccanismi antireflusso.
Meso-esofago:
Il meso-esofago è un tessuto cellulo-fibroso denso che trova posto nello spazio
di divaricazione tra i due foglietti peritoneali che collegano il viscere alla parete
posteriore. Occupa tutta la larghezza dell’esofago e connette in tal modo le sue
facce posteriori e laterali all’aorta e ai pilastri del diaframma garantendo in tal
modo la permanenza del viscere in addome; la sua sezione o dissezione
permette, infatti, l’ascenzione intra-toracica dell’esofago. Il legamento gastro-

14
frenico, altro elemento cellulo-fibroso denso, prolunga verso sinistra il meso-
esofago ed àncora la grande tuberosità gastrica al diaframma.
Muscolatura del corpo dell’esofago:
Le normali contrazioni della parete dell’esofago sono necessarie per il completo
e normale svuotamento del viscere. La parete muscolare dell’esofago comprende
uno strato di fibre superficiali longitudinali ed uno strato di fibre circolari
profonde. Queste fibre circolari circondano l’angolo di His, intrecciate con le
fibre oblique dello stomaco e scendono sui due versanti della piccola curva (
cravatta di Helvetius).

15
FISIOLOGIA DEL GIUNTO ESOFAGO-GASTRICO
A livello della giunzione esofago-gastrica, una zona funzionalmente di grande
importanza è lo sfintere esofageo inferiore, costituito da fibre lisce e contratte
tonicamente volte a creare una zona ad alta pressione. Una serie di fattori
condiziona il tono dello sfintere, con il compito precipuo di consentirne il
rilasciamento, dopo l’inizio della deglutizione, e la contrazione post-deglutitoria
per prevenirne il reflusso.
Il nervo vago è principalmente coinvolto nel controllo riflesso della contrazione
o del rilasciamento del SEI. I neuroni pregangliari iniziano nel nucleo motore
dorsale del vago e arrivano al SEI. Tali neuroni colinergici sono eccitatori e
stimolano neuroni eccitatori (muscarinici), o inibitori (NANC), che controllano
il tono del SEI. Questi neuroni NANC rilasciano NO, che causa il rilasciamento
del SEI. I rilasciamenti possono essere anche transitori e indipendenti dalla
deglutizione e durano generalmente più a lungo dei rilasciamenti post-
deglutitori. I rilasciamenti transitori facilitano il passaggio retrogrado dell’aria
intragastrica e quindi l’eruttazione e sono causati soprattutto dalla distensione
del fondo gastrico.
La pressione del SEI è altresì influenzata da fattori diversi. Difatti essa aumenta
considerevolmente in risposta ad un pasto proteico, da vari ormoni (gastrina,
motilina, Sostanza P), da alcuni farmaci (metoclopramide, domperidone), mentre

16
è diminuita da un pasto prettamente lipidico, dalla cioccolata, dall’alcol, da
ormoni (colecistochinina, glucagone, progesterone), da diversi farmaci
(diazepam, morfina, calcio antagonisti, nitrati).

17
AUMENTO DIMINUZIONE
AGENTI
ORMONALI
Gastrina
Motilina
Sostanza P
Somatostatina
Secretina
Colecistochinina
Peptide
intestinale
vasoattvo
Progesterone
AGENTI
NERVOSI
Agonisti-alpha-
adrenergici
Antagonisti-beta-
adrenergici
Agonisti
colinergici
Agonisti-beta-
adrenergici
Antagonisti-
alpha-
adrenergici
Antagonisti
colinergici
CIBI Pasti proteici Grassi
Cioccolato
Etanolo
Menta piperita
ALTRI Istamina
Antiacidi
Metoclopramide
Caffè
Complesso
motorio migrante
Aumento
pressione
addominale
Ossido nitrico
Teofillina
Caffeina
Acido
Fumo
Gravidanza
Morfina
Dopamina
Calcio
antagonisti
Diazepam

18
CCAAPPIITTOOLLOO IIII
FFIISSIIOOPPAATTOOLLOOGGIIAA DDEELLLLAA MMAALLAATTTTIIAA DDAA
RREEFFLLUUSSSSOO GGAASSTTRROOEESSOOFFAAGGEEOO
Grazie al monitoraggio ph-metrico computerizzato delle 24 o 36h, è chiaramente
dimostrato che ogni individuo presenta saltuari episodi di reflusso di materiale
gastrico in esofago, soprattutto in seguito ai pasti e in posizione clinostatica. Un
reflusso acido è considerato fisiologica quando il numero, nelle 24h, risulti
essere inferiore a 50 episodi, e il tempo totale di contatto del materiale refluito è
inferiore al 4.2 per cento del tempo di monitorizzazione e quando i reflussi di
durata superiore ai 5 minuti siano, sempre nelle 24 h, meno di 3.
Al di sopra tali parametri, il reflusso diviene patologico, alterando la funzionalità
e l’integrità anatomica della giunzione gastro-esofagea da cui dipende il
mantenimento dell’equilibrio tra agenti lesivi e difensivi dell’epitelio esofageo.
La prima linea di difesa che controlla la quantità e la frequenza dei reflussi è
rappresentata dalla Barriera Anti-Reflusso.
La barriera primaria è rappresentata dallo sfintere esofageo inferiore (SEI), che
separa la pressione negativa intraesofagea, da quella positiva intragastrica.
Episodi di reflusso potenzialmente lesivi si verificano per diverse variabili:
- ogni qual volta che lo sfintere diviene incompetente ( pressione inferiore ai 5
mmHg );

19
- per gli imprevedibili rilasciamenti di uno sfintere normotonico (pressione
superiore ai 10-12mmHg);
-per aumento della pressione intragastrica in pz con sfintere ipotonico (pressione
tra i 5-10 mmHg);
-per insufficiente adattamento del LES.
Barriere secondarie nella prevenzione del reflusso gastro-esofageo sono: la
membrana freno-esofagea, l’Angolo di His, l’esofago intra-addominale, le
rosette mucose, il meccanismo di chiusura per stiramento delle fibre elicoidali
dell’esofago poste tra la muscolatura longitudinale e quella circolare del pilastro
diaframmatico.
I fattori condizionanti la capacità erosiva del materiale refluito sono
rappresentati da:
Composizione del contenuto gastrico ( acido, pepsina, succo duodenale)
Tempo di svuotamento gastrico
E’ indubbio che un’alterazione dello svuotamento gastrico, per lo squilibrio della
pompa antro-pilorica, condizioni l’entità del reflusso, sia per un aumento della
pressione endo-gastrica, sia per un aumento del volume del materiale refluito.
L’entità della forza offensiva è determinata dalle caratteristiche del materiale
refluito. Il maggior agente lesivo per la mucosa esofagea è indubbiamente
rappresentato dall’associazione di acido cloridrico e di Sali biliari, più dannosi
dei singoli componenti.

20
I meccanismi di difesa da parte dell’esofago sono rappresentati dalla:
-capacità di “clearing esofago-gastrica”
-resistenza epiteliale
La capacità di clearing esofageo rappresenta il principale meccanismo di difesa
sostenuto principalmente dalla sua funzione motoria. Infatti la presenza di
materiale refluito è in grado di iniziare un’onda peristaltica secondaria insorta
per stimolazione locale capace di rimuovere il materiale refluito, limitando il
tempo di contatto con la mucosa esofagea.
Altro fattore è rappresentato dalla secrezione salivare che, esercitando una
diluizione e neutralizzazione del materiale refluito, riporta a valori di pH
fisiologico il contenuto dell’esofago terminale. Poiché durante il sonno la
peristalsi e la salivazione sono meno efficaci, si spiega come proprio durante il
periodo notturno, il reflusso arrechi i danni maggiori all’epitelio esofageo. La
mancanza di anche uno dei meccanismi, causata da malattia ( ad ex:
sclerodermia, farmaci, anticolinergici, varici, neoplasie…), è in grado di
aggravare il reflusso.
L’altro meccanismo di difesa è rappresentato dalla resistenza epiteliale deputata
alla prevenzione e riduzione dei danni epiteliali conseguenti al contatto con gli
agenti lesivi contenuti nel materiale refluito. Essa esprime in modo unitario
l’azione di diversi fattori, quali la secrezione mucosa dell’esofago distale, le
membrane cellulari, le strutture giunzionali intercellulari, i processi di trasporto
ionico, il flusso ematico e lo stato acquoso quieto.

21
Lo strato mucoso evita la diffusione intracellulare, e contribuisce alla
formazione dello strato acquoso quieto, il quale rappresenta una zona di bassa
turbolenza adiacente alle superfici cellulari ed in grado di intrappolare ioni
bicarbonati. Le barriere strutturali, rappresentate dalle membrane cellulari e dai
sistemi giunzionali, limitano la penetrazione( ionica o molecolare), e sono vitali
per il corretto funzionamento dei sistemi di trasporto. Di questi ultimi, due in
particolare proteggono l’epitelio dall’acidità: lo scambio Sodio-Idrogeno a
livello della membrana apicale, e lo scambio cloro-bicarbonato delle membrane
baso-laterali. Questi meccanismi contribuiscono al mantenimento del pH
intracellulare, espellendo dalla cellula gli ioni idrogeno ( scambio sodio-
idrogenioni ), o potenziando i sistemi tamponi intracellulari ( scambio cloro-
bicarbonato). Un adeguato flusso ematico è quindi importante a scopo protettivo,
in quanto fornisce ossigeno, nutrienti e tamponi ai tessuti e rimuove gli
idrogenioni e gli altri metaboliti potenzialmente lesivi.
Altro fattore patogenetico di particolare importanza è l’ernia iatale da
scivolamento, il cui ruolo nel determinismo della MRGE è piuttosto controverso.
Infatti, sebbene l’ernia iatale sia un reperto comune ( circa il 50% della
popolazione >50 anni), e la maggior parte dei pazienti con ernia iatale non abbia
MRGE, l’esofagite è spesso associata ad ernia, suggerendo un ruolo
patogenetico di quest’ultima nell’insorgenza dell’esofagite. Poco chiaro è il
meccanismo mediante cui l’ernia iatale determinerebbe la MRGE. Si ritiene che
l’ernia causi un’alterazione tra sfintere crurale e SEI, cui si assocerebbe un

22
prolungamento del transito esofageo, con intrappolamento di parte del contenuto
esofageo all’interno dell’ernia e reflusso dello stesso in esofago durante i
rilasciamenti transitori del SEI.
L’ERNIA IATALE
La maggior parte delle ernie iatali dell’adulto è acquisita. Nel 1951 Allison ne
propose la loro classificazione in base alle caratteristiche anatomiche e
fisiopatologiche delle ernie da scivolamento (tipo I), caratterizzate dalla
migrazione prossimale della giunzione Esofago-Gastrica nel mediastino
posteriore, ed in ernie Paraesofagee o da rotazione (tipo II),caratterizzate dalla
dislocazione craniale del fondo gastrico a lato della Giunzione Esofago-Gastrica
normalmente posizionata.
I due tipi possono presentarsi anche in una forma combinata col risultato di un
ernia di tipo misto (tipo III), caratterizzata da una dislocazione craniale sia del
cardias che del fondo gastrico. In realtà più del 90% delle ernie cosiddette
“paraesofagee” sono di tipo misto.
Ernia Da Scivolamento
Questo tipo di ernia costituisce il 90-95% delle ernie iatali. La loro presenza è
spesso intermittente, sono in parte o del tutto riconducibili ed evocabili con i
cambiamenti di postura o all’aumentare della pressione endoaddominale.
Diversi Autori ritengono che possa esservi una meiopragia congentia dello iatus
e dei mezzi di fissazione freno-esofagei, che rimane per lo più inoperante,

23
fintanto che altri cofattori quali l’obesità (aumento della pressione
endoaddominale), il rapido dimagrimento (rarefazione delle cellule del
mesoesofago), l’età senile (per la riduzione del tono e dell’elasticità
diaframmatica), deformazioni della colonna lombo dorsale (alterazione dei
pilastri diaframmatici e della trazione esercitata sul giunto, appiattimento della
cupola diaframmatica, con conseguente aumento della pressione
endoaddominale), non intervengano a ridurre la validità dei mezzi di
contenzione dello stomaco in addome.
Le strutture fasciali cardio-diaframmatiche dell’esofago e le riflessioni cardiali
del peritoneo risultano allungate mentre lo iatus appare allargato. Tali alterazioni
anatomiche sembrano legate da una parte ad una lassità congenita di questi
tessuti, dall’altra ad uno stiramento progressivo dei medesimi causato dalla
risalita del cardias in mediastino. Nella sua progressione il cardias dilata lo iatus
e induce un accorciamento dell’esofago, che risulta reversibile quando è legato
ad una retrazione delle fibre longitudinali muscolari ed elastiche dello stesso,
irreversibile quando si sovrappongono fenomeni infiammatori cronici ad
evoluzione sclerocicatriziale. Nella sua migrazione il cardias trascina anche il
peritoneo, che a questo livello è presente solo anteriormente e lateralmente allo
stomaco; formando così un sacco erniario che risulta incompleto, essendo situato
solo sul davanti e sui lati del viscere erniato.

24
Ernia Paraesofagea
La maggioranza delle ernie paraesofagee sono il risultato finale di una ernia da
scivolamento.
Un’ ernia paraesofagea pura, piuttosto che un’ernia iatale da scivolamento, si
sviluppa quando è un difetto, almeno in parte congenito, dello iato esofageo,
anteriormente all’esofago stesso. Col tempo si ha una degenerazione strutturale
della membrana freno-esofagea con assottigliamento dello strato fasciale
superiore di essa (continuazione sovra-diaframmatica della fascia endotoracica ),
e perdita di elasticità dello strato fasciale inferiore ( continuazione sotto
diaframmatica della fascia trasversalis ).
Lo strato fasciale superiore è formato solo da connettivo lasso ed ha una minore
importanza. Lo strato fasciale inferiore è più spesso e robusto, e si divide esso
stesso in due foglietti, superiore ed inferiore, circa un centimetro prima di
fondersi intimamente con l’avventizia esofagea. L’inserzione del foglietto
inferiore dello strato inferiore protrude verso l’alto e può essere spesso
identificato nel corso di una toracotomia. Questi dati anatomici suggeriscono che
lo sviluppo di un’ernia paraesofagea sia un fenomeno ampiamente correlato
all’età, ed è secondario allo stiramento verso l’alto della membrana freno-
esofagea durante i movimenti cranio-caudali dell’esofago che si ripetono nel
corso della deglutizione e alla notevole spinta verso l’alto prodotta dalla
pressione intraddominale. L’unica differenza essenziale nella genesi di un’ernia
paraesofagea da un’ernia da scivolamento è il risparmio della fissazione

25
posteriore del cardias alla fascia preaortica al legamento arcuato mediano.
Attraverso un deterioramento in più stadi di queste strutture chiave si costituisce
un difetto anteriore dello iato e si sviluppa un’ernia mista (tipo III). Le ernie
paraesofagee sono comunemente associate ad una rotazione di 180° dello
stomaco attorno al suo asse longitudinale che porta ad una modificazione
dell’orientamento della parete anteriore e posteriore del corpo gastrico.
Patogenesi della MRGE
a) Forma idiopatica
b) Forme secondarie:
Obesità
Malattie endocrino-metabolich (Diabete-Mellito; Ipotiroidismo)
Collagenopatie (Sclerodermia; LES)
Neuropatie Viscerali
Neuropatie Sistemiche
Malattie dell’Apparato Respiratorio (Asma)
Stati Ipersecretivi (Sindrome di Zollinger-Ellison)
Interventi chirurgici
Farmaci
Gravidanza

26
CCAAPPIITTOOLLOO IIIIII
PPRREESSEENNTTAAZZIIOONNEE CCLLIINNIICCAA
La malattia da Reflusso Gastro-Esofageo si estrinseca clinicamente attraverso
sintomi e modalità di presentazione molto diversi tra loro; peraltro è possibile
anche un reflusso asintomatico, diagnosticato in genere a posteriori dopo il
brusco esordio di una esofagite complicata. Mentre alcuni sintomi, come la
pirosi ed il rigurgito, inducono paziente e medico a sospettare la presenza di un
reflusso, altri, come il dolore toracico o la tosse, sono indubbiamente più
generici, essendo attribuibili anche a numerose altre condizioni cliniche. Sorge
allora la necessità di quantificare il peso clinico che differenti sintomi, sia
singolarmente che in associazione tra loro, possono avere sia nell’approccio
diagnostico alla malattia da reflusso che nel riconoscimento di altre patologie.
SINTOMI TIPICI
PIROSI
E’ indubbiamente il sintomo più frequente in presenza di malattia da reflusso,
ma solo il 50% dei pazienti ne riferisce la presenza. Inoltre, è un sintomo
comune nella popolazione generale e pertanto la sua specificità è bassa. Viene
descritto come sensazione di bruciore, spesso dolorosa, a volte intollerabile, che
si irradia in genere in sede retro sternale propagandosi, dalla sua porzione

27
xifoidea, verso l’alto, verso il giugulo; a volte raggiunge la gola e la bocca ed in
questi casi è frequente l’associazione con un rigurgito di materiale liquido,
acidulo o amarognolo. In genere si presenta in fase postprandiale, a volte
soltanto in seguito a pasti copiosi, verosimilmente per una eccessiva distensione
gastrica, ma più spesso dopo i pasti regolari. Può comparire anche in
conseguenza di movimenti che aumentino la pressione intra-addominale (colpi
di tosse, Manovra di Valsalva, flessione anteriore del busto).
RIGURGITO
Il termine rigurgito indica la percezione di flusso spontaneo o provocato del
contenuto gastrico all’esofago e all’orofaringe, che si produce in assenza dei
fenomeni muscolari estrinseci del vomito. Frequentemente compare in
clinostatismo e durante l’antiflessione del corpo. Non è di regola accompagnato
da nausea, conati, né contrazioni addominali.
SINTOMI ATIPICI
DISFAGIA
E’ un sintomo molto frequente fra i pazienti con malattia da reflusso e consiste
nella sensazione di un rallentamento o di un completo arresto del cibo durante il
transito verso lo stomaco. Alla sua genesi possono contribuire sia disordini

28
funzionali che danni anatomici. Questi ultimi sono rappresentati da stenosi
peptiche, anelli della porzione inferiore dell’esofago e dai carcinomi.
ODINOFAGIA
In corso di malattia da reflusso il dolore alla deglutizione non è particolarmente
frequente; la sua comparsa deve essere però considerata con molta attenzione
dato che essa può essere dovuta ad una disfunzione motoria, ma anche ad una
complicanza severa, quale una neoplasia.
DOLORE TORACICO
Circa il 20-30% di pazienti con dolore anginoso più o meno tipico hanno una
coronarografia normale e per loro viene posta diagnosi di dolore toracico da
causa non precisata. In realtà si tratta verosimilmente di reflusso (causa più
frequente di dolore toracico nei soggetto con coronarografia negativa).
Bisogna,inoltre, tenere sempre presente che la malattia da reflusso può coesistere
con quella coronarica.
Altri sintomi minori, con i quali a volte esordisce il quadro clinico, sono la
scialorrea e la raucedine.
I soggetti con reflusso gastro esofageo hanno un elevato rischio di andare
incontro a manifestazioni cliniche coinvolgenti altri organi od apparati, con un
livello di gravità molto variabile, ma che in alcuni casi può essere tale da

29
condurre all’exitus. Le manifestazioni più comuni sono: l’asma, la polmonite ab
ingestis, la laringite cronica, la raucedine, la tosse cronica.
SINTOMI EXTRA-ESOFAGEI
SERIOUS SLEEP DISTURBANCES
Pazienti con MRGE riferiscono risvegli frequenti durante il riposo notturno o
presentano difficoltà nell’addormentamento a causa della loro sintomatologia. I
sintomi peggiorano in decubito supino.Pazienti con MRGE riferiscono risvegli
frequenti durante il riposo notturno o presentano difficoltà
nell’addormentamento a causa della loro sintomatologia.
Sintomi dell’Apparato Respiratorio (Tosse cronica, Asma)
La patogenesi delle manifestazioni respiratorie è complessa. Due ipotesi sono
state chiamate in causa per spiegare l’insorgenza di sintomi respiratori nei
pazienti con MRGE:
a) Microaspirazione di contenuto gastrico che, refluito nel laringe, passa
all’interno dei bronchi dove causa un danno alle mucose per effetto dell’azione
lesiva dell’acido o degli enzimi;
b) Broncospasmo mediato da un riflesso neuronale attivato dall’esposizione
della mucosa esofagea all’acido.
Va anche tenuto presente che nel paziente asmatico, l’asma stessa, in virtù del
gioco delle variazioni delle pressioni endo-toraciche, endo-addominali e

30
dell’attività diaframmatica, può per sé scatenare un episodio di reflusso che a sua
volta contribuisce al broncospasmo. Un origine prettamente esofagea dell’asma
va sospettata nel paziente con sintomatologia prettamente notturna.
La tosse cronica, definita come tosse persistente da oltre 8 settimane, è causata
da MRGE nel 20% dei casi. [ 25;26 ]
Criteri per associare la Tosse cronica alla MRGE:
a) Tosse cronica >8 settimane
b) Pz non sottoposto a terapia con ACE-Inibitori
c) Pz non fumatore nè esposto a antigeni ambientali irritativi
d) Rx torace negativa
e) Esclusione (in seguito di appropriati accertamenti diagnostici), di:
Asma Allergica, Bronchite Eosinofila, Rinite Allergica
Altre manifestazioni polmonari associate a MRGE (di riscontro
occosionale):
a) Fibrosi Polmonare Idiopatica
b) Bronchite Cronica

31
c) Broncopneumopatia Cronica Ostruttiva (BPCO)
d) Polmonite ab ingestis
e) Ascesso Polmonare
f) Bronchiectasie
Sintomi Otorinolaringoiatrici ( Otalgia, Disfonia, Raucedine)
I sintomi orofaringei risultano essere più frequenti di quanto si ritenga
comunemente, tanto che circa il 25% dei pazienti con MRGE riferisce soltanto
questo tipo di sintomatologia. [26]
Manifestazioni laringee della MRGE
Laringite cronica
Ulcere e granulomi delle corde vocali
Bisogno frequente di “schiarirsi la voce”
Manifestazioni orofagingee della MRGE
Raucedine Scialorrea
Dolenzia Cervicale Globo Faringeo

32
Lesioni Dentarie Otite Media
Odinodinia

33
CCAAPPIITTOOLLOO IIVV
CCOOMMPPLLIICCAANNZZEE
Le complicanze che si possono osservare sono:
a) Stenosi peptiche: tipiche dei pazienti anziani, sono la complicanza più
frequente della MRGE con esofagite e rappresentano circa l’80% delle stenosi
esofagee benigne. La presenza di stenosi si correla abbastanza bene con la durata
dell’esofagite e la severità del reflusso acido-obiettivabile con la pH-metria. La
stenosi peptica si forma per la sostituzione del tessuto muscolare delle pareti
esofagee con tessuto fibroso non distendibile e il sintomo più comune che ne
deriva è la disfagia da ostacolo meccanico e funzionale dal passaggio del bolo;
b) Emorragia: in presenza di esofagite è frequente il riscontro di anemie
sideropeniche dovute allo stillicidio cronico di sangue che la condizione
patologica comporta. Emorragie massive che necessitano di trattamento
endoscopicoe/o chirurgico sono invece più rare, interessando circa il 2% dei
pazienti con esofagite. L’ipotesi patogenetica dell’emorragia in corso di
esofagite è quella dell’assottigliamento della tonaca mucosa indotto dal reflusso
acido con erosione del plesso vascolare contenuto nelle protuberanze papillari.
In presenza di un’ulcerazione, inoltre, possono essere compromessi vasi di
maggior calibro, con maggior probabilità di sanguinamento importante. E’

34
comunque raro che le emorragie peptiche siano di maggior gravità dei
sanguinamenti gastroduodenali.
c) L’esofago di Barrett: è un disordine caratterizzato da una sostituzione
del normale epitelio squamoso pluristratificato dell’esofago distale con un
epitelio metaplastico di tipo colonnare. Questa metaplasia rappresenta una
condizione di rischio per lo sviluppo di displasia e conseguentemente di
adenocarcinoma dell’esofago distale e della giunzione esofago gastrica.
Si definisce Long-Barrett il segmento metaplastico la cui estensione, a partire
della Sfintere Esofageo Inferiore è >3 cm; in caso di estensione <3 cm, si parla
di Short-Barrett. Al di sotto del centimetro di estensione, si definisce Ultrashort-
Barrett o Barrett giunzionale.
La prevalenza dell’esofago di Barrett è stimata intorno al 3-7% in pazienti che si
sottopongono ad esame endoscopico a causa di frequenti sintomi da reflusso;
d) Adenocarcinoma esofageo e della giunzione esofago-gastrica:
numerosi studi in letteratura documentano che il reflusso gastro esofageo ne
rappresenta uno dei maggiori fattori di rischio. Il rischio neoplastico incrementa
in maniera direttamente proporzionale con la durata e la severità dei reflusso: la
possibilità di sviluppare canro sarebbe stimata circa 8 volte maggiore in soggetti
con storia clinica di reflusso superiore ai 5 anni e frequenza di pirosi e/o
rigurgito settimanale. Inoltre il reflusso, se associato ad ernia iatale, esofagite e/o

35
ulcera esofagea e disfagia determina un ulteriore incremento del rischio da 2 a 4
volte.
Studi in vitro hanno investigato la patogenesi del danno diretto da reflusso acido.
In particolare è stato dimostrato che nel breve intervallo di tre minuti, dopo
un’esposizione acida intermittente, le cellule esofagee mostrano l’attivazione di
meccanismi proliferativi e anti-apoptotici; [27]

36
CCAAPPIITTOOLLOO VV
DDIIAAGGNNOOSSTTIICCAA CCLLIINNIICCAA--SSTTRRUUMMEENNTTAALLEE DDEELL
RREEFFLLUUSSSSOO GGAASSTTRROO--EESSOOFFAAGGEEOO
Manometria esofagea
La manometria esofagea, introdotta da oltre un secolo ha consentito negli ultimi
30 anni, soprattutto dopo l’introduzione della pompa d’infusione a bassa
compliance, del sensore “a manicotto” per le aree sfinteriali e dei trasduttori
intraluminali con possibilità di registrazione per 24 ore, un considerevole
progresso delle cognizioni della fisiopatologia della motilità esofagea.
La Manometria Esofagea viene eseguita per studiare la fisiopatologia esofagea
attraverso la valutazione della pressione intraesofagea nei vari settori del suo
lume.
Tale esame pernette la valutazione dei quadri clinici di disfagia, di reflusso
gastro-esofageo (GERD/MRGE) o di altre patologie delle vie
gastroenterologiche superiori.
L'esame dura circa 30-40 minuti, e viene svolto solitamente in modalità
ambulatoriale. Non è possibile eseguire sedazione (ad es., con benzodiazepine),

37
perché, oltre ad essere necessaria la collaborazione del paziente durante tutto
l'esame, l'effetto miorilassante della sedazione interferirebbe con la motilità
esofagea che è l'oggetto di studio.
Il paziente, a digiuno, riceve una blanda anestesia topica nelle coane nasali,
attraverso la quale viene inserito delicatamente un sottilissimo catetere, che
viene spinto in rinofaringe e quindi in orofaringe. A questo punto, il catetere
viene sospinto in esofago attraverso lo sfintere esofageo superiore (SES); il
passaggio, che nella maggior parte dei casi crea un certo fastidio (conati dovuti
ai riflessi ipofaringei), viene spesso facilitato attraverso la suzione di piccoli
sorsi d'acqua tramite una cannuccia. Una volta entrato il catetere in esofago, il
fastidio diminuisce notevolmente. Il catetere viene fatto scendere fino allo
sfintere esofageo inferiore (SEI), e poi ritratto leggermente fino a identificare il
punto di variazione della pressione intraesofagea (linea Z). A questo punto il
paziente viene fatto stendere su un lettino, ed inizia la valutazione. Attraverso le
rilevazioni del catetere, continuamente registrate da un computer, vengono
valutate le anomalie motorie e pressorie, la propagazione delle onde di peristalsi,
etc. La valutazione viene effettuata facendo eseguire al paziente una serie di
deglutizioni secche (a vuoto), o umide (piccoli sorsi d'acqua, assunti tramite una
cannuccia), che permettono lo studio dettagliato delle varie fasi della motilità di
tutti i settori esofagei. Al termine dell'esame il paziente viene fatto sedere ed il
catetere estratto delicatamente. A questo punto il paziente può riprendere la sua
normale attività lavorativa, senza alcun problema. Nelle ore seguenti può

38
occasionalmente manifestarsi una leggera congestione nasale, o una leggerissima
algia faringea di breve durata.
INDICAZIONI:
Pazienti con disfagia, dopo aver escluso l'esistenza di patologia organica
e per formulare diagnosi di patologia motoria esofagea (acalasia, SED etc.).
Pazienti con dolore toracico, dopo aver escluso l'origine cardiopolmonare e
dopo aver effettuato indagini morfologiche esofago-gastriche (Rx, endoscopia).
Pazienti con malattie sistemiche (es. collagenopatie) in cui si voglia
stabilire l'esistenza di un interessamento esofageo (patologia multiorgano).
Pazienti con GERD, come completamento delle indagini in previsione
dell'intervento chirurgico antireflusso.
Pazienti in cui è necessario posizionare un catetere intraesofageo (es. sonda
pH-metrica) che necessiti di una precisa allocazione rispetto alle aree sfinteriali.
CONTROINDICAZIONI
Assolute:
Stenosi od ostruzione della faringe o dell'esofago superiore.
Patologie cardiache in cui sia controindicata una stimolazione vagale.
Coagulopatie gravi e non controllate.
Non compliance del paziente.
Relative:
Tumori o ulcere dell'esofago.

39
Grosse varici esofagee.
Grossi diverticoli esofagei o crico-faringei.
pH-METRIA ESOFAGEA DELLE 24 ORE
La pH-metria ambulatoriale, introdotta da quasi 30 anni per la diagnostica della
MRGE in analogia alla registrazione prolungata dell’ECG è risultata di grande
importanza soprattutto nell’individuare le forme con sintomi atipici e nel
verificare l’efficacia della terapia. Un incremento dell’accuratezza si è ottenuto
con l’utilizzo di più elettrodi (ad es., l’area sotto la curva e la correlazione con i
sintomi).
La MRGE ha sempre destato molto interesse fra i patologi e i fisiopatologi.
Usufruendo delle nozioni di base derivanti dagli studi fisiologici, Spencer
descrisse nel 1969 la tecnica di registrazione prolungata del pH esofageo. Nel
1974 Johnson e De Meester studiarono volontari sani registrando per 24 ore il
pH endoesofageo. Questi primi studi hanno introdotto il concetto fondamentale
di "reflusso fisiologico", cioè presente normalmente negli individui sani,
stabilendo il limite "soglia" alla diagnostica della MRGE. La pHmetria delle 24
ore ha quindi dato al Clinico lo strumento essenziale alla diagnosi della MRGE.
È universalmente accettato che il danno alla mucosa esofagea si realizza tutte le
volte che il pH esofageo scende a valori inferiori a 4.

40
Il punteggio di De Meester è la metodica d'interpretazione dei dati pHmetrici
maggiormente utilizzata fino ad oggi. Questa si basa sulle sei classiche variabili
esofagee, e cioè:
la percentuale di tempo totale di reflusso a pH < 4 (T.T.R.).
il numero di reflussi sotto la soglia di pH 4.
la durata del reflusso più lungo.
il numero dei reflussi < 4 con durata superiore a cinque minuti.
la percentuale di tempo in posizione supina con pH < 4.
La percentuale di tempo in posizione eretta con pH < 4.
Il punteggio viene valutato con una formula che dipende dalle deviazioni
standard di ognuna di queste variabili per ogni valore normale (Johnson-
DeMeester); i valori di riferimento usati da De Meester sono stati ricavati da
persone adulte asintomatiche. Questo punteggio risulta superiore a 18 nei
pazienti con MRGE. Le maggiori obiezioni che vengono mosse allo score di De
Meester consistono nel fatto che questo punteggio manca di relazione con la
prognosi e con il grado di esofagite. Sono stati perciò ricercati dei parametri che
non esprimessero esclusivamente la durata del tempo di esposizione acida
dell'esofago, ma che ci informassero anche sul valore di pH raggiunto
nell'esofago: si sono cercati cioè, dei valori bidimensionali indice di durata e
profondità dell'insulto acido. Questi nuovi parametri sono rappresentati dal:

41
integrale di pH;
integrale di H+
la percentuale dei reflussi brevi;
la pendenza media di rientro;
la permanenza percentuale in zone di pH.
Tra questi parametri l'integrale di pH < 4, il così detto A.U.C. (Area Sotto la
Curva) è quello più studiato in quanto sembra avere una correlazione diretta con
la presenza di esofagite nel senso che un elevato valore di A.U.C. si ritrova nei
pazienti reflussori con esofagite, al contrario i pazienti con un elevato T.T.R. non
sempre hanno un'elevata incidenza di esofagite. La percentuale dei reflussi brevi
e la pendenza di rientro sono dei parametri che ci danno delle indicazioni sulla
capacità di clearance dell'esofago, una percentuale di reflusso breve superiore al
60% è indice di una buona clearance.
LA DIAGNOSTICA PER IMMAGINI NELLO STUDIO
DELL’ESOFAGO
L’esofago è per lo più oggetto di studio radiologico “mirato” solo allorquando la
sintomatologia clinica del paziente (disfagia, bruciori, dolore retro sternale), induce
a rivolgergli primitivamente l’attenzione. Di norma, però, è oggetto di studio “di
passaggio” nel contesto di indagini volte a patologie gastriche o duodenali. Anche
in questo caso, comunque, è buona norma non sottovalutare quest’organo, nel

42
quale la presenza di patologie più o meno gravi, possono, ad uno stadio iniziale,
non essere accompagnate da sintomi se non in fase avanzata.
Lo studio dell’esofago a fini morfologici può essere realizzato mediante Rx
Esofago con Bario.
RX ESOFAGOGRAMMA IN TRENDELENBURG
Nelle esofagiti medie e severe è ricco di segni indicativi. Difatti mostra:
Ridotta distensibilità dell’esofago;
Ispessimento delle pliche longitudinali (indicative di flogosi della mucosa, di
edema sottomucoso);
Scomparsa dell’aspetto liscio della superficie mucosa;
Aspetto granulare della mucosa, sollevata a mò di pomfo ( indicativo di edema,
flogosi);
Presenza di essudato infiammatorio che tende a rapprendersi in vere e proprie
pseudomembrane, talora di grandi dimensioni;
Erosioni ed ulcere piatte multiple, a chiazza o a strie serpiginose;
Ulcere vere e proprie (cratere ulceroso profondo), in cui il processo ulcerativo si
diffonde in maniera continua;
Reflusso del mezzo di contrasto, eseguendo l’esame in posizione Trendelenburg.
Modalità di esecuzione dell’esame:

43
Il paziente, digiuno, eventualmente medicato con ipotonizzanti , inizialmente in
stazione eretta, viene invitato a ingerire, con l’aiuto di 5-10 ml di acqua, una
dose di polveri effervescenti. Il gas distende il lume esofageo. Si fanno quindi
ingerire rapidamente 50-100 ml di soluzione di solfato di Bario a elevata
concentrazione e bassa viscosità, sì da indurre un vernicia mento a strato sottile e
uniforme della mucosa esofagea. Si assumono quindi radiogrammi mirati nelle
proiezioni oblique (onde dissociare proiettivamente l’esofago dalla colonna
vertebrale e dal cuore).
Questo esame risulta essere fondamentale anche per lo studio funzionale della
giunzione esofago-gastrica. Difatti, eseguendo l’Rx in posizione Trendelenburg
possono mostrare il reflusso del mezzo di contrasto dallo stomaco all’esofago.

44

45
L’ENDOSCOPIA DIGESTIVA
L’endoscopia digestiva è stata sperimentata per oltre 200 anni, ma solamente
l’introduzione, nella metà del ventesimo secolo, dei gastroscopi semirigidi ha
segnato l’inizio della moderna era endoscopica. Da allora enormi passi avanti
nella tecnologia endoscopica hanno portato a radicali cambiamenti nella
diagnosi e nel trattamento di molte patologie del tratto gastroenterico. Innovativi
strumenti endoscopici e nuove modalità di trattamento continuano ad ampliare il
campo di applicazione dell’endoscopia nella cura del paziente.
Gli endoscopi flessibili forniscono o un’immagine ottica (trasmessa attraverso
fasci di fibre ottiche), o un’immagine video-elettronica (prodotta da un congegno
miniaturizzato posto sulla punta dell’endoscopio). I controlli dell’operatore
permettono la deflessione dell’estremità dell’endoscopio; i fasci di fibre ottiche
portano la luce alla punta dell’endoscopio e i canali laterali di servizio
permettono il lavaggio, la suzione e l’introduzione di vari strumenti operativi.
Progressivi cambiamenti nel diametro e nella rigidità degli endoscopi hanno
migliorato la tolleranza dei pazienti all’endoscopia.

46
EsofagoGastroDuodenoscopia (EGDS)
L’endoscopia con strumento flessibile ha largamente sostituito l’esofagoscopia
con tubo rigido, poiché essa fornisce una migliore visualizzazione, è meno lesiva
e permette un concomitante esame dello stomaco. Con
l’EsofagoGastroDuodenoscopia si fa passare l’endoscopio flessibile, attraverso
la bocca, nell’esofago, nello stomaco e nel bulbo duodenale. A livello gastrico,
eseguendo la manovra di retroversione è possibile ispezionare l’orifizio cardiale
che non è accessibile all’endoscopio rigido. Quest’ultimo è ancora utilizzato nei
seguenti casi:
rimozione di corpi estranei;
necessità di ottenere prelievi bioptici di grosse dimensioni quando non sia
possibile definire una diagnosi istologica sulla base di biopsie più minute e più
superficiali di quelle ottenute con la tecnica a fibre ottiche.
L’esofagogastroduodenoscopia deve essere proposta in tutti i pazienti che
presentino disfagia o altri sintomi specifici.
Essa fornisce utili informazioni nei casi di esofagite, indicandone la gravità o la
presenza di complicanze, e ne permette una classificazione in stadi, evenienza
possibile solo grazie alla visualizzazione diretta della mucosa esofagea (che solo
l’esame endoscopico è in grado di fornire). È inoltre di fondamentale importanza
nell’identificazione di neoplasie esofagee. Ma soprattutto, l’endoscopia permette
di eseguire biopsie, che sono strettamente necessarie nei seguenti casi:

47
per dimostrare alterazioni istologiche caratteristiche o suggestive di esofagite
in pazienti sintomatici ed in cui l’aspetto macroscopico della mucosa sia solo
lievemente alterato o addirittura normale;
per differenziare l’origine peptica o neoplastica di una lesione sospetta, come
un’ulcera o una stenosi;
per diagnosticare con certezza una metaplasia di Barrett.
È importante sottolineare che il riconoscimento di quest’ultima condizione
imporrà di seguire nel tempo il paziente con controlli endoscopici ed istologici,
al fine di sorprendere precocemente un’eventuale trasformazione neoplastica o
alterazioni istologiche di significato francamente precanceroso come la
displasia.
L’endoscopia va sempre eseguita anche nei casi di disturbi motori
apparentemente solo funzionali per accertare che la discinesia non sia, come può
accadere, un epifenomeno di una neoplasia radiologicamente occulta. Essa è,
inoltre, di particolare utilità dopo interventi chirurgici, quando il reperto
radiologico è spesso di difficile interpretazione.

48
CCAAPPIITTOOLLOO VVII
TTEERRAAPPIIAA
Gli scopi della terapia medica della MRGE sono i seguenti:
a) alleviare i sintomi;
b) favorire la cicatrizzazione delle lesioni esofagitiche;
c) prevenire le complicanze;
d) modificare la storia naturale della malattia.
Alleviare i sintomi risulta essere uno punti cardine nello scopo della terapia. Uno
studio recente condotto in una popolazione di 6215 pazienti ha dimostrato che la
Quality of Life in pazienti affetti da Malattia da Reflusso Gastro-Esofageo è
paragonabile a quella dei pazienti affetti da patologie debilitanti e croniche come
quelle cardiovascolari, Diabete Mellito o Malattia Ipertensiva.
Essa consiste, in primo luogo, in misure di ordine Igienico-dietetico (VEDI
DIETA E STILE DI VITA), e, successivamente, nell’adozione di una terapia
farmacologica mirante a ridurre il reflusso acido. (VEDI TERAPIA
FARMACOLOGICA).

49
Dieta e Stile Di Vita
Innanzitutto è consigliabile raggiungere o mantenere un peso corporeo corretto
per ridurre i rischi di malattia da reflusso. È bene evitare di mangiare troppo
tardi alla sera o di fare spuntini durante la notte, perché questo può favorire il
fenomeno del reflusso di acido nelle ore notturne, quando si assume la posizione
sdraiata.
Sono da preferire gli alimenti poveri di grassi (pane, pasta, riso,
patate, verdure, frutta, carni magre, latte e yogurt scremati) mentre
vanno evitati i cibi che possono favorire il rilasciamento dello
sfintere esofageo inferiore (fritture, carni e formaggi grassi, panna,
salse e condimenti ricchi di burro) oltre a bevande alcoliche,
menta, aglio e cipolla.
È consigliabile limitare gli alimenti che possono irritare la mucosa dell'esofago:
agrumi e relativi succhi, pomodoro e succo di pomodoro, caffè, cioccolato, tè,
coca cola e bevande gassate in genere, menta piperita.
Meritano di essere ricordate alcune piccole regole igieniche, per esempio:
non sdraiarsi subito dopo il pasto ed evitare attività che comportano una
posizione prolungata di flessione in avanti (per esempio, il giardinaggio);

50
non andare a dormire prima che siano trascorse almeno due-tre ore dal pasto;
sollevare il letto di 10-15 centimetri dalla parte in cui si appoggia la testa;
evitare gli indumenti troppo stretti in vita.
Terapia medica
Caratteristiche dei farmaci maggiormente utilizzati:
Antagonisti dei recettori H2 dell’istamina
Gli antagonisti dei recettori H2 bloccano in maniera competitiva il recettore
istaminico localizzato sulla cellula parietale( alla cui attivazione segue l’aumento
delle concentrazioni intracellulari dell’AMP-ciclico che porta all’attivazione
finale della Pompa Protonica), riducendo la secrezione acida basale. L’effetto è
maggiore sulla secrezione acida notturna, minore sulla secrezione stimolata dal
pasto o dall’attivazione vagale. Gli antagonisti dei recetto istaminici H2
maggiormente utilizzati nella pratica clinica per la terapia della MRGE, sono la
Cimetidina, Famotidina, Nizatidina, Ranitidina. [7]
Inibitori di Pompa Protonica (PPI)
Gli inibitori di Pompa Protonica disponibili per l’uso clinico comprendono
Omeprazolo, Lansoprazolo, Pantoprazolo, Rabeprazolo ed Esomeprazolo.
Raggiunta la mucosa gastrica attraverso la circolazione sistemica, questi farmaci
si accumulano all’interno dei canalicoli secretori delle cellule parietali dove, a
causa dell’ambiente fortemente acido, subiscono una conversione in un
composto (la sulfenamide), in grado di legare e di conseguenza bloccare la

51
pompa protonica. A questa azione fa seguito un’inibizione marcata della
secrezione acida gastrica.
Sucralfato
Il sucralfato è un polissaccaride solfato costituito da saccarosio octasolfato
complessato con Idrissido di Alluminio. Nell’ambiente acido del lume gastrico,
l’alluminio si dissocia ed il saccarosio polimerizza dando luogo alla formazione
di un gel viscoso che si deposita sul cratere ulceroso e per mezzo di forze
elettrostatiche si lega al materiale necrotico della mucosa lesa per oltre 6 ore
dalla somministrazione. Il farmaco, quindi, forma una barriera che protegge la
mucosa dall’azione aggressiva dell’HCl e dall’azione proteolitica della pepsina.
MRGE lieve
Linee guida sottolineano l’opportunità di un primo step terapeutico rappresentato
dalle modificazioni della abitudini alimentari e dello stile di vita che, sebbene
non supportati da evidenze sulla loro reale efficacia, vengono sempre
raccomandate lungo tutto il percorso terapeutico della MRGE.
L’uso di antiacidi/arginati o antagonisti dei recettori H2 dell’istamina (anti-H2-
R) sta oggi perdendo significato anche nelle forme lievi, data la disponibilità di
farmaci più efficaci (IPP) e, almeno per quanto riguarda la realtà italiana, anche

52
a costo ridotto. Diversi studi, difatti, hanno evidenziato un netto miglioramento
della sintomatologia.
MRGE severa o sintomi di allarme
Pazienti con esofagite (ERD). Gli IPP sono i farmaci di prima scelta. Una
review sistematica di 11 RCT sul trattamento empirico dimostra che, sebbene la
terapia con IPP e con anti-H2-R a breve termine (1-12 settimane) sia efficace nel
controllo dei sintomi tipici, gli IPP si sono dimostrati superiori agli anti-H2-R . Il
tasso di guarigione a 4 settimane è superiore per omeprazolo 20 mg/die e 40
mg/die , rispetto a ranitidina 300 mg/die e ranitidina 600 mg/die. Esomeprazolo
40 mg die favorisce la guarigione a 4 settimane in maniera maggiore di
omeprazolo 20 mg die. Nessuna differenza per quanto riguarda il beneficio
clinico tra gli altri IPP.
Pazienti con endoscopia negativa (NERD)
IPP e anti-H2-R hanno efficacia sovrapponibile. Poiché un breve ciclo di terapia
con IPP ad alte dosi riduce i sintomi ed ha valore diagnostico, gli IPP sono
raccomandati come farmaci di prima scelta. In pazienti non responsivi agli IPP è
necessario approfondimento diagnostico con pH-metria delle 24 ore. Se
negativa, devono essere prese in considerazione diagnosi diverse dalla MRGE (a
parte i casi con reflusso acido minimo o con reflusso alcalino),quali la pirosi
funzionale o le anomalie motorie.

53
Terapia di mantenimento:
Circa il 90% dei pazienti con esofagite e il 44-75% dei pazienti con endoscopia
negativa presenterà una recidiva dei sintomi entro 6 mesi dalla sospensione della
terapia.Non vi sono dati solidi sull'efficacia delle modalità di terapia step-up
(IPP in mantenimento dopo terapia iniziale con anti-H2-R), step-down
(mantenimento con anti-H2-R dopo terapia iniziale con IPP) e step-in
(mantenimento della stessa categoria di farmaco alla dose efficace nella terapia
iniziale). Gli IPP sono i farmaci di prima scelta. Essi riducono il tasso di recidiva
dei sintomi e di esofagite rispetto agli anti-H2-R. Tra gli IPP, l’omeprazolo è il
farmaco maggiormente studiato. Omeprazolo sia alla dose di 20 md/die che di
10 mg/die è più efficace di ranitidina 150 mg bid a 12 mesi. Per quanto riguarda
gli altri IPP, non vi è differenza tra lansoprazolo a dose strandard (30 mg/die) e
omeprazolo 20 mg/die ne fra rabeprazolo (10 o 20 mg/die) e omeprazolo 20
mg/die a 12 mesi, mentre lansoprazolo a bassa dose (15 mg/die) si è dimostrato
meno efficace di lansoprazolo 30 mg/die, omeprazolo 20 mg/die ed
esomeprazolo 20 mg/die nel mantenimento della guarigione a 12 mesi.

54
Modalità di controllo lungo termine dei sintomi
Vi sono diverse modalità che si possono ricondurre sostanzialmente a due
diversi approcci:
il trattamento giornaliero continuativo. Può essere protratto per periodi
variabili, in qualche caso per tutta la vita, adeguandolo di volta in volta alle
necessità del singolo paziente. Tale strategia è raccomandata nei pazienti con
esofagite severa (grado C e D) dove vi è anche un buon rapporto costo-efficacia.
trattamento “on demand”: il farmaco viene utilizzato ripetitivamente solo in
occasione della comparsa dei sintomi e per tutta la durata dello stesso, poi
sospeso. E’ una modalità consigliata nella MRGE lieve-moderata e nella NERD.
In alcune linee guida compaiono altre 2 modalità: il “trattamento intermittente”
(condotto per 2-4 settimane e successivamente ripreso alla ricomparsa dei
sintomi per la stessa durata e alla stessa dose che aveva indotto la precedente
remissione) che ha però minor efficacia clinica dei
precedenti.
il trattamento nel solo week-end (“week-end therapy”), che non ha
presupposti fisiopatologici e quindi va evitato.

55
MRGE complicata
Anche in pazienti con MRGE complicata gli IPP sono i farmaci di prima scelta.
In pazienti con esofagite di grado ≥ 2, stenosi esofagea benigna e almeno 1
episodio di disfagia/settimana, omeprazolo 20 mg/die è superiore agli anti-H2-R
(ranitidina e famotidina) nel tasso di guarigione dell'esofagite (100% vs 53%),
nel tasso di riduzione della disfagia (94% vs 40%) e per la minor necessità di
dilatazioni esofagee (41% vs 73%).

56
CCAAPPIITTOOLLOO VVIIII
EENNDDOOSSCCOOPPIICC FFUULLLL--TTHHIICCKKNNEESS PPLLIICCAATTIIOONN
Il trattamento endoscopico della MRGE è di recente introduzione ed ancora in
fase sperimentale. Esso consiste nella creazione di una plica trans murale a circa
1 cm della giunzione gastro-esofagea ( endoscopic full-thickness plication ), al
fine di ristabilire la competenza del cardias gastrico. Lo studio di Pleskow e
collaboratori [21] condotto su 64 pazienti, ha mostrato una buona riuscita
dell’intervento nel breve periodo (eliminazione della terapia medica
rappresentata da PPI dopo un periodo di 6 mesi dall’esecuzione dell’intervento),
con un miglioramento della QoL. Ma studi dimostranti la sua efficacia nel lungo
periodo non ci sono ancora noti, considerando che si tratta di una terapia
decisamente recente ed ancora per uso sperimentale.
STRUMENTI:
L’Endoscopic Plication System (EPS), è uno strumento riutilizzabile che viene
utilizzato per far passare due aghi attraverso i tessuti, nel punto desiderato, con
lo scopo di creare una plicatura. Lo strumento contiene due canali, uno per
l’inserzione del Retrattore dei tessuti, l’altro per il passaggio dell’endoscopio.
ENDOSCOPIC TISSUE RETRACTOR: L’Endoscopic Tissue Retractor
è un sistema in grado di fissare la parete gastrica ad 1cm distalmente alla

57
Giunzione Esofago-Gastrica con lo scopo di creare una plicatura tra sierosa-
sierosa.
Il device è riutilizzabile, mentre l’impianto di sutura può essere utilizzato una
singola volta. Per la seguente procedura vengono utilizzati un retrattore dei
tessuti ed un Overtube standard.
PROCEDURA
Dapprima si introduce un Endoscopio per esaminare l’esofago distale e lo
stomaco. Si fa passare un filo-guida metallico attraverso l’endoscopio nel piloro.
In seguito, si rimuove l’endoscopio e si introducono, grazie al filo metallico, un
Dilatatore (54 F), ed un Overtube (60 F). Si rimuovono il dilatatore e il filo-
guida metallico, e l’EPS e l’endoscopio vengono introdotti nello stomaco.
L’overtube viene retratto in modo tale da posizionarlo prossimalmente alla
giunzione esofago-gastrica, e lo stomaco viene dilatato con aria. L’endoscopio
viene fatto avanzare e retro flettere, in modo tale da visualizzare e posizionare
correttamente lo strumento. L’EPS viene fatto retro flettere ad 1 cm di
distalmente rispetto alla giunzione esofago-gastrica, ed il retrattore tissutale
viene fatto avanzare profondamente nella parete gastrica.
In seguito, si retrae la parete gastrica nel braccio dell’EPS, con la quale viene
chiusa e suturata per fissare la full-thickness plication.
Il retrattore tissutale viene disimpegnato, così come l’impianto di sutura. L’EPS
e l’endoscopio vengono tolti, così come l’overtube.

58
Immagini per via endoscopica sono state ottenute durante l’intera procedura.
TRATTAMENTO POST-INTERVENTO: Ai pazienti viene somministrato anti-
dolorifico (Acetaminofene), al bisogno per il trattamento del dolore. Per 7 giorni
i pazienti continuano ad assumere PPI, la cui somministrazione verrà poi
interrotta.[22]
CRITERI DI INCLUSIONE AL TRATTAMENTO ENDOSCOPICO:
Ernia Iatale <2 cm;
Esofagite di I-II grado;
Assenza di esofago di Barrett;
QoL ridotta per la MRGE;
Sintomatologia di pirosi e rigurgito di durata >6 mesi;
pH-metria delle 24h dimostrante un reflusso patologico (definito
come pH<4 nelle 24 h);
Manometria esofagea dimostrante una peristalsi esofagea adeguata
(definita come una contrazione media del corpo esofageo >35 mmHg)
e Pressione a riposo del LES di 5 mmHg;

59
CCAAPPIITTOOLLOO VVIIIIII
TTEERRAAPPIIAA CCHHIIRRUURRGGIICCAA
INDICAZIONI AL TRATTAMENTO CHIRURGICO
La MRGE è una patologia estremamente diffusa nella popolazione occidentale.Il
trattamento medico, tuttavia, è capace di risolvere la sintomatologia nella gran
parte dei casi. Una minoranza della popolazione dei pazienti affetti da MRGE,
invece, lamenta, nonostante un trattamento medico appropriato e continuo, un
perpetuarsi della sintomatologia, oltre alla comparsa di temibili complicanze. Da
qui, l’importanza di un trattamento alternativo, efficace e tendenzialmente
risolutivo.
INDICAZIONI ASSOLUTE AL TRATTAMENTO CHIRURGICO:
Esofagite di IV grado;
Stenosi peptica esofagea;
Esofago di Barrett complicato (ulcera, stenosi);
Esogagite di III grado senza miglioramento con terapia medica;
Ulcera giunzionale senza miglioramento con terapia medica.

60
INDICAZIONI RELATIVE AL TRATTAMENTO CHIRURGICO:
Esofagite di II grado senza miglioramento con terapia medica;
MRGE con complicazioni broncopolmonari e laringiti che;
MRGE associata ad Ernia Iatale e Volvolo paraesofageo;
MRGE giovanile persistente e resistente ai farmaci;
MRGE senza esofagite ma fortemente sintomatica.
CENNI STORICI E TECNICHE CHIRURGICHE
La MRGE divenne per la prima volta di interesse chirurgico nel 1951 quando
Allison capì che era necessario che la giunzione esofago-gastrica fosse in

61
addome perché facesse la sua corretta funzione evitando il reflusso delle
secrezioni gastriche in esofago. Veniva compreso che la correzione dell’ernia
iatale in presenza di MRGE doveva, con un solo intervento, riuscire a correggere
le tre componenti fondamentali:
Ridurre lo stomaco, il cardias e l’esofago in addome;
Restaurare l’angolo di His per impedire il reflusso peptico;
Restringere lo iato per prevenire le recidive.
Le vie che permettevano di accedere alla regione dello iato erano due: quella
toracica e quella addominale; la toracica fu la prima ad imporsi, ma quella che
trova ancor oggi larghi consensi, è quella addominale, concretizzata quando
Nissen, nel 1956 propose la fundoplicatio totale a 360°.[ 12]
Questa tecnica chirurgica prevede quale accesso all’addome, un’incisione
mediana xifo-sottombellicale. Si seziona il legamento triangolare sinistro del
fegato e si espone il peritoneo che riveste la giunzione esofago-gastrica, il quale
viene inciso insieme ai residui della membrana freno-esofagea. Con l’aiuto del
dito indice, l’esofago viene completamento isolato insieme ai nervi vaghi e viene
passata in questo spazio una fettuccia. Si mettono 2-3 punti in seta nel pilastro
destro del diaframma, includendo il peritoneo che in parte lo riveste; questi fili
devono essere annodati senza alcuna tensione in modo da avvicinare soltanto i
margini dello iato e non lacerare le fibre muscolari estremamente fragili. Si
prepara la grande curvatura gastrica sezionando i primi 2-3 vasi brevi. Dopo aver
fatto progredire una sonda esofagea, il fondo gastrico viene fatto passare dietro

62
l’esofago e viene realizzata la plastica ancorando il fondo dello stomaco da
ambedue i lati e l’esofago al centro.
Nel 1966 Rossetti, allievo di Nissen, proponeva una modifica della
Fundoplicatio del suo Maestro.
Questa tecnica differisce da quella di Nissen in quanto non prevede la
Iatoplastica e la sezione dei vasi brevi, inoltre per la realizzazione della
fundoplicatio la parete gastrica è fissata con 3 o 4 punti siero-muscolari senza
trafiggere l’esofago.
Alla tecnica di Nissen seguirono diverse varianti oltre a quella di Rossetti.
La gastropessia posteriore di Hill che, come nella Nissen, adotta la stessa via di
accesso, realizza il distacco del legamento triangolare sinistro del fegato,
l’isolamento dell’esofago e la sezione dei primi 2-3 vasi brevi. E’ a questo punto
che si sutura posteriormente lo iato senza stringere troppo e si esegue la
gastropessia posteriore con 3 o 4 staccati in seta che includono i due margini
peritoneali della piccola curva ed il legamento arcuato mediano.
Simile nella fase iniziale della Nissen è la tecnica proposta da Lortat-Jacob che
dopo la riduzione dell’ernia e la iato plastica, effettua la ricostruzione
dell’angolo di His con 3-4 punti di seta fra il margine sinistro dell’esofago e del
bordo destro del fondo gastrico e la gastropessia ponendo 3-4 punti fra l’apice
del fondo gastrico e cupola diaframmatica.
Queste tecniche si rivelarono efficaci per il controllo del reflusso ma non furono
scevre di effetti collaterali: il più importante è la “gas bloat syndrome” che

63
consiste nella impossibilità di eruttare l’aria deglutita sino ad arrivare
all’impossibilità di vomitare, con la necessità in alcuni casi di dover posizionare
un sondino naso-gastrico d’urgenza.
Nascono così altre tecniche, agli inizi degli anni ’60. Dor e Toupet (1962 e
1963), [14]misero a punto una emifundoplicatio rispettivamente anteriore e
posteriore con la quale tale inconveniente fu evitato. (VEDI TECNICA
SECONDO DOR E TOUPET).
Negli Stati Uniti riscuote ancora larghi consensi la Protesi di Angelchik per la
sua semplicità di posizionamento; questa tecnica consiste in una dissezione
minima dell’esofago addominale, attorno al quale viene passata la protesi,
rappresentata da un anello in silicone di 2 cm di spessore; il suo posizionamento
viene garantito da due lacci in Dacron che, annodati sulla faccia anteriore
dell’esofago, garantiscono la chiusura della protesi ed il suo mantenimento
attorno all’esofago; è buona norma chiudere i pilastri diaframmatici per
scongiurare la migrazione dell’anello in mediastino. Questa metodica, in Europa,
non ha riscontrato consensi.
Ma la prima plastica antireflusso per via laparoscopica è stata eseguita nel 1991
grazie a Bernard Dallemagne.
L’esecuzione per via laparoscopica della plastica anti-reflusso secondo la
tecnica di Nissen riscosse immediatamente ampi consensi grazie all’accuratezza
con la quale l’anatomia della regione iatale può essere individuata e affrontata.

64
Rapidamente sono state prese in esame le diverse fundoplicatio e sono state
proposte nuove tecniche o varianti:
la variante di Rossetti, anch’essa fundoplicatio completa;
le emifundoplicatio secondo Toupet e Dor, tecniche salite alla ribalta per la
facilità di esecuzione.
TECNICA SECONDO NISSEN-ROSSETTI
Preparazione del paziente
Il paziente viene operato dopo un digiuno di 12 ore, avendo praticato un clistere
evacuativo la sera dell’intervento. Nei giorni precedenti l’intervento, viene
praticato un regime alimentare senza particolari restrizioni.[3]
Strumentario chirurgico
Ottica;
Ago di Verres;
5 trocars (3 da 5 mm e 2 da 10 mm);
Pinza da presa tipo Babcock;
Aspiratore/Irrigatore;
Due pinza da presa fenestrate tipo Johann da 5 mm;
Dissettore a radiofrequenza/ultrasuoni;
Portaghi;
Retrattore esofageo;

65
Fili di sutura in materiale non riassorbibile intrecciato ad annodamento
extracorporeo.
Posizione del paziente in sala operatoria
Il paziente in anestesia generale e ventilato attraverso un tubo oro tracheale, viene
posto in posizione litotomica modificata come nella colecistectomia secondo la tecnica
francese. Il tavolo operatorio viene inclinato a circa 20° in anti-Trendelenburg. Il
chirurgo si pone tra le gambe divaricate del paziente, l’aiuto alla sua destra e
l’assistente addetto all’ottica alla sua sinistra. Infine, la strumentista si pone alla destra
dell’operatore, ai piedi del paziente.La colonna laparoscopica ( monitor, fonte
luminosa, telecamera, insufflatore), è posizionata alla destra del paziente, all’altezza
della testa. La colonna endoscopica è collocata, invece, alla sua SINISTRA.
Tecnica chirurgica fundoplicatio secondo Nissen-Rossetti per via
laparoscopica
La tecnica chirurgica comprende dei tempi operatori ben standardizzati, che in sintesi,
possono essere riassunti come di seguito:
Il paziente è posto sul tavolo operatorio supino e con gli arti inferiori divaricati di 60°.
L’arto superiore sinistro viene esteso lateralmente in modo da offrire all’anestesista un
facile accesso venoso.

66
Indotto lo pneumoperitoneo a 12 mmHg mediante ago di Verèss in sede
ombelicale, si procede al posizionamento di cinque Trocars: due con calibro di
10-12 mm ed i restanti tre, con calibro di 5 mm.
In un paziente normotipo, il primo trocars viene posizionato sulla linea Xifo-
ombelicale al limite fra il terzo inferiore e il terzo medio della stessa. Attraverso
questo trocars da 10-12mm transiterà durante tutto l’intervento, l’ottica
laparoscopica. Il secondo trocars, del calibro di 5 mm, viene posizionato in sede
Sotto-Xifoidea, alcuni cm a destra della linea mediana; questo trocar darà
passaggio ad uno strumento di divaricazione, retto o a curvatura variabile che,
affidato all’assistente, permetterà, grazie anche alla leva esercitata sul legamento
falciforme, di sollevare il fegato sinistro, manovra indispensabile per garantire
l’accesso visivo ed operativo alla regione dello iato esofageo.

67
Il terzo trocar, da 5 mm, viene posto in sede sottocostale sinistra, sulla linea
emiclaveare: questa via sarà utilizzata prevalentemente dall’aiuto per gestire il
sistema di lavaggio – aspirazione e soprattutto per effettuare un’azione modulata
di trazione sulla parete del corpo gastrico. Il quarto trocar, da 5 mm, viene posto
in fianco destro allo stesso livello dell’ottica.
L’ultimo trocar, da 10-12 mm, viene posizionato in fianco sinistro, alcuni
centimetri sopra la linea ombelicale trasversa. Gli ultimi due trocars
rappresentano i veri e propri accessi operativi gestiti bi manualmente dal
chirurgo nel corso dell’intervento.
La prima fase dell’intervento prevede l’apertura del piccolo omento con
l’eventuale ausilio della coagulazione bipolare (durante tale manovra bisogna
porre particolare attenzione alla eventuale presenza di una arteria epatica sinistra
accessoria), così da visualizzare il pilastro diaframmatico destro; si procede poi
alla liberazione dello iato fino ad esporre il versante mediale del pilastro sinistro;
la dissezione si completa, infine, liberando l’angolo di His.
Successivamente, si passa alla liberazione dell’esofago; durante tale tempo il
nervo vago posteriore deve essere visualizzato e lasciato cadere su un piano
posteriore rispetto alla dissezione. Queste manovre espongono al rischio di
aprire accidentalmente la pleura mediastinica; evenienza questa che deve essere

68
prontamente riconosciuta dall’anestesista e rapidamente trattata con il
posizionamento di un trocar in torace per drenare il pneumotorace.
Isolato completamente l’esofago, si procede al “test” di passaggio della valva
gastrica sotto l’esofago terminale: la sua retrazione spontanea impone il “tempo”
sui vasi brevi. La sezione dei vasi brevi contenuti nel legamento gastro-splenico
viene eseguita di principio con la pinza bipolare. Questa manovra, nella
fundoplicatio secondo Nissen, garantisce una trazione non eccessiva sul fondo
gastrico, così da evitare la rotazione in senso orario dell’asse longitudinale
dell’esofago con conseguenti ripercussioni sulla funzionalità della giunzione
esofago-gastrica.
Verificata la fattibilità di una Floppy-fundoplicatio, si confeziona una iato-
plastica posteriore mediante uno o due punti di sutura ad annodamento extra-
corporeo. La cravatta gastrica, dell’altezza di tre centimetri, viene confezionata

69
anch’essa a punti staccati, con annodamento extra-corporeo, calibrata su sonda
esofagea da 40 f. Il filo utilizzato è in polipropilene con ago curvo. Il primo
punto aggancia l’estremità superiore sinistra del fondo gastrico, l’estremità
superiore del versante destro del fondo gastrico e, infine, il pilastro destro del
diaframma. Il secondo punto interesserà il fondo gastrico a sinistra ed il fondo
gastrico a destra. In modo del tutto analogo si procederà col terzo punto. Questa
tecnica non richiede la trasfissione dell’esofago; un eventuale quarto punto
interesserà il fondo ed il corpo gastrico (Variante di Rossetti).
L’intervento termina dopo un’attenta verifica dell’emostasi. Nessun drenaggio
viene lasciato solitamente nel cavo addominale.
FUNDOPLICATIO PARZIALE: PLASTICA SECONDO DOR E
TOUPET
Quando la motilità esofagea è scarsa (peristalsi < 60% o ampiezza esofagea
distale <30 mmHg ), si dovrebbe eseguire una fundoplicatio parziale per
prevenire l’ostruzione da bolo in esofago.
La dissezione iniziale è la stessa.
Se si preferisce eseguire una plastica anteriore ( tipo Dor ), non vi è necessità di
sezionare le connessioni esofagee posteriori. La plastica sec. Dor sono state
create con il fondo posto sopra la faccia anteriore esofagea e sono ancorate allo
iato ed all’esofago come nella plastica a 360° sec. Nissen-Rossetti. L’esperienza
con questo tipo di plastica anti-reflusso è limitata nei pazienti con MRGE, in

70
quanto le principali indicazioni a questo tipo di intervento risiedono
principalmente nei pazienti affetti da Acalasia.
Se si esegue una Plastica Posteriore secondo Toupet, l’intera dissezione esofagea
è sovrapponibile a quella descritta per la plastica a 360°, con eguale
riavvicinamento diaframmatico. La ricostruzione della Fundoplicatio posteriore
è iniziata passando il fondo posteriormente all’esofago da sinistra a destra. La
fundoplicatio è stata creata ancorando il fondo posteriormente ai pilastri ed
all’esofago. Le suture più prossimali della plastica includono tutte e tre le
strutture, fondo, pilastri ed esofago. La plastica è ancorata posteriormente ai
pilastri con due o tre suture. Il fondo è suturato all’esofago lungo gli spazi
antero-laterali, creando una plastica di 225°/250°.[3;10;14]

71
CCAAPPIITTOOLLOO IIXX
CCOOMMPPLLIICCAANNZZEE DDEELLLLAA TTEECCNNIICCAA CCHHIIRRUURRGGIICCAA
NNIISSSSEENN--RROOSSSSEETTTTII
La plastica antireflusso secondo Nissen per via laparoscopica è una metodica che
sta prendendo larga diffusione per la sicurezza della procedura in termini di
morbilità e mortalità. Le complicanze che possono insorgere in seguito a tale
procedura sono:
Erniazione trans diaframmatica (wrap migration): evenienza particolarmente
rara (la letteratura ne riporta un’incidenza tra il 7-20%). Si manifesta con dolore
retrosternale acuto. La strategia utilizzata da diversi centri per ridurre l’incidenza
della Wrap Migration consiste nella saturazione routinaria dello iato (in
particolare, riparazione della porzione posteriore crurale), una buona analgesia
post-operatoria e terapia anti-emetica; può comparire sia nel post-operatorio
precoce, che dopo diversi mesi dall’intervento.
Wrap Ischemia con perforazione: complicanza rara, riscontrata in letteratura
soprattutto in soggetti anziani con arteriopatia, o in seguito ad assunzioni
importanti di alcool dopo poche settimane dall’intervento. Diagnosticabile
attraverso Rx-Diretta Addome in urgenza e TC-scan, che mostrerà la Wrap

72
migration e la perforazione gastrica. L’intervento, in emergenza, consiste in
gastrectomia parziale.
Perforazioni del tratto GastroEnterico: La perforazione dell’esofago e dello
stomaco costituisce una grave complicanza di questo tipo di chirurgia con
un’incidenza, per la chirurgia Laparoscopica (2,1%) 2 volte superiore a quella
della tecnica chirurgica tradizionale “open”(1,1%), ed una mortalità del 26%. Le
cause possono essere ascrivibili a:
1- Perforazione dell’esofago durante la sua mobilizzazione;
2- Perforazione dello stomaco per eccessiva trazione del viscere o per uso di
un inappropriato strumento da presa;
3- Passaggio del dilatatore intraesofageo o del SNG.
Il trattamento sarà determinato dall’entità della lesione e dal suo riconoscimento
più o meno precoce.
Disfagia post-operatoria: rara la disfagia post-operatoria assoluta.
Ricorrenza del Rigurgito
Ricorrenza del Bruciore: evenienza non rara, specie se considerata a lungo
termine, ma con diminuzione della sintomatologia se paragonata alla situazione
pre-operatoria ed un miglioramento della QoL del paziente.
Bloating syndrome: sensazione di ripienezza post-prandiale con distensione
addominale. L’incidenza è del 20-30%, ma in meno del 4% dei casi residua dopo
2 mesi dall’intervento. Evenienza molto più frequente quando si utilizza la
tecnica “open”, rispetto alla via laparoscopica.

73
Pneumotorace: evenienza rara, causata da un veloce assorbimento della
CO2, introdotta per creare il pneumoperitoneo, da parte della cavità pleurica.
Enfisema chirurgico e pneumomediastino: complicanza abbastanza comune,
difficilmente riconoscibile per la di segni e sintomi patognomonici. E’,
all’esordio, solitamente palpabile nell’area sopra-clavicolare di sinistra; in
seguito può divenire bilaterale ed estendersi al collo.
Embolia polmonare: L’incidenza è stimabile intorno all’ 1,8% con un
aumento di quest’ultima nella procedura per via laparoscopica rispetto alla
tecnica “open”. Le cause alla quale è ascrivibile sono: Pneumoperitoneo, la
posizione intra-operatoria Anti-Trendelemburg, l’attivazione del sistema della
coagulazione. E’ opportuno effettuare una adeguata prevenzione primaria,
mediante terapia anticoagulante pre- e post-operatoria, compressione pneumatica
intermittente e bendaggio compressivo graduato, soprattutto nei soggetti affetti
da Trombosi Venosa Profonda (TVP).
Nausea e vomito post-operatorio: trattabile con anti-emetici e, nei casi più
gravi, con Sondino-Naso-Gastrico.

74
CCAAPPIITTOOLLOO XX
CCAASSIISSTTIICCAA
Questo studio retrospettivo prende in considerazione 122 pazienti affetti da Malattia
da Reflusso Gastro Esofageo ricoverati presso il UOS di Chirurgia Laparoscopica,
diretta dal Prof. Giorgio Palazzini, del Policlinico Umberto I° “La Sapienza.
Università di Roma”, nel periodo compreso tra il gennaio 1998 ed il dicembre 2008.
Di questi, 29 sono stati sottoposti a terapia medica e 93 sono stati sottoposti ad
intervento chirurgico di Plastica Anti-Reflusso per via laparoscopica.
PAZIENTI SOTTOPOSTI A TERAPIA MEDICA
I 29 pazienti erano 14 uomini, età media 58 anni (range: 25-85), e 15 donne, età
media 60 anni (range: 25-72). I pazienti venivano inviati alla nostra struttura dal
DEA di 2° livello del Policlinico Umberto I°
I pazienti sono stati valutati mediante EGDS e RX-transito esofageo.
La valutazione endoscopica ha messo in evidenenza:
In 11 pazienti (41%): Ernia Iatale in assenza di Esofagite;
In 10 pazienti ( 34%) : Esofagite di I° grado;
In 6 pazienti ( 21 %) : Esofagite di II° ;
In 1 paziente ( 3%) : Esofagite di IV° grado;
In 1 paziente: quadro endoscopico del tutto normale.

75
I criteri utilizzati per candidare i pazienti alla sola terapia farmacologica sono
stati:
Sintomatologia di recente insorgenza;
Assenza di complicanze;
Esofagite di I°-II° grado all’EGDS;
Ernia Iatale di grado lieve;
Buona risposta alla terapia medica.
I pazienti sono stati trattati con Inibitori di Pompa Protonica (PPI), H2-
Antagonisti, farmaci a base di Acido Alginico con dosaggi e modalità di
somministrazione valutate per ogni singolo paziente.
PAZIENTI SOTTOPOSTI A TRATTAMENTO CHIRUGICO
I 93 pazienti sottoposti a trattamento chirurgico erano 49 uomini, età media 52 anni
(range: 38-58), e 44 donne, età media 60 anni (range: 40-77).
I pazienti sottoposti a trattamento chirurgico sono stati valutati pre-operatoriamente
mediante:
Rx transito esofageo;
EGDS;
Manometria Esofagea;
pH-metria esofagea delle 24 h;
La valutazione endoscopica pre-operatoria ha messo in evidenza:

76
In 62 pazienti (66%) : esofagite di I° grado
In 15 pazienti (16%) : Esofagite di I° grado associata ad ernia iatale.
In 8 pazienti (9%) : assenza di esofagite, ma presenza di una voluminosa
ernia sovra diaframmatica;
In 8 pazienti (9%) : assenza di esofagite, ma presenza di un’ernia
paraesofagea strozzata.
I criteri utilizzati per candidare i pazienti alla plastica anti-reflusso sono stati:
sintomatologia persistente o ricorrente dopo un anno di terapia
farmacologica;
comparsa di complicanze;
pH-metria delle 24h significativa per malattia da Reflusso;
manometria significativa per una alterazione a carico dello sfintere esofageo
inferiore.
Secondo la classificazione ASA, 24 pazienti (26%) appartenevano alla Classe ASA
II, mentre 69 pazienti (74%) appartenevano alla Classe ASA III.
Nella scelta del tipo di plastica anti reflusso da utilizzare, è stato importante
valutare la motilità esofagea.
I pazienti con motilità esofagea nella norma sono stati sottoposti a fundoplicatio
completa. In presenza di alterata o assente motilità esofagea, invece, si è
proceduto a emifundoplicatio.
L’intervento di prima scelta è stato una fundoplicatio completa.

77
La fundoplicatio secondo Nissen è stata realizzata per via laparoscopica in 84
pazienti (90%), 41 di sesso femminile, 43 di sesso maschile mentre, in 9 casi
(10%), si è effettuata una emifundoplicatio secondo Dor.
Il confezionamento della fundoplicatio senza la preventiva sezione dei vasi brevi
è sempre eseguibile, ma deve essere preceduto dal “test” di passaggio del fondo
gastrico sotto l’esofago terminale: la retrazione rapida e spontanea della valva
deve imporre il “tempo” dei vasi brevi e, di conseguenza, la realizzazione della
procedura di Nissen invece della variante Rossetti.

78
CCAAPPIITTOOLLOO XXII -- RRIISSUULLTTAATTII
PZ SOTTOPOSTI A TERAPIA MEDICA
Dei pazienti sottoposti a terapia medica nessun paziente ha avuto effetti
collaterali legati all’assunzione dei farmaci somministrati.
Dopo circa 3 settimane:
25 pazienti ( 86%), riferivano la scomparsa della sintomatologia, dei quali,15
(52%), col solo uso dei PPI e 10 (34%), previa associazione ai PPI di Acido
Alginico.
In 4 pazienti (14%), si è assistito a miglioramento della sintomatologia senza
la scomparsa di quest’ultima.
Per il miglioramento del quadro clinico, tali pazienti non sono stati sottoposti a
terapia chirurgica.
Un primo follow-up, eseguito un anno dopo, evidenziava:
In 2 pazienti ( 7%): totale scomparsa della sintomatologia e
interruzione di ogni terapia farmacologica per il trattamento della
MRGE;
In 8 pazienti (28%): scomparsa della sintomatologia ma prosecuzione
della terapia medica dovuta alla concomitante assunzione di farmci
gastro-lesivi (cardioaspirina, cortisonici), per altre patologie;
5 pazienti ( 17%), riferivano assunzione della terapia medica
saltuariamente alla ricomparsa della sintomatologia;

79
7 pazienti (24%) : non hanno interrotto la terapia medica in quanto la
sua sospensione causava la ricomparsa della sintomatologia;
2 pazienti ( 7%): riferivano assunzione quotidiana della terapia ma
senza alcun miglioramento clinico;
5 pazienti (17%) : persi al follow-up.
Ad un follow-up di 10 anni, i risultati rimangono sostanzialmente immutati, eccezione
fatta per una paziente che, visto il peggioramento del quadro clinico, ha scelto
l’alternativa chirurgica.
PAZIENTI SOTTOPOSTI A TERAPIA CHIRURGICA
In tutti i pazienti candidati all’intervento chirurgico è stato possibile eseguire una
plastica antireflusso per via laparoscopica.
Il tempo operatorio medio è stato di 120 minuti (range 70-250).
Non si è assistito a mortalità peri- o intra-operatoria.
Una paziente sottoposta a Fundoplicatio secondo Nissen ha presentato in X
giornata post-operatoria, embolia polmonare, trattata con Eparina, con modalità
di somministrazione e dosaggi conformi alle linee guida per il trattamento
dell’embolia polmonare.

80
Il protocollo post-operatorio ha previsto l’esecuzione in prima giornata di un
controllo radiologico del transito esofago-gastrico per valutare la posizione e la
funzionalità della valva anti reflusso e l’assenza di stenosi significative. In
presenza di esame normale è stato possibile rimuovere il sondino naso-gastrico,
sospendere la terapia infusionale e riprendere l’alimentazione.
I pazienti sono stati dimessi tra la quinta e l’ottava giornata post-operatoria.
Un mese dopo l’intervento chirurgico, i pazienti sono stati sottoposti ad un
primo controllo clinico che ha evidenziato Disfagia in 24 pazienti (26%).
Tre mesi dopo l’intervento chirurgico, una paziente ha avuto la ricomparsa dei
sintomi da MRGE, ed un Rx Esofagogramma ha notato una recidiva dell’ernia.
Per tale motivo, è stata sottoposta nuovamente a intervento.
Sei mesi dopo l’intervento chirurgico, 17 pazienti (18%), riferivano saltuari
episodi di disfagia per i cibi solidi. Tale disturbo, tuttavia, non era di frequenza
tale da compromettere la QoL dei pazienti.
A 12 mesi di distanza dall’intervento, il follow-up mostrava:
In 32 pazienti (34%) : scomparsa totale della sintomatologia;
In 7 pazienti (8%) : ricomparsa della sintomatologia caratterizzata da
pirosi, rigurgito e saltuari episodi di disfagia. In questi pazienti, alla
ricomparsa del quadro clinico, la terapia basata su PPI è stata in grado di
controllare totalmente la sintomatologia.
In 15 pazienti (16%): completa remissione della sintomatologia, eccezione
fatta per saltuari (1-2/anno) episodi di disfagia per cibi solidi;

81
In 39 pazienti (42%): completa remissione della sintomatologia, ma
recidiva dell’ernia iatale di grado lieve, mostrata attraverso un controllo
endoscopico eseguito di routine. Per la totale negatività del quadro clinico,
non sono stati previsti provvedimenti terapeutici.
Ad un follow-up di 10 anni, i risultati si sono dimostrati sostanzialmente
sovrapponibili, eccezione fatta per 8 pazienti (9%), che assumono saltuariamente
PPI (circa 2 volte all’anno), in seguito a episodi di epigastralgia di grado lieve.

82
CCAAPPIITTOOLLOO XXIIII
DISCUSSIONE E CONCLUSIONI
L’affermazione ed il successo della chirurgia mini-invasiva sono
indiscutibilmente legate all’esecuzione della colecistectomia laparoscopica, al
suo rapido diffondersi ed al suo altrettanto rapido imporsi come tecnica
operatoria di prima scelta nel trattamento chirurgico della colelitiasi.
La rilevanza e lo spessore di questa novità chirurgica ne hanno incoraggiato, via
via, l’applicazione a nuove tipologie di intervento.
Tra essi, un posto di primo piano è certamente occupato dalla ricostruzione
anatomica della giunzione esofago-gastrica, che si propone quale atto risolutivo
della malattia da reflusso gastro esofageo.
A tale proposito stiamo assistendo ad un fenomeno alquanto importante ed
interessante, una vera e propria inversione di tendenza circa le indicazioni
terapeutiche della MRGE. Com’è noto, infatti, la sintesi di farmaci capaci di
contrastare l’acidità gastrica e quindi, in definitiva, di dominare la componente
patologica del reflusso , aveva ridotto drasticamente l’approccio chirurgico per
la cura di questa malattia. L’intervento, tra l’altro, realizzato per via open aveva
dato sì soddisfazioni, ma anche delusioni in termini di recidiva.
Oggi, tuttavia, la cura chirurgica, eseguita elettivamente tramite accesso video
laparoscopico, si sta paradossalmente riaffermando, considerando tra gli indubbi

83
vantaggi, la peculiare visione ingrandita e dettagliata offerta dall’accesso
laparoscopico di una regione, quale quella dello iato, così angusta e profonda.
Infatti, diversamente da quanto si è abituati a vedere, o meglio, a non vedere con
la tecnica tradizionale, per via mini-invasiva ogni repere e dettaglio anatomico
risulta meglio visualizzabile e pertanto ogni gesto chirurgico può essere
accurato, preciso e sicuro.
Queste considerazioni possono portare a rilevare che l’intervento di iato plastica
abbinato alla fundoplicatio si sposa felicemente con la tecnica laparoscopica e
deve essere considerato senza dubbio tra i più idonei all’approccio mini-
invasivo. Ciò è confermato anche da trial randomizzati che mostrano, ad una
distanza di 5 anni, uguale incidenza di recidive e/o ricomparsa della
sintomatologia in seguito a intervento di plastica anti-reflusso, sia essa eseguita
per via laparoscopica che con metodica tradizionale.[ 30 ] Se a tutto ciò
aggiungiamo l’approvazione da parte del paziente, si comprende perché la
metodica si stia diffondendo prepotentemente, restituendo al chirurgo il
trattamento di una patologia per la quale era stata decretata l’obbligatorietà,
tranne in casi sporadici, del trattamento farmacologico.
Nella nostra personale esperienza, abbiamo potuto constatare che, anche in
regime d’urgenza, l’approccio laparoscopico risulti essere sempre altamente
valido, soprattutto se eseguito in mani esperte. [18]
E’ però importante a questo punto, anche in previsione di una più diffusa
applicazione della metodica, pervenire alla definizione di protocolli diagnostici,

84
di indicazione all’intervento e di atti operativi codificati e, soprattutto, delineare
un giusto confine tra, l’ormai consolidata e estremamente diffusa terapia medica,
la recente terapia endoscopica e la terapia chirurgica.
La terapia medica viene comunemente indicata nei casi di:
Sintomatologia di recente insorgenza;
Assenza di complicanze;
Esofagite di I°-II° grado all’EGDS;
Ernia Iatale di grado lieve;
Secondo la nostra esperienza, è sempre lecito non consigliare un trattamento
chirurgico a quei pazienti che presentano queste caratteristiche e che,
soprattutto, alla sospensione della terapia medica non vedono un ripresentarsi
della sintomatologia. Basandoci sui nostri risultati e sulla più recente letteratura
[ 31;32;33;34 ], è opportuno non ritenere appropriato l’approccio
farmacologico ad oltranza quando i pazienti non rispondono alla terapia
medica, né in termini di miglioramento della QoL, né in termini di regressione
del quadro anatomo-patologico endoscopico. In questa categoria di pazienti
sarà opportuno consigliare un’alternativa terapeutica, tra cui l’intervento di
fundoplicatio, la quale si propone di curare definitivamente la MRGE,
ristabilendo una adeguata competenza della Barriera anti-Reflusso. Questo
risulta possibile, a livello anatomico, anche grazie alla riduzione e riparazione
dell’ernia iatale. Da qui la superiorità della terapia chirurgica rispetto a quella

85
medica, la quale si propone di ridurre l’acidità del succo gastrico
evidentemente non sufficiente in talune categorie di pazienti con MRGE.
Negli ultimi anni è comparsa una alternativa sia alla terapia medica che alla
terapia chirurgica, ovvero l’approccio per via endoscopica. Tale tecnica viene
indicata nei non-responders alla terapia medica. Le indicazioni, secondo la
recente letteratura[21;22 ], sono:
Ernia Iatale <2 cm;
Esofagite di I-II grado;
Assenza di esofago di Barrett;
QoL ridotta per la MRGE;
Sintomatologia di pirosi e rigurgito di durata >6 mesi;
pH-metria delle 24h dimostrante un reflusso patologico (definito come
pH<4 nelle 24 h);
Manometria esofagea dimostrante una peristalsi esofagea adeguata
(definita come una contrazione media del corpo esofageo >35 mmHg) e
Pressione a riposo del LES di 5 mmHg.
In realtà si tratta di una metodica ancora in via di studio, soprattutto se si
prendono in considerazione i risultati nel lungo periodo. Tale metodica è
caratterizzata, infatti, da un alto numero di recidive. Potrebbe, quindi, essere
indicata a scopo palliativo, vale a dire in quei casi che non rispondono alla

86
terapia medica, nei quali non è, per co-morbidità, indicato l’approccio
chirurgico.
In base alla nostra esperienza e alla letteratura internazionale, l’atto chirurgico è
indicato in caso di:
Mancata compliance alla terapia medica (intesa sia come scarsa QoL del
paziente che come eccessiva dipendenza dai farmaci [33;34;35;36; ] );
Esofagite di IV grado;
Stenosi peptica esofagea;
Esofago di Barrett complicato (ulcera, stenosi);
Esogagite di III grado senza miglioramento con terapia medica;
Ulcera giunzionale senza miglioramento con terapia medica.
Al contrario di quanto ritenuto in passato, l’obesità e l’età avanzata non sono
più da considerarsi fattori controindicanti l’intervento chirurgico, secondo
un’opinione condivisa, oltre che dal seguente studio, anche dalla letteratura
più recente [ 40 ].
L’indicazione al trattamento chirurgico è ancor più corretta se il paziente non
solo è affetto da MRGE, ma anche portatore di ernia iatale.
E’ bene citare, per conferma un importante trial clinico randomizzato [ 32 ],
condotto in 21 ospedali del Regno Unito, il quale ha dimostrato la superiorità del
trattamento chirurgico, ad un anno, in termini di miglioramento della QoL,

87
rispetto alla terapia medica, indipendentemente dalla tecnica chirurgica utilizzata
(fundoplicatio a 360° o emifundoplicatio), o dal tipo di trattamento
farmacologico somministrato (scelte effettuate in base all’esperienza del medico
o del chirurgo).
Delineati i casi in cui la terapia chirurgica risulti una indubbia indicazione,
restano ancora da chiarire le più idonee strategie terapeutiche nei casi limite,
cioè, in quella categoria di pazienti, responders solo ad una terapia medica
intensiva ma che vedono il ripresentarsi della loro sintomatologia al cessare di
quest’ultima. Questi pazienti difficilmente giungono precocemente al tavolo
operatorio. Solo il peggioramento da un punto di vista anatomo-patologico
dell’esofago convince di necessità al trattamento chirurgico; tuttavia, così
facendo, l’atto operatorio può risultare tecnicamente più complesso (ad esempio:
per la comparsa di periviscerite), ed il raggiungimento degli ottimi risultati post-
chirurgici potrebbe, allora, risultare compromesso.
Delineate sinteticamente le precedenti indicazioni ed entrando in merito ad un
discorso di tecnica chirugica, la scelta deve cadere su una fundoplicatio di 360°,
mediante ausilio dell’endoscopia intra-operatoria allo scopo di assicurare una
adeguata valva antireflusso. Ciò, oltre ad assicurare una migliore protezione
dell’esofago dal reflusso gastro-esofageo, riduce nettamente i disturbi disfagici,
assai frequenti nel primo post-operatorio. Tale complicanza risulta, nella nostra
casistica, in netta diminuzione se confrontata a studi presenti in letteratura.

88
Nei casi in cui il reflusso si associ ad un ritardato svuotamento gastrico, si
preferisce eseguire un intervento chirurgico che deve preferire il
confezionamento di una emifundoplicatio.
La tecnica di emifundoplicatio deve essere scelta obbligata anche per tutti quei
pazienti che presentano un difficoltoso transito esofageo e questo per evitare una
grave disfagia dovuta alla incapacità propulsiva del viscere. In questi ultimi
pazienti la manometria esofagea si rende assolutamente indispensabile.
Per quanto riguarda le voluminose ernie iatali, spesso associate al reflusso, esse
indubbiamente possono essere trattate per via laparoscopica, ma la capacità degli
operatori deve essere elevata e particolare attenzione deve essere posta
nell’evitare una accidentale, ma possibile, apertura delle pleure mediastiniche;
La presenza di un vero brachiesofago può essere invece la vera ed unica
controindicazione all’approccio laparoscopico.
La nostra esperienza ha dimostrato che è sempre lecito consigliare il trattamento
chirurgico in quei pazienti che presentano una MRGE complicata o refrattaria
alla terapia farmacologica. Non bisogna dimenticare i casi in cui esiste una bassa
compliance, da parte del paziente, ad una intensiva terapia medica. Anche in
questa categoria di pazienti, soprattutto si giovani, è sempre lecito consigliare
l’esecuzione di una Plastica Antireflusso.
L’intervento di Fundoplicatio secondo Nissen per Via video laparoscopica,
costituisce allo stato attuale, il trattamento di scelta. Presenta, difatti, i seguenti
vantaggi:

89
Mini invasività;
Riduzione delle complicanze post-operatorie (soprattutto quando si associ
l’uso dell’endoscopio o di altra sonda esofagea da 40/60F per la
calibratura dell’esofago);
Minore degenza ospedaliera;
Riduzione dei costi;
Maggiore compliance da parte dei pazienti.
Determinante il successo operatorio, sarà uno scrupoloso work-up pre-
operatorio, basato, oltre ad una valutazione clinica accurata per delineare
eventuali rischi operatori, per selezionare la tecnica operatoria più idonea ( la
scelta di una fundoplicatio a 360° rispetto ad una Emifundoplicatio secondo
Dor o Toupet).[ 42;43]
Difatti, paragonando i nostri dati alla più recente letteratura, l’esecuzione di
un’accurato work-up pre-operatorio, volto ad una selezione appropriata del
paziente, ha portato dei risultati favorevoli in termini di riduzione delle
complicanze post-operatorie e successo dell’intervento. Abbiamo, infatti,
assistito ad una riduzione importante della Disfagia Post-operatoria (riferita
dal 18% dei pazienti a 6 mesi dall’intervento), la quale si è andata nettamente
a ridurre nei mesi successivi, ricomparendo solo saltuariamente. Anche
questi saltuari episodi sono scomparsi in seguito a semplici accortezze di
ordine dietetico-comportamentali.

90
Paragonando i nostri dati alla più recente letteratura, abbiamo assistito ad
una netta diminuzione nella ricorrenza della sintomatologia, con necessità, da
parte del solo 8% dei pazienti, di assumere quotidianamente PPI per la
ricorrenza di rigurgito e/o di pirosi (versus 32-39 % presente in letteratura[
15;16]).
Riteniamo che questi successi siano da ricondurre anche ad una acquisita
esperienza da parte dell’èquipe chirurgica sia nell’esecuzione della tecnica,
che nella selezione accurata del paziente a cui consigliare l’intervento di
plastica anti-reflusso.

91
BBIIBBLLIIOOGGRRAAFFIIAA
[1] Harrison “Principi di Medicina Interna” 17 edizione Kasper,
Braunwald, Fauci, Longo, Jameson Casa Editrice Mc Graw Hill 2008;
[2] “Manuale di Gastroenterologia” Coordinamento Nazionale dei
Docenti Universitari di Gastroenterologia Edizione 2007-2009 Editrice
Gastroenterologica Italiana;
[3] “Encyclopedie Medico Chirurgicale”A.A.V.V. Casa Editrice
ELSEVIER MASSON
[4] “Anatomia Umana” Balboni, Bastianini, Brizzi, Castorina, Comparini,
Donato, Filogamo, Fusaroli, Lanza, Grossi, Manzoli, Miani, Mitolo, Motta,
Nesci, Orlandini, Passaponti, Pizzini, Reale, Renda, Ridola, Ruggeri,
Santoro, Tedde, Zaccheo. Edi-ERMES Edizioni;
[5] Guyton – Hall “Fisiologia Medica” EdiSES Edizioni;
[6] G. Cittadini “Diagnostica per Immagini e Radioterapia” Edizioni
Culturali Internazionali Genova; pagg. 414-427; 449-457;
[7] Rossi, Cuomo, Ricciardi “FARMACOLOGIA-Principi di base e
applicazioni terapeutiche” Edizioni Minerva Medica; pagg.463-492;

92
[8] Netter “Atlante di Anatomia Umana” Edizioni Masson;
[9] Robbins “Le Basi Anatomopatologiche delle Malattie” Cotran, Kumar,
Collins VII Edizione, Piccin Editore;
[10] R.Dionigi “CHIRURGIA” Carcano, Boni, G-Dionigi. Masson
Edizioni;
[11] Chiriatti A, PanzutoF, Bevilacqua S, et al. La MRGE, un progetto di
collaborazione tra medici di medicina generale e specialisti
gastroenterologi.Atti del 55° Congresso Nazionale FIMMG, Salsomaggiore
2003.
[12] Nissen R (1956) A simple operation for control of reflux esophagitis.
Schweiz Med Wochenschr 86:590–592;
[13] Vakil N, van Zanten SV, Kahrilas P, et al. The Montreal definition and
classification of gastroesophageal reflux disease: a global evidence-based
consensus. Am J Gastroenterol. 2006 Aug;101(8):1900-20
[14] Toupet A (1963) Technique of esophago-gastroplasty with
phrenogastropexy used in radical treatment of hiatal hernias as a
supplement to Heller’s operation in cardiospasms. Mem Acad Chir (Paris)
89:384–389

93
[15] Singhal, Balakrishnan, Hussain, Grandy-Smith, Paix, El-Hasani
“Management of complications after laparoscopic Nissen’s
Fundoplication: a surgeon’s perspective” Annals of Surgical Innovation
and Research 2009,3:1
[16] Rudolf Garcia-Gallont “Laparoscopic fundoplication for GERD: Are
we there yet?”Dig.Dis 2008;26:304-308
[17] Coster DD, Bower WH, Wilson VT, et al. (1997) Laparoscopic partial
fundoplication versus laparoscopic Nissen–Rosetti fundoplication. Short-
term results of 231 cases. Surg Endosc 11:625–631
[18] S.Aricieri, G.Palazzini, A.M.Romani, E.Orsi, C.Belfiore, S.Candioli,
A.Manigrasso, D.Mascagni, A.Filippini “Trattamento chirurgico
miniinvasivo d’urgenza di ernia gastrica iatale paraesofagea strozzata.
Caso clinico.” G.Chir. Vol.26 pp.438-442; Novembre-Dicembre 2005
[19] Lundell L, Abrahamsson H, Ruth M, et al. (1996) Long-term results of
a prospective randomized comparison of total fundic wrap (Nissen–
Rossetti) or semifundoplication (Toupet) for gastro-oesophageal reflux. Br
J Surg 83:830–835;
[20] NeufeldM, Graham A. Levels of evidence for techniques in
antireflux surgery. Dis Esophagus 2007;20:161-7.

94
[21] Pleskow, Rothstein, Kozark, Haber, Gostout, Lembo “Endoscopic full-
thickness plication for the treatment of GERD: long-term multicentric
result” Surg.Endosc. 2007;21:439-444;
[22] Pleskow, Rothstein, Kozarek, Haber, Gostout, Hawes Lembo
“Endoscopic full-thickness placation for the treatment of GERD: a
multicentric trial” Gastrointestinal Endoscopy Volume 59, No2, 2004;
[23] Kenneth R. De Vault M.D., F.A.C.G., Donald O, Castell M.D.
M.A.C.G. Departments of Medicine, Mayo Clinic College of Medicine,
Jacksonville, Florida Update Guidelines for the diagnosis and treatment of
gastroesophageal Reflux Disease Am J Gastroenterol 2005;100:190-200;
[ 24] E. M. Faybush, R. E. Sampliner Randomized trials in the treatment of
Barrett’s esophagus Diseases of the Esophagus (2005) 18, 291–297;
[25] J . P. Galmiche, F. Zerbib, S. Bruley des Varannes Review article:
respiratory manifestations of gastro-oesophageal reflux disease 2008 The
Authors, Aliment Pharmacol Ther 27, 449–464
Journal compilation a 2008 Blackwell Publishing Ltd;
[26] M.Nocon, Labenz, Jaspersen, Leodolter, K. Richter, M. Vieth, T. Lind,
Malfertheiner, N. Willich Clinical course of laryngo-respiratory symptoms
in gastrooesophageal reflux

95
disease during routine care: a 5-year follow-up Aliment Pharmacol Ther
1365-2036.2009
[27] Anupender Singh Sidhu, George Triadafi lopoulos Neuro-regulation of
lower esophageal sphincter function as treatment for
gastroesophageal refl ux disease World J Gastroenterol 2008 February 21;
14(7): 985-990
[28] E.Landi “Fisiopatologia del Giunto Esofago-Gastrico” Editoriale,
Ann.Italiani Chirurgia, LXI,2,1990;
[29] Radu Tutuian Update in the Diagnosis of Gastroesophageal Reflux
Disease J Gastrointestin Liver Dis September 2006 Vol.15 No.3, 243-247;
[30] P. Priego, E. Lobo, A. Sanjuanbenito, E. Martínez Molina, J. Pérez de
Oteyza, J. Ruiz Tovar,
G. Rodríguez Velasco and V. Fresneda Causes of conversion in
laparoscopic surgery for gastroesophageal reflux disease: An analysis of
our experience Rev Esp Enferm Dig 2008; 100: 263-267.
[31] A Grant, S Wileman, C Ramsay, L Bojke, D Epstein,M Sculpher, S
Macran, M Kilonzo, L Vale, J Francis, A Mowat, Z Krukowski, R Heading,
M Thursz, I Russell and M Campbell, on behalf of the reflux trial group The
effectiveness and cost-effectiveness of minimal access surgery amongst

96
people with gastro-oesophageal reflux disease – a UK collaborative study.
The reflux trial Health Technology Assessment 2008; Vol. 12: No. 31;
[32] Adrian M Grant, professor of health services research,1 Samantha M
Wileman, trial coordinator,1 Craig R Ramsay, senior statistician,1 N
Ashley Mowat, physician,2 Zygmunt H Krukowski, surgeon,2 Robert C
Heading, physician,3 Mark R Thursz, physician,4 Marion K Campbell,
director,1 and the REFLUX Trial GroupMinimal access surgery compared
with medical management for chronic gastro-oesophageal reflux disease:
UK collaborative randomised trial BMJ 2008;337:a2664;
[33] O. Chassany, G. Holtmann, J. Malagelada, U. Gebauer, H. Doerfle
and & K. Devault Systematic review: health-related quality of life
(HRQOL) questionnaires in gastro-oesophageal reflux disease 2008 The
Authors, Aliment Pharmacol Ther 27, 1053–1070;
[34 ] Vincenzo Stanghellini Rosanna Cogliandro Giovanni Barbara Cesare
Cremon, Roberto De Giorgio Roberto Corinaldesi How Relevant Is
Symptom Evaluation in NERD? Digestion 2008;78(suppl 1):11–16;
[35] M.Nocon, Labenz, Jaspersen, Leodolter, K. Richter, M. Vieth, T. Lind,
Malfertheiner, N. Willich, Health-related quality of life in patients with
gastro-oesophageal reflux disease under routine care:5-year follow-up
results of the ProGERD study Aliment Pharmacol Ther 29, 662–668 a 2009
Blackwell Publishing Ltd;

97
[ 36] N. W. Flook,1 I. Wiklund Accounting for the effect of GERD
symptoms on patients’
health-related quality of life: supporting optimal disease management by
primary care physicians Int J Clin Pract, December 2007, 61, 12, 2071–
2078;
[37] Susan Macran, Samantha Wileman2, Garry Barton, Ian Russel The
development of a new measure of quality of life in the management of
gastro-oesophageal reflux disease: the Reflux questionnaire Quality of Life
Research (2007) 16: 331–343
[38] Freys SM, Fuchs KH, Heimbucher J, et al. (1997) Tailored
augmentation of the lower esophageal sphincter in experimental antireflux
operations. Surg Endosc 11:1183–1188
[39] Hunter JG, Swanstrom L, Waring JP (1996) Dysphagia after
laparoscopic antireflux surgery. The impact of operative technique.Ann
Surg 224:51–57
[40] Jacob A. Chisholm & Glyn G. Jamieson & Carolyn J. Lally & Peter
G. Devitt & Philip A. Game & David I. Watson The Effect of Obesity on
the Outcome of Laparoscopic Antireflux Surgery J Gastrointest Surg
11605-009-0837-3 2009

98
[41] Vakil N, van Zanten SV, Kahrilas P, et al. The Montreal definition and
classification of gastroesophageal reflux disease: a global evidence-based
consensus. Am J Gastroenterol. 2006 Aug;101(8):1900-2000;
[42] Nigel Flook MD Roger Jones DM Nimish Vakil MD Approach to
gastroesophageal reflux disease in primary care Putting the Montreal
definition into practice; Can Fam Physician 2008;54:701-5;
[43] U. Strate A. Emmermann C. Fibbe P. Layer C. Zornig Laparoscopic
fundoplication: Nissen versus Toupet two-year outcome of a prospective
randomized study of 200 patients regarding preoperative esophageal
motility Surg Endosc (2008) 22:21–30
[44] Junghard and on behalf of the LOTUS trial collaborators L Lundell, S
Attwood, C Ell, R Fiocca, J-P Galmiche, J Hatlebakk, T Lind, O
Comparing laparoscopic antireflux surgery with esomeprazole in the
management of patients with chronic gastro-esofageal reflux disease: a 3-
year interim analysis of the LOTUS trial chronic gastro-oesophageal reflux
disease. Gut 2008;57;1207-1213;
[45] Carlo Calabrese, Davide Treré, Giuseppina Liguori, Veronica
Gabusi, Manuela Vici, Giovanna Cenacchi, Massimo Derenzini, Giulio Di
Febo Esophageal cell proliferation in gastroesophageal reflux disease:
Clinical-morphological data before and after pantoprazole World J
Gastroenterol 2009 February 28; 15(8): 936-941;

99
[46 ] E. M. Faybush, R. E. Sampliner Randomized trials in the treatment of
Barrett’s esophagus Diseases of the Esophagus (2005) 18, 291–297;
[47] Colm J. O’Boyle, Davidi, Watson, Andrew C. Debeaux and Glyng G.,
Jamieson Preoperative prediction of long term outcome following
laparoscopic fundoplication ANZ J. Surg.2002;72: 471–475;
[48] W. Cai1, D. I. Watson1, C. J. Lally1,2, P. G. Devitt2, P. A. Game2 and
G. G. Jamieson Ten-year clinical outcome of a prospective randomized
clinical trial of laparoscopic Nissen versus anterior 180° partial
fundoplication British Journal of Surgery 2008; 95: 1501–1505;
[49] S. Pérez-Holanda, G. L. Urdiales, J. A. Fernández, L. España, J.
Rodríguez-Rubio, M. D. Martínez, F. Fernández, S. Tojo, P. Fernández-
Muñiz, M. Calleja and D. Valverde Preoperative workup to assess
indication for laparoscopic treatment in gastroesophageal reflux disease
Rev Esp Enferm Dig 2008; 100: 405-410;
[50] Biertho L, Dallemagne B, Dewandre JM, Jehaes C, Markiewicz S,
Monami B, Wahlen C, Weerts J. Laparoscopic treatment of Barrett's
esophagus: long-term results.Surg Endosc. 2007 Jan;21(1):11-5. Epub 2006
Nov 16.
[51] Dallemagne B, Weerts J, Markiewicz S, Dewandre JM, Wahlen C,
Monami B, Jehaes C. Clinical results of laparoscopic fundoplication at ten
years after surgery; Surg.Endosc.2006 Jan;20(1):159-65.

100
[52] Dallemagne B, Weerts JM, Jeahes C, Markiewicz S Results of
laparoscopic Nissen fundoplication. Hepatogastroenterology. 1998 Sep-
Oct;45(23):1338-43.
[53] Jaspersen D, Kulig M, Labenz J, et al. Prevalence of
gastroesophageal manifestations in gastroesophageal reflux disease: an
analysis based on the ProGERD Study. Aliment Pharmacol Ther
2003;17:1515-20.
[54] Zentilin P, Iiritano E, Dulbecco P, et al. Normal values of 24-h
ambulatory intraluminal impedance combined with pH-metry in subjects
eating a Mediterranean diet. Dig Liver Dis 2006 Apr;38(4):226-32.
[55] Macran S,Wileman S, Barton G, Russell I. The development of a new
measure of quality of life in the management of gastro-oesophageal reflux
disease: the Reflux questionnaire. Qual Life Res 2007;16:331-43.
[56] AnvariM, Allen C,Marshall J, Armstrong D, Goeree R, UngarW, et al.
A randomized controlled trial of laparoscopic Nissen fundoplication versus
proton pump inhibitors for treatment of patients with chronic
gastroesophageal reflux disease: one-year follow-up. Surg Innov
2006;13:238-49;

101
[57] Coster DD, Bower WH, Wilson VT, et al. (1997) Laparoscopic partial
fundoplication versus laparoscopic Nissen–Rosetti fundoplication. Short-
term results of 231 cases. Surg Endosc
11:625–631
[58] D’Alessio MJ, Arnaoutakis D, Giarelli N, Villadolid DV, Rosemurgy
AS. Obesity is not a contraindication to laparoscopic Nissen
fundoplication. J Gastrointest Surg 2005; 9 (7): 949-54.
[59] Sampliner R E, Practice Parameters Committee ACG.Updated
guidelines for the diagnosis, surveillance, and therapy of Barrett’s
esophagus. Am J Gastroenterol 2002; 97: 1888–95.
[60] Brown L M, Devesa S S. Epidemiologic trends in esophageal and
gastric cancer in the United States. Surg Oncol Clin N Am 2002; 11: 235–
56.
[61] Eisen G M. Ablation therapy for Barrett’s esophagus.Gastrintest
Endosc 2003; 58: 760–9.
[62] Parilla P, Martinez de Haro L, Ortiz A et al. Long-term results of a
randomized prospective study comparing medical and surgical treatment of
Barrett’s esophagus. Ann Surg 2003; 237: 291–8.

102
[63] Dulai G S, Jensen D M, Cortina G, Fontana L, Ippoliti A.Randomized
trial of argon plasma coagulation versus multipolar electrocoagulation for
ablation of Barrett’s esophagus. Gastrintest Endosc 2005; 61: 232–40.
[64] Ackroyd R, Tam W, Schoeman M, Devitt P G, Watson D I.Prospective
randomized controlled trial of argon plasma coagulation ablation vs.
endoscopic surveillance of patients with Barrett’s esophagus after
antireflux surgery. Gastrintest Endosc 2004; 59: 1–7.
[65] Hage M, Siersema P D, van Dekken H et al. 5-aminolevulinic acid
photodynamic therapy versus argon plasma coagulation for ablation of
Barrett’s oesophagus: a randomised trial. Gut
2004; 53: 785–90.
[66] Zeman Z, Rozsa S, Tihanyi T, Tarko E.Psychometric documentation of
a quality-of-life questionnaire for patients undergoing antireflux surgery
(QOLARS). Surg Endosc 2005; 19: 257–
61.
[67] Tarun Singhal*, Santosh Balakrishnan, Abdulzahra Hussain, Starlene
Grandy-Smith, Andrew Paix and Shamsi El-Hasani Management of
complications after laparoscopic Nissen's fundoplication: a surgeon's
perspective Annals of Surgical Innovation and Research 2009, 3:1 ;

103
[68] Zacharoulis D, O’Boyle CJ, Sedman PC, Brough WA, Royston
CMS.Laparoscopic fundoplication: a 10-year learning curve. Surg Endosc
2006;20:1662-70

104