1/33 OSSIDAZIONE DI RAME METALLICO. PREPARAZIONE DI OSSIDO DI RAME DI RAME (I). DISMUTAZIONE DELLO...
-
Upload
ladislas-pala -
Category
Documents
-
view
257 -
download
6
Transcript of 1/33 OSSIDAZIONE DI RAME METALLICO. PREPARAZIONE DI OSSIDO DI RAME DI RAME (I). DISMUTAZIONE DELLO...

1/33
OSSIDAZIONE DI RAME METALLICO. OSSIDAZIONE DI RAME METALLICO. PREPARAZIONE DI OSSIDO DI RAME DI PREPARAZIONE DI OSSIDO DI RAME DI RAME (I). DISMUTAZIONE DELLO IONE RAME (I). DISMUTAZIONE DELLO IONE RAMEOSO. RAMEOSO. ELETTROLISI DEL RAME ELETTROLISI DEL RAME METALLICO.METALLICO.
1a ESPERIENZA

2/33
Osservare la chimica acquosa del rame nei suoi aspetti più importanti.
Condurre reazioni acido-base, di ossido-riduzione, di complessamento in cui è coinvolto il rame nei suoi stati di ossidazione più comuni (0,+1,+2);
Riflettere su diversi argomenti spiegati nel corso di Chimica Generale ed Inorganica: equilibrio mobile, potenziali di ossido-riduzione, elettrolisi, stechiometria ecc.;
OBIETTIVI

3/33
Ogni singola operazione che viene eseguita nel corso della esperienza ha uno scopo (teorico o pratico) ben preciso. Lo studente dovrebbe sforzarsi di trovare (o chiedere) una spiegazione per ognuna di esse.

4/33
50% ridotto Zn
Cu
50% precipitatoNaOH
Cu(OH)2
CuCl2
Lavato e sciolto con HCl
Le due parti unitecomproporzionamentosi ottiene rame(I)
In ambiente acido(acido solforico)disproporzionamento
CuRame(II) ridotto con Zn
Schema della parte “chimica”
CuCl
II) Preparazione ossido di rame(I)comproporzionamento
CuCu2+50% 50%
III) Ritorno al rame metallico(disproporzione)
Cu
I) Preparazione rame(II) solfato(ossidazione)Ossidazione
acido nitrico
CuSO4
Ambiente moderatamentebasico
Cu2O

5/33
3Cu(s) + 2HNO3 + 3H2SO4 3CuSO4 + 2NO(g)
+4H2O
2 NO(g)+O2 2 NO2(g)
2 NO2(g) N2O4Come si bilancia la reazione ? (salta)A cosa serve l'acido nitrico ?Non basta usare solo l'acido solforico ?
Parte prima Parte prima Preparazione del solfato di rame Preparazione del solfato di rame
pentaidratopentaidrato ( ( OssidazioneOssidazione del rame metallico a del rame metallico a
CuCu2+2+))

6/33
Cu(s) +HNO3 +H2SO4 CuSO4 +NO(g)+H2O
Bilanciamento della reazione di ossido-riduzione (1)
1) Individuare le specie che cambiano numero di ossidazione
0 2
Aumenta - ossidazione
5 2
Diminuisce - riduzioneGli altri non cambianoH +1, S +6 , O-2
2) Separare le due semireazioni
Cu Cu2+ ossidazione – si producono elettroni
HNO3 NO riduzione - si consumano elettroni
3) Bilanciamento delle due semireazioni (elettroni come reagenti o prodotti)
Ci deve essere sempre almeno una semireazione di riduzione e una di ossidazione

7/33
3-r) Bilanciamento della reazione di riduzione
A) Bilanciare la massa dell'elemento che si riduce (Ok) B) Aggiungere elettroni tra i reagenti per compensare il cambio di numero di ossidazione (52, 3 elettroni reagenti)C) Bilanciare la massa degli altri elementi senza cambiare il loro stato di ossidazioneIn soluzione acida si introduce (se necessario) acqua e ioni H+
HNO3 NO
HNO3 +3e NO
HNO3 +3e NO +2H2O
HNO3 +3e +3H+ NO +2H2O
D) Al termine verificare che è stato rispettato il bilancio di carica 0 = 0 (Ok)
Bilanciato l'ossigeno introducendo 2 molecole d'acqua
Bilanciato l'idrogeno introducendo 3 ioni H+

8/33
3-o) Bilanciamento della reazione di ossidazione
A) Bilanciare la massa dell'elemento che si riduce (Ok) B) Aggiungere elettroni tra i reagenti per compensare il cambio di numero di ossidazione (02, 2 elettroni prodotti)C) Bilanciare la massa degli altri elementi senza cambiare il loro stato di ossidazione (Ok)
Cu Cu2+
Cu Cu2+ + 2e
D) Al termine verificare che è stato rispettato il bilancio di carica 0 = 0 (Ok)
Ox) Cu Cu2+ + 2e
Rid) HNO3 +3e +3H+ NO +2H2O

9/33
4) Ricomporre la reazione complessiva in modo che non compaiano gli elettroni
Ox) Cu Cu2+ +2e
Rid) HNO3 +3e +3H+ NO +2H2O
3 x
2 x
Minimo comune multiplo
3Cu + 2HNO3 +6H+ 3Cu2+ + 2NO +4H2O3Cu + 2NO3
- +8H+ 3Cu2+ + 2NO +4H2O
Scritta in forma ionica
5) Completare la reazione inserendo le specie (ioniche) mancanti
3Cu(s) + 2HNO3 + 3H2SO4 3CuSO4 + 2NO(g)+4H2O
Inserendo sia tra i reagenti che tra i prodotti 3 ioni solfato e raggruppando

10/33
Alcuni metalli sono ossidati dallo ione H+. Il rame è un metallo nobile, per ossidarlo si deve usare qualcosa di più forte: acido nitrico concentrato (un acido "ossidante")
2H+ + 2e H2(g)
Per acidi come l'acido solforico l'ossidante è H+
E= -0.059 pH222
22 ][log
2
0592.0][log
2
0592.0
HHH
H p
H
p
HEE
Al3+ +2e Al(s) E°=-1.66 VZn2+ +2e Zn(s) E°=-0.76 V2H+ + 2e H2(g) E°= 0 V (per definizione è il riferiemento)
Cu2+ +2e Cu(s) E°= 0.31 VAg+ + e Ag(s) E°= 0.80 V
H+ non è in grado di ossidare i metalli nobili E°> 0
La forza di un ossidante può essere espressa da una forza elettromotrice, il potenziale ossido-riduttivo (E)
Si
No

11/33
4H+ + NO3- + 3e NO(g) + H2O E°=~ 0.96 V
L'acido nitrico (acido ossidante)
Il potenziale red-ox dipende dal pH

12/33
L’ ossido di azoto che si forma (NO) si ossida all’ ariaper dare biossido di azoto NO2 un gas di colore brunoche è in equilibrio col suo dimero tetraossido di diazotoN2O4 incolore.
3Cu(s) + 2HNO3 + 3H2SO4 3CuSO4 + 2NO(g)
+4H2O
2 NO(g)+O2 2 NO2(g)
2 NO2(g) N2O4
L’acido solforico ha due funzioni:Fornisce ioni solfato e accresce l’acidità della soluzione
VAPORI BRUNI

13/33
Preparazione dell’ossido rameosoPreparazione dell’ossido rameoso(Composti di rame(I) per comproporzionamento di rame(II) e rame (Composti di rame(I) per comproporzionamento di rame(II) e rame
metallico)metallico)
Il rame(I) non è stabile in acqua: disproporziona (dismuta)
2 Cu+ Cu + Cu2+ K=~106
Per ottenere composti di rame(I) in soluzione acquosa per dismutazione del rame(II) bisogna fare due cose:
aggiungere rame metallico in rapporto stechiometrico;sottrarre all’equilibrio in modo opportuno lo ione rameoso.
disproporzionamento
E' possibile preparare composti di rame(I) in acqua ?
comproporzionamento

14/33
2 Cu+ Cu + Cu2+
Complessamento oFormazione di composti poco solubili
Lo ione rameoso forma precipitati e complessi con gli ioni alogenuri e pseudo-alogenuri:CuI; CuCN; CuCl;CuBr – CuI2
- ; CuCl2- ecc..

15/33
Il rame solfato (soluzione) viene divisa in due parti uguali (per ottenere il rapporto stechiometrico)
Cu2+ + 2OH- Cu(OH)2(s)
lavaggio
A – si elimina lo ione solfato (sostituito dal cloruro)
Cu(OH)2(s) + 2HCl Cu2+ + 2Cl- + 2H2O

16/33
B – si riduce il rame(II) a rame metallico
Cu2+ + Zn(s) Zn2+ + Cu(s)
A+B –> comproporzionamento in presenza di un eccesso di ione cloruro
Cu2+ + Cu(s) +4Cl- 2CuCl2-
CuCl2- CuCl(s) + Cl-
E°(Cu2+/Cu) = 0.31 VE°(Zn2+/Zn) = -0.76 V

17/33
In ambiente debolmente basico si forma l’ossido rameoso (ossidulo di rame)
2CuCl(s) +2OH- Cu2O(s) + 2Cl-

18/33
Cu2O(s) + 2H+ Cu+ + H2O
2Cu+ Cu(s) + Cu2+
Cu2+ + Zn(s) Zn2+ + Cu(s)
Posso acidificare con HCl ?
Disproporzione dello ione rameosoDisproporzione dello ione rameosoSi torna indietroSi torna indietro

19/33
~5g di rame
Coperti con 25 ml d'acquaaggiunta ~ 10 ml H2SO4 conc.;aggiunta ~ 10 ml HNO3 conc.;
Riscaldamento fino a scomparsa dei vapori bruni e riduzione a piccolo volume.Filtrazione su gooch (2) e lavaggio con poca acqua (~0°C) e acetone.
CuSO4 5H2O CALCOLO DELLA RESA %Purificazione e titolazioneProseguire con la seconda parte
Note
Sotto cappa
Il solfato di rame pentaidrato è azzurro, quello anidro è bianco
Non aggiungere acetone prima diAvere lavato con acqua;Il solfato di rame pentaidrato è molto solubile in acqua. Non eccedere
Volume Beaker ~ 150 cm3
3Cu(s) + 2HNO3 + 3H2SO4 3CuSO4 + 2NO(g)+4H2O
Usare la massa molare corretta (ricordare le molecole d'acqua)
PARTE SPERIMENTALE -1PARTE SPERIMENTALE -1

20/33
~5g di CuSO4 5H2Oin 100 ml di soluzione
Soluzione A50 ml trattati con NaOH 1.0 M
Soluzione B50 ml trattati con Zn in granuli
Cu(OH)2 filtrato su carta. Lavato e sciolto con HCl
Zn in eccessprimosso.Rame filtrato e lavato
Alla soluzione di CuCl2 (A) viene aggiunto il rame in polvere (B)
Soluzione di CuCl2- che viene diluita
per dare CuCl(s). La sospensione va alla parte III.
Note
Usare granuli di zinco grandi
Lavare fino alla scomparsa dello ione solfato. Controllare l' assenza con soluzione BaCl2
PARTE SPERIMENTALE - 2PARTE SPERIMENTALE - 2

21/33
La sospensione di CuCl
Viene aggiunta una soluzione di tetraborato sodico. Il tutto viene fatto bollire ~30 min
Il precipitato marrone (Cu2O) filtrato e lavato viene usato nella parte IV
Note
Non lasciare tutta la notte il precipitato bagnato sul gooch (in parte si ossida all'aria (rame(II)))
PARTE SPERIMENTALE - 3PARTE SPERIMENTALE - 3

22/33
Note
Cu2O inumidito
Trattato con H2SO4 diluito a caldo.Filtrazione e lavaggio con acqua.
Soluzione filtrata alla parte V.
Residuo (Cu metallico)CALCOLARE LA RESA % Aggiungere al prodotto della parte V
Il trattamento con HCl avrebbe portato allo stesso risultato ?
PARTE SPERIMENTALE - 4PARTE SPERIMENTALE - 4

23/33
Soluzione di Cu2+
Trattata con NaOH e poi con Zn metallico in granuli (come gia fatto in precedenza)
Unire con il rame proveniente dalla parte precedente. CALCOLARE LA RESA % Globale
Residuo (Cu metallico) lavato e filtrato. CALCOLARE LA RESA %
Note
Se ottenete le due rese parziali molto diverse cercate di dare una spiegazione.
Perché devo neutralizzare la soluzione?
PARTE SPERIMENTALE - 5PARTE SPERIMENTALE - 5

24/33
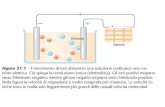
Anodo (+) ossidazione
Cu Cu2+ + 2e
Catodo (-) riduzione
2H+ + 2e H2
ELETTROLISI DEL RAME METALLICOELETTROLISI DEL RAME METALLICO

25/33
Cu2+
H2,(NH3)
NH4Cl, 2 mol dm-3
Evitare che i morsetti tocchinole soluzioni
La presenza di bolle impedisce il contatto elettrico
PARTE SPERIMENTALEPARTE SPERIMENTALE

26/33
Questioni aperte:
Cosa altro si può ossidare?Cosa altro si può ridurre?Perché si libera idrogeno ?Perché si sente, dopo un po' di odore di ammoniaca ?
Suggerimenti:- altre specie presenti: H2O (OH-), NH4
+,NH3, Cu2+(?), Cl- - osservare tutte le specie che si possono ridurre; confrontare il potenziale di ossido riduzione.- E' presente in soluzione ione ammonio (NH4
+); verificare le sue proprietà acido base.

27/33
?Domand
e

28/33
Preparazione di una soluzione - Calcoli
- Necessari volume (V) della soluzione da preparare, concentrazione molare (CA) e massa molare (MMA) della sostanza A
Primo caso la sostanza pura, si può pesare (è un solido)1) Calcolare le moli (nA) necessarie: dalla definizione di molarità
nA = CA V2) Ottenere la quantità (mA) da pesare (definizione di massa molare)
mA = MMA nA
Prendere un matraccio pulito di volume V, versare la sostanza sul fondo e aggiungere acqua in modo che il volume finale della soluzione raggiunga la linea che si trova sul collo del recipiente

29/33
Calcoli per preparare una soluzione (2)
Secondo caso la sostanza A non si può pesare (è una soluzione liquida con una certa percentuale di A (%A)
1) Calcolare le moli (nA) necessarie (come prima)nA = CA Vsol
2) Ottenere la massa di A (mA) necessaria (come prima) mA = MMA nA
Serve anche la densità della soluzione liquida dsolA
3) Calcolare la massa di soluzione msolA (A e H2O) necessaria (dalla definizione di percentuale)
msolA = 100 mA / %A
4) Calcolare il volume da prelevare (VsolA) necessaria nota la densità della soluzione (dalla definizione di densità)
VsolA = msolA / dsolA

30/33
Un sistema all'equilibrio risponde ad una perturbazione spostando l'equilibrio nelladirezione che minimizza la perturbazione stessa.
Dissoluzioneendotermica
Dissoluzioneesotermica
si scioglieancora
Purificazione del solfato di rame (II) pentaidratoper re-cristallizzazione "caldo-freddo"
Il solfato di rame(II) è molto più solubile a caldo che a freddoTutti le sostanze che si sciolgono in un solvente assorbendo calore (reazione endotermica) aumentano la solubilità al crescere della temperatura. Questa è una conseguenza del principio di "Le Chatelier – vant'Hoff"
Riscaldamento Riscaldamento Cresce il precipitato

31/33

32/33
Determinazione del numero di molecole d'acqua di cristallizzazione
x = numero di molecole d'acqua di idratazione CuSO4
xH2OMM(CuSO4,idrato) = MM(CuSO4) + x MM(H2O)
x = (MM(CuSO4,idrato) - MM(CuSO4)) / MM(H2O)
Dalla definizione di MM = m/n
Trovare quante moli ci sono in una quantità nota di solfato di rame
moli solfato di rame(II) = moli di Cu2+
Titolare il rame(II) in una quantità (massa) nota di solfato di rame

33/33
Titolazione iodometrica del rame(II)
2Cu2+ + 4I- 2CuI + I2
Aggiungendo ad una soluzione di Cu2+ un eccesso di ione ioduro (sotto forma di KI) si ha la seguente reazione di ossido-riduzione:
Reazione quantitativa n(Cu2+) = 2 n(I2)
Lo iodio si titola facilmente con tiosolfato sodico:
2S2O32- + I2 S4O6
2- + 2I-
oppure
2S2O32- + I3
- S4O62- + 3I-
Al punto equivalente n(S2O32-) = 2n(I2) = n(Cu2+)
Altra reazione di ossido-riduzione